Clear Sky Science · fr
Les synthases de signal de quorum à double fonction DspII et DspI coordonnent l’interrupteur de virulence chez Pseudomonas aeruginosa
Comment un super-bactérie hospitalière change sa stratégie d’attaque
Pseudomonas aeruginosa est un microbe hospitalier notoire capable de provoquer des infections pulmonaires et des plaies tenaces, en particulier chez les patients vulnérables. Il survit en alternant entre deux modes de vie : une communauté protégée et à croissance lente appelée biofilm, et une forme mobile et agressive qui envahit les tissus. Cette étude révèle comment la bactérie décide elle-même de rompre un biofilm de longue durée et de lancer une attaque aiguë soudaine, mettant au jour de nouvelles vulnérabilités potentielles pour de futurs traitements.
Une vie microbienne entre cachette et attaque
De nombreuses infections bactériennes se déroulent en plusieurs phases. Au début, des cellules librement mobiles se propagent dans l’organisme et déploient des armes puissantes qui endommagent les tissus de l’hôte. Plus tard, elles s’installent souvent en biofilms — des couches épaisses et visqueuses adhérant à des surfaces telles que des cathéters, le tissu pulmonaire ou des plaies. Dans ces communautés, les cellules sont enveloppées dans une matrice protectrice qui les rend difficiles à éliminer par les antibiotiques ou les défenses immunitaires. Pourtant, le biofilm n’est pas une impasse : les cellules peuvent en partir, retrouver leur motilité et déclencher de nouveaux épisodes d’infection aiguë ailleurs. Jusqu’ici, on ignorait comment Pseudomonas aeruginosa coordonne activement ce passage de la persistance chronique à la maladie agressive.
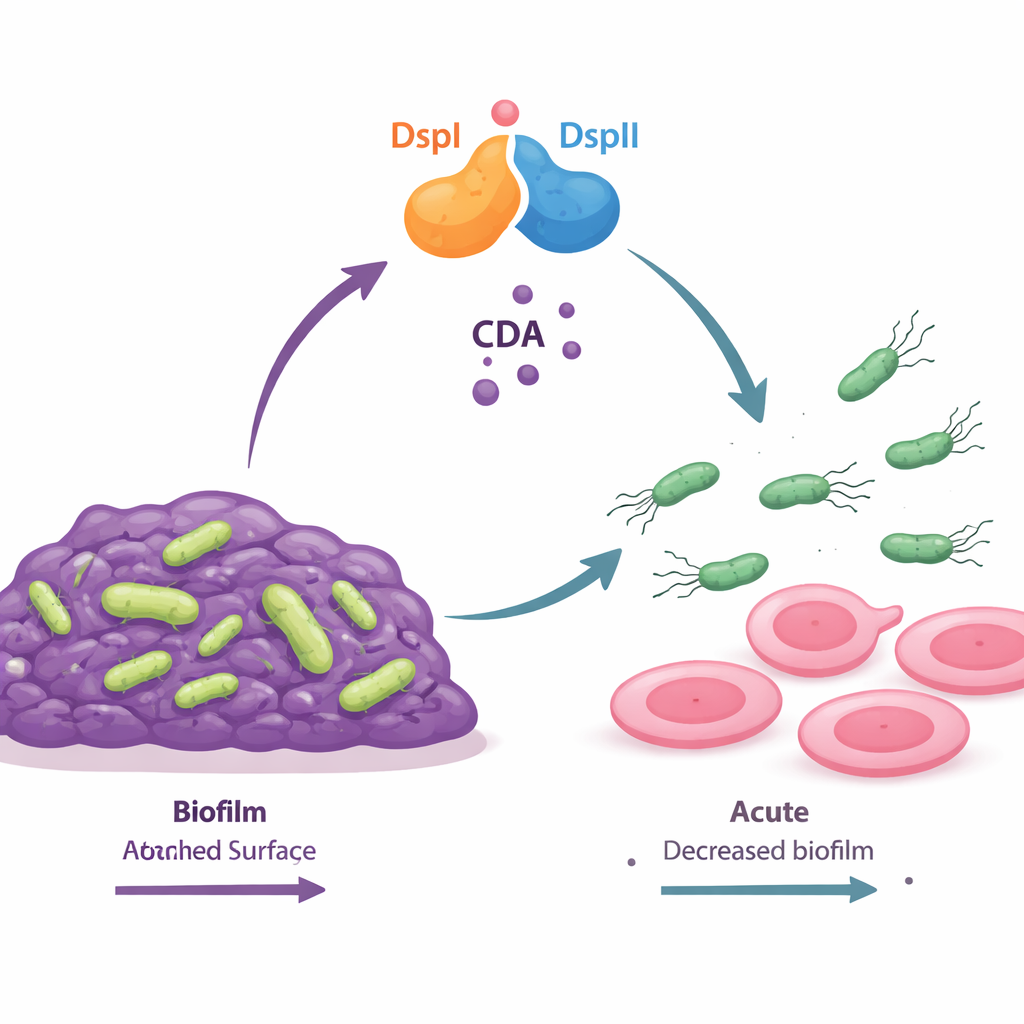
Un interrupteur à deux protéines qui fabrique un signal chimique « go »
Les auteurs ont découvert que deux protéines bactériennes, nommées DspI et DspII, fonctionnent ensemble comme une sorte d’interrupteur moléculaire. Les deux sont des enzymes du même type général et sont positionnées côte à côte dans le génome bactérien, s’exprimant simultanément à mesure que la population s’épaissit. Lorsqu’elles forment un couple, elles synthétisent un petit acide gras signal appelé cis-2-décénoïque (CDA), appartenant à un groupe plus large de molécules de communication connues sous le nom de signaux DSF. Les mutants dépourvus de DspI ou de DspII ne pouvaient plus produire de CDA, formaient des biofilms anormalement épais et perdaient leur capacité à ramper sur les surfaces. Ce n’est que lorsque les deux protéines étaient restaurées ensemble que les cellules retrouvaient une production normale du signal, la dispersion des biofilms et la motilité, montrant que les deux enzymes fonctionnent comme une équipe interdépendante.
Du signal chimique au mouvement et à l’évasion
Le CDA n’agit pas seul ; il s’intègre au circuit interne de la bactérie. L’équipe a montré que le CDA abaisse les niveaux d’un autre messager, le cyclic di‑GMP, en augmentant l’activité d’une enzyme spécifique appelée RbdA qui dégrade ce messager. Un taux élevé de cyclic di‑GMP favorise normalement la formation de biofilm en stimulant la production d’une matrice sucrée et en réprimant les flagelles, ces minuscules propulseurs qui assurent la nage. En présence de CDA, les niveaux de cyclic di‑GMP chutent, un régulateur nommé FleQ change de mode, la production de sucres adhésifs diminue et les flagelles sont étendus et renforcés. En conséquence, les biofilms se relâchent et les cellules retrouvent la capacité de se déplacer, colonisant de nouveaux territoires.
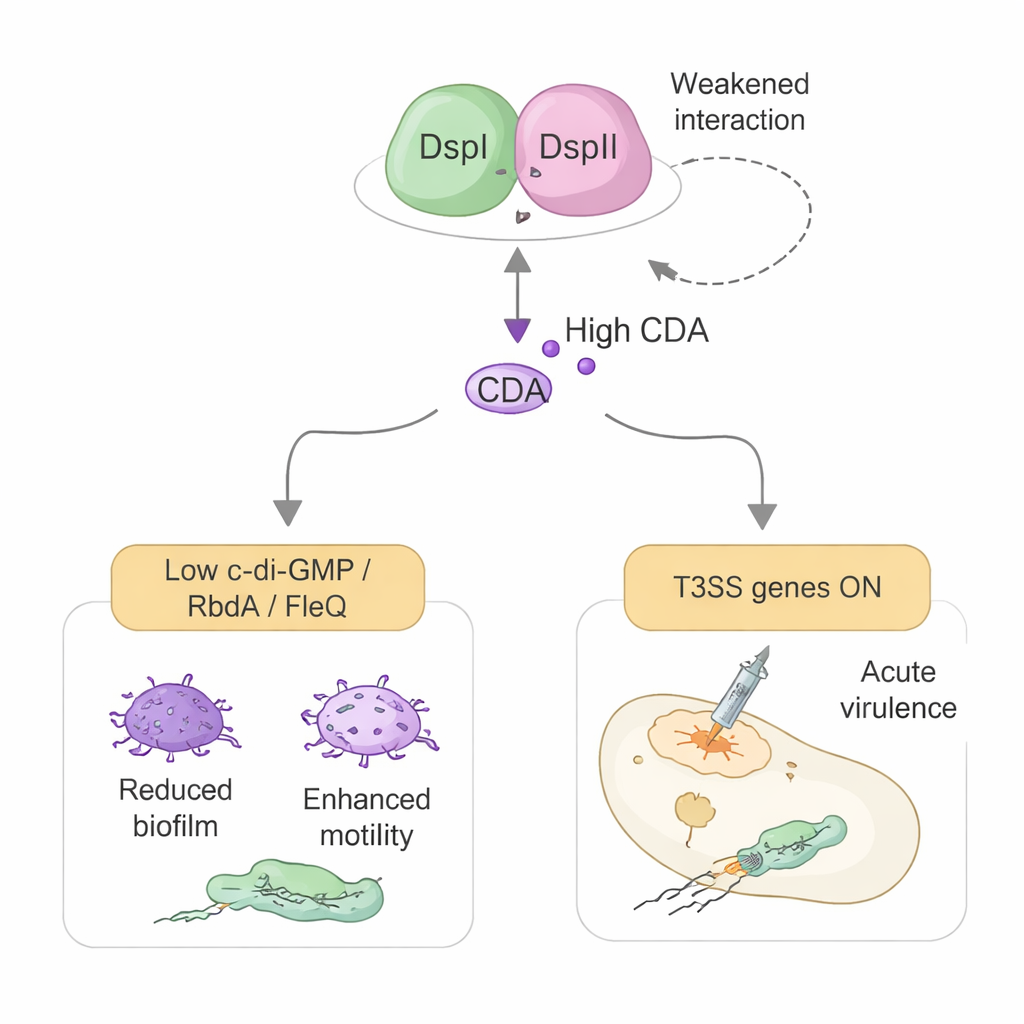
Reprogrammation du système d’armes bactérien
L’étude révèle également un second rôle inattendu de DspI et DspII qui dépasse la simple chimie. Le même couple protéique aide à activer le système de sécrétion de type III (T3SS) de la bactérie, un dispositif en forme de seringue utilisé pour injecter des toxines directement dans les cellules hôtes. Plutôt que d’agir via le CDA, cet effet se fait par un contrôle direct des commutateurs génétiques. DspI et DspII réduisent la production de deux petits ARN régulateurs, RsmY et RsmZ, qui inhibent normalement la fabrication des protéines du T3SS. Ils le font en se liant à la région de contrôle de l’ADN d’un de ces ARN et en interagissant physiquement avec une protéine régulatrice maîtresse appelée GacA. Lorsque RsmY et RsmZ sont maintenus en échec, un activateur en aval nommé RsmA est libéré, et les gènes du T3SS ainsi que son contrôleur maître ExsA sont activés, augmentant la cytotoxicité en culture cellulaire et la mortalité dans un modèle d’infection chez l’insecte.
Un système auto-ajustable avec des cibles médicamenteuses
Astucieusement, la force du partenariat DspI–DspII et son contrôle de la virulence sont eux-mêmes réglés par les niveaux de CDA. À faibles concentrations — comme celles attendues chez les cellules quittant un biofilm — le CDA renforce l’interaction entre les deux protéines et favorise une production accrue de signal et l’activation du T3SS. À fortes concentrations à l’intérieur des biofilms denses, le CDA affaiblit leur interaction et réduit leur liaison à l’ADN, limitant la synthèse de signal supplémentaire et la production coûteuse d’armes chez les cellules qui restent en place. Ce double rôle fait du complexe DspI–DspII un point central reliant la taille de la population, l’évasion du biofilm et la virulence aiguë. Parce que perturber ce complexe peut bloquer à la fois la production de signal et l’activation du système de toxines, il constitue une cible attractive pour de futurs médicaments visant à maintenir Pseudomonas dans un état chronique moins nocif et prévenir des flambées dangereuses.
Citation: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Mots-clés: Pseudomonas aeruginosa, dispersion de biofilm, quorum sensing, interrupteur de virulence, cis-2-décénoïque