Clear Sky Science · fr
Un stimulateur vagal triboélectrique entièrement dégradable pour atténuer le remodelage cardiaque et l’insuffisance cardiaque à différents stades
Pourquoi un dispositif cardiaque dissolvable compte
L’insuffisance cardiaque est une maladie fréquente et mortelle, touchant des dizaines de millions de personnes et conduisant souvent à des années de fatigue, d’essoufflement et d’hospitalisations répétées. Les médecins savent qu’une stimulation douce d’un nerf majeur, le nerf vague, peut aider le cœur en défaillance, mais les implants actuels sont volumineux, alimentés par batterie et doivent être retirés ou remplacés chirurgicalement. Cette étude présente un stimulateur minuscule et flexible qui s’alimente des mouvements du corps puis se dissout en toute sécurité à l’intérieur de l’organisme après le traitement, ouvrant la voie à des thérapies à court terme et personnalisées sans interventions supplémentaires.
Une manière plus douce d’utiliser le câblage du corps
Le nerf vague s’étend du cerveau vers de nombreux organes et aide à équilibrer les systèmes de stress et de relaxation du corps. Dans l’insuffisance cardiaque, cet équilibre bascule vers une activation permanente du mode « combat ou fuite », ce qui aggrave les lésions cardiaques. La stimulation vagale de faible intensité (LL-VNS) délivre des signaux trop faibles pour ralentir le cœur ou perturber son rythme, mais suffisamment forts pour restaurer une partie de cet équilibre et réduire l’inflammation nuisible. Les essais cliniques antérieurs utilisant des stimulateurs classiques alimentés par batterie ont montré que la LL-VNS pouvait améliorer les symptômes et la qualité de vie, mais le matériel lui-même posait problème : autonomie limitée, nécessité d’opérations de remplacement et présence prolongée de corps étrangers dans l’organisme.
Un dispositif auto-alimenté qui disparaît
Pour résoudre ces problèmes, les chercheurs ont conçu un nanogénérateur triboélectrique entièrement biodégradable, ou BTENG, qui convertit de légers mouvements mécaniques en électricité. Le dispositif est composé de couches de polymères biodégradables courants et de films métalliques fins, scellés dans un enrobage protecteur. Lorsque les couches se touchent et se séparent—mouvements induits par de petites oscillations—des charges électriques s’accumulent et sont dirigées vers une manche qui entoure le nerf vague. En laboratoire, le BTENG a produit de façon fiable des tensions d’environ 9 volts et des courants d’environ 4 microampères, suffisants pour correspondre au niveau de stimulation sûr établi chez la souris. La sortie est restée stable sur des milliers de cycles et pendant au moins quatre semaines dans un milieu rempli de fluide similaire à l’environnement corporel. Après le traitement, une impulsion d’ultrasons médicaux peut fissurer l’enrobage extérieur et accélérer la dégradation de l’appareil, le réduisant en fragments inoffensifs que l’organisme élimine progressivement. 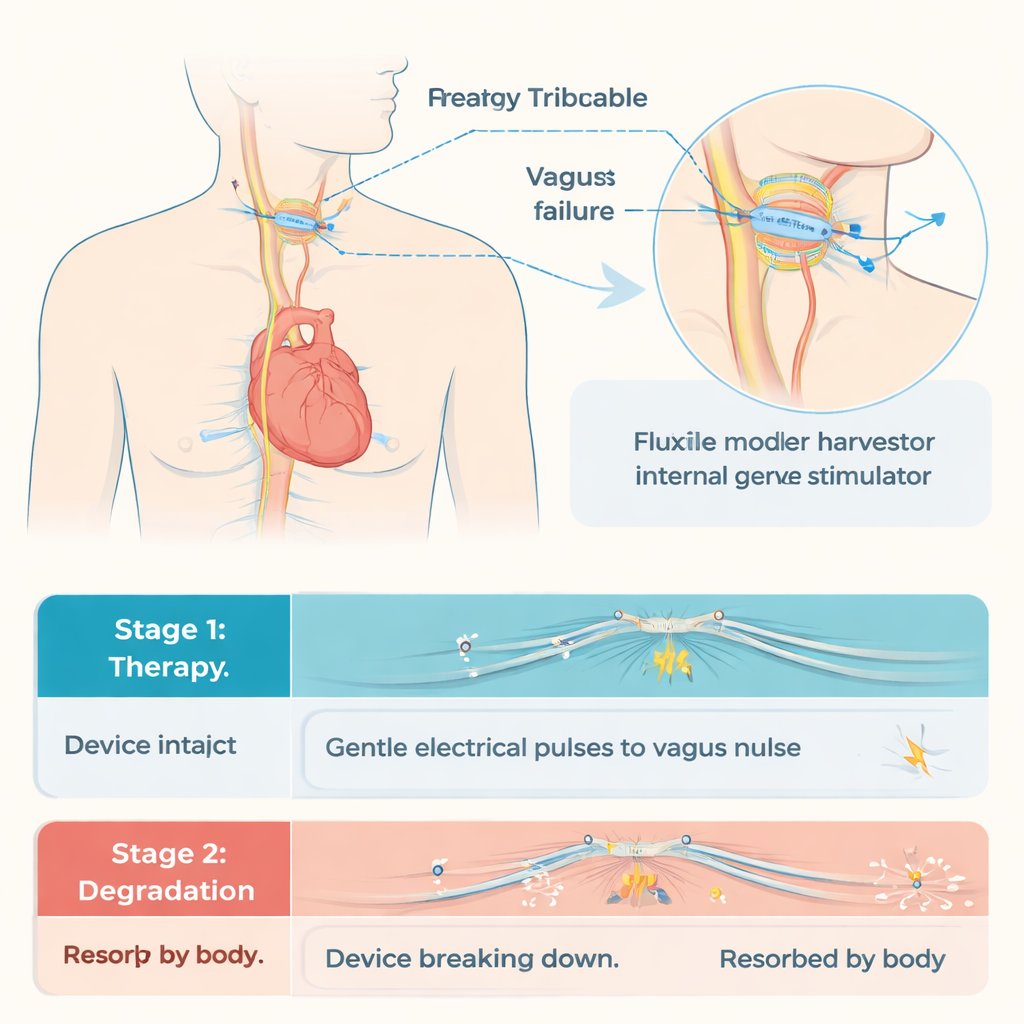
Protéger et réparer le cœur en défaillance
L’équipe a testé le système sur un modèle murin d’insuffisance cardiaque causée par une surcharge de pression à long terme du cœur, semblable à ce qui se produit en cas d’hypertension artérielle sévère ou de rétrécissement des valves cardiaques. Ils ont commencé la LL-VNS à trois stades différents : très tôt (avant des lésions majeures), après un épaississement précoce du muscle cardiaque, et après l’apparition d’une insuffisance cardiaque complète. Dans les trois scénarios, les souris ayant reçu une stimulation quotidienne de faible intensité via le BTENG présentaient une meilleure fonction de pompage, moins d’élargissement cardiaque et moins de tissu cicatriciel que les animaux non traités ou ceux qui avaient subi la chirurgie et l’implant sans stimulation. Des mesures telles que la fraction d’éjection, la congestion pulmonaire et le rapport poids cardiaque/poids corporel se sont toutes améliorées, montrant que la thérapie pouvait non seulement ralentir les lésions mais aussi les inverser partiellement, même lorsqu’elle était commencée tardivement.
Comment les signaux nerveux remodèlent la biologie cardiaque
Pour comprendre comment un petit signal électrique pouvait produire des effets aussi étendus, les chercheurs ont examiné le tissu cardiaque au niveau génétique. Ils ont découvert que la LL-VNS modifiait l’activité de centaines de gènes impliqués dans l’armature de soutien du cœur (la matrice extracellulaire), la structure musculaire, la mort cellulaire, la croissance et l’inflammation. Ces changements correspondaient à la baisse observée de la cicatrisation tissulaire et à l’amélioration de la santé musculaire. Comme le nerf vague communique via le messager chimique acétylcholine, l’équipe a testé si cette molécule était essentielle en bloquant ses principaux récepteurs avec le médicament atropine. Lorsque l’atropine a été administrée, les bénéfices de la LL-VNS ont disparu : la fonction cardiaque s’est détériorée, la cicatrisation a augmenté et les gènes liés à la maladie sont restés élevés. Cela a montré que la libération d’acétylcholine déclenchée par les signaux vagaux est un moteur clé des effets protecteurs sur le cœur. 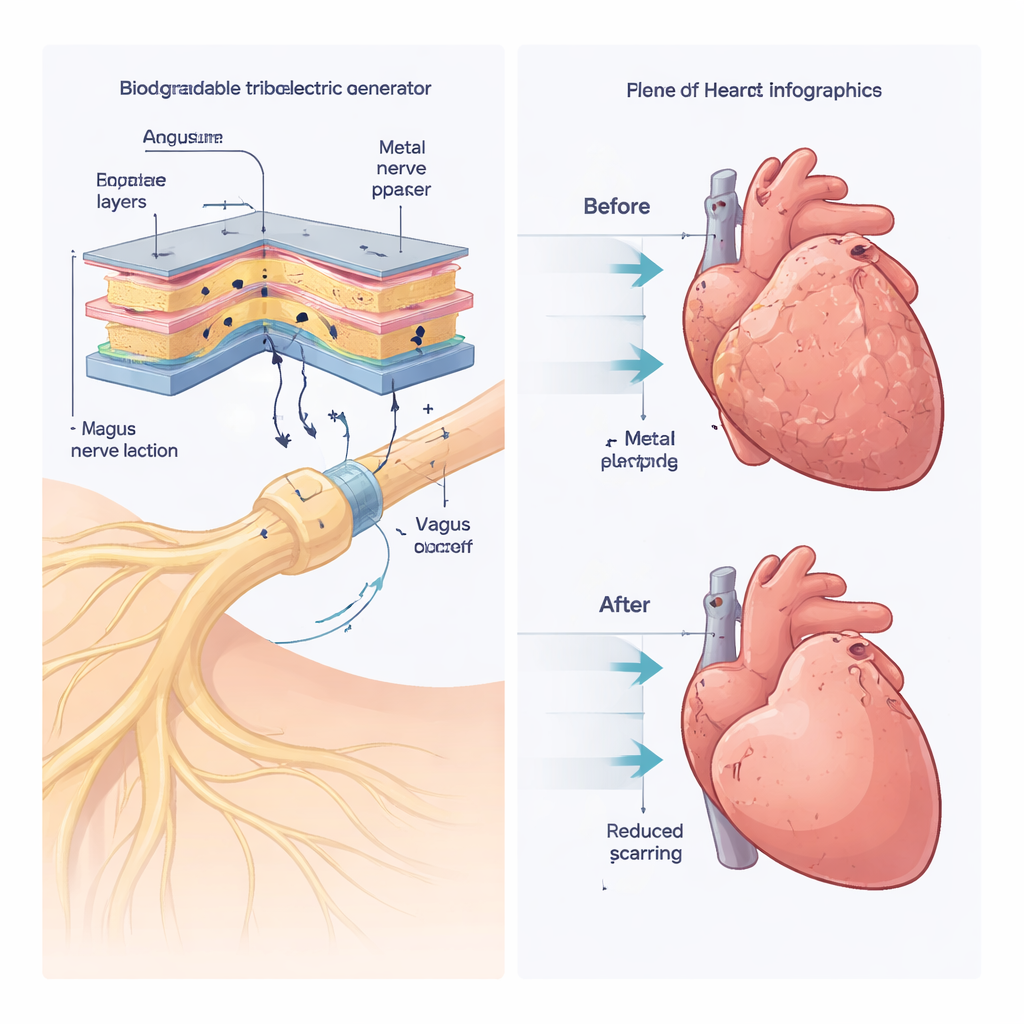
Des implants dissolvables à des soins cardiaques personnalisés
Ensemble, les résultats montrent qu’un petit stimulateur auto-alimenté et entièrement dégradable peut délivrer en toute sécurité des signaux nerveux qui empêchent ou inversent le remodelage cardiaque délétère chez la souris. Pour les patients, une version future de cette technologie pourrait être implantée uniquement pour la durée nécessaire, alimentée par leurs propres mouvements, puis effacée du corps par une simple séance d’ultrasons—sans changement de batterie ni chirurgie d’extraction. En combinant une stimulation nerveuse précise avec des matériaux intelligents qui disparaissent à la demande, cette approche ouvre la voie à une nouvelle catégorie de traitements temporaires et personnalisés de l’insuffisance cardiaque, susceptibles de réduire les complications, de diminuer les coûts et d’améliorer la qualité de vie.
Citation: Guo, Z., Chao, SY., Kong, CY. et al. A fully degradable triboelectric vagus nerve stimulator for attenuating cardiac remodeling and heart failure at different stages. Nat Commun 17, 1893 (2026). https://doi.org/10.1038/s41467-026-68619-6
Mots-clés: insuffisance cardiaque, stimulation du nerf vague, implant biodégradable, générateur triboélectrique, remodelage cardiaque