Clear Sky Science · fr
Un atlas spatialement résolu du cancer gastrique caractérise une région agrégée de lymphocytes
Pourquoi le voisinage autour d’une tumeur compte
Le cancer n’est pas simplement un amas de cellules dévoyées ; il vit dans un voisinage animé d’immunitaires et de cellules structurales qui peuvent soit aider à combattre la tumeur, soit la laisser se développer sans contrôle. Cette étude cartographie ce voisinage dans le cancer gastrique avec un niveau de détail inédit, montrant comment de petits points chauds et froids immunitaires à l’intérieur d’une même tumeur peuvent influencer la réponse d’un patient aux immunothérapies modernes.
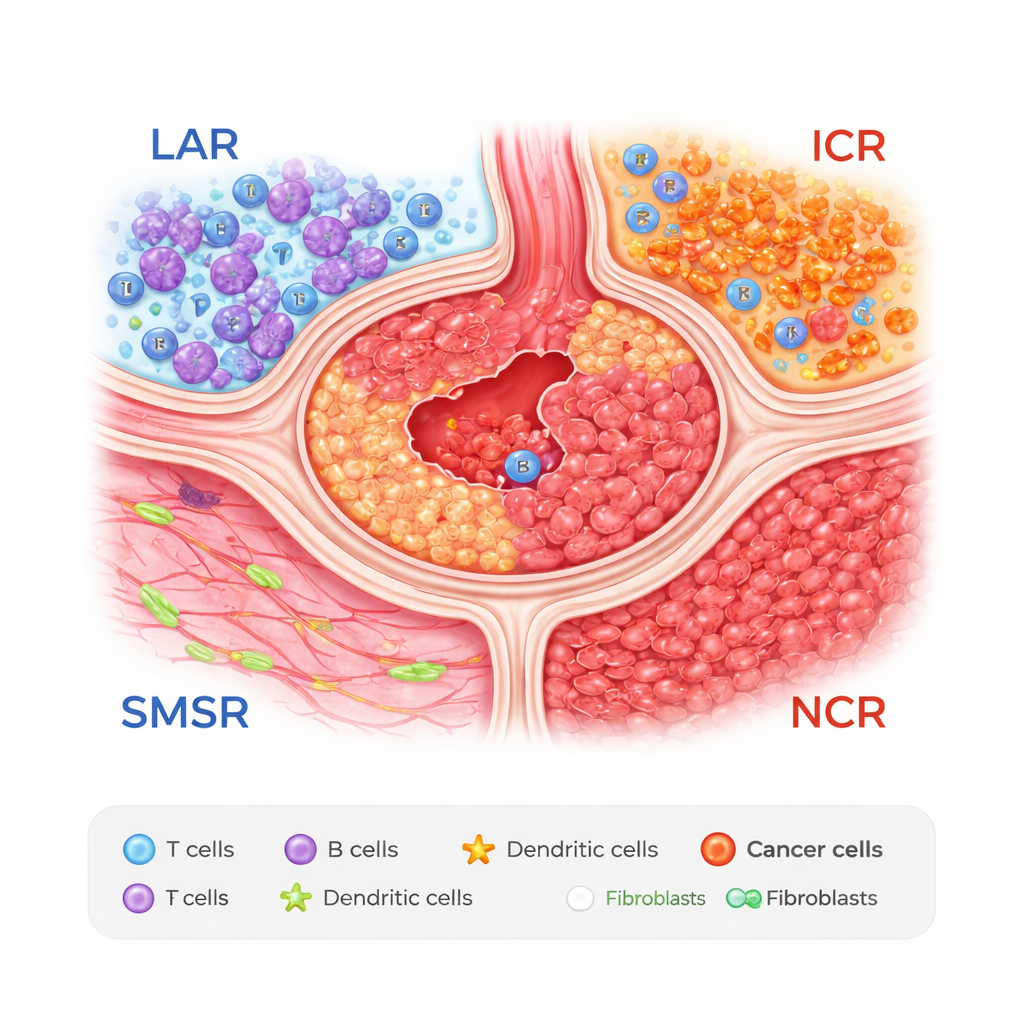
Quatre zones à l’intérieur d’une tumeur gastrique
Les chercheurs ont combiné deux outils puissants : le séquençage d’ARN unicellulaire, qui mesure l’activité génique cellule par cellule, et la transcriptomique spatiale, qui enregistre la position de ces cellules dans des coupes de tissu. En étudiant des échantillons de 27 patients, ils ont découvert que les tumeurs gastriques peuvent se diviser en quatre zones récurrentes. L’une est une région agrégée de lymphocytes (LAR), riche en amas de cellules T et B qui ressemblent à de petits ganglions lymphatiques. Une autre est une région de muscle lisse et stroma (SMSR), dominée par le muscle et le tissu conjonctif. Les deux zones restantes sont des zones denses en cancer : une région tumorale immunogénique (ICR), où les cellules tumorales se mêlent à certains types cellulaires protecteurs de l’estomac, et une région tumorale négativement immunogénique (NCR), remplie de cellules malignes et contenant relativement peu de cellules immunitaires défensives.
Les points chauds immunitaires liés à de meilleurs résultats
L’équipe a constaté que la zone LAR est enrichie en gènes habituellement exprimés dans les ganglions lymphatiques, où les cellules immunitaires sont entraînées et activées. Cela inclut des signaux qui favorisent le recrutement des lymphocytes et leur organisation en structures appelées structures lymphoïdes tertiaires. En analysant de larges jeux de données publics sur le cancer, les tumeurs présentant une expression plus élevée de gènes liés à la LAR avaient tendance à présenter une meilleure survie des patients et une probabilité légèrement plus élevée de répondre aux thérapies anti-points de contrôle qui lèvent le frein sur les cellules T. En revanche, les signatures géniques provenant de régions riches en muscle ou fortement cancéreuses étaient généralement associées à des pronostics plus défavorables dans plusieurs types de cancer.
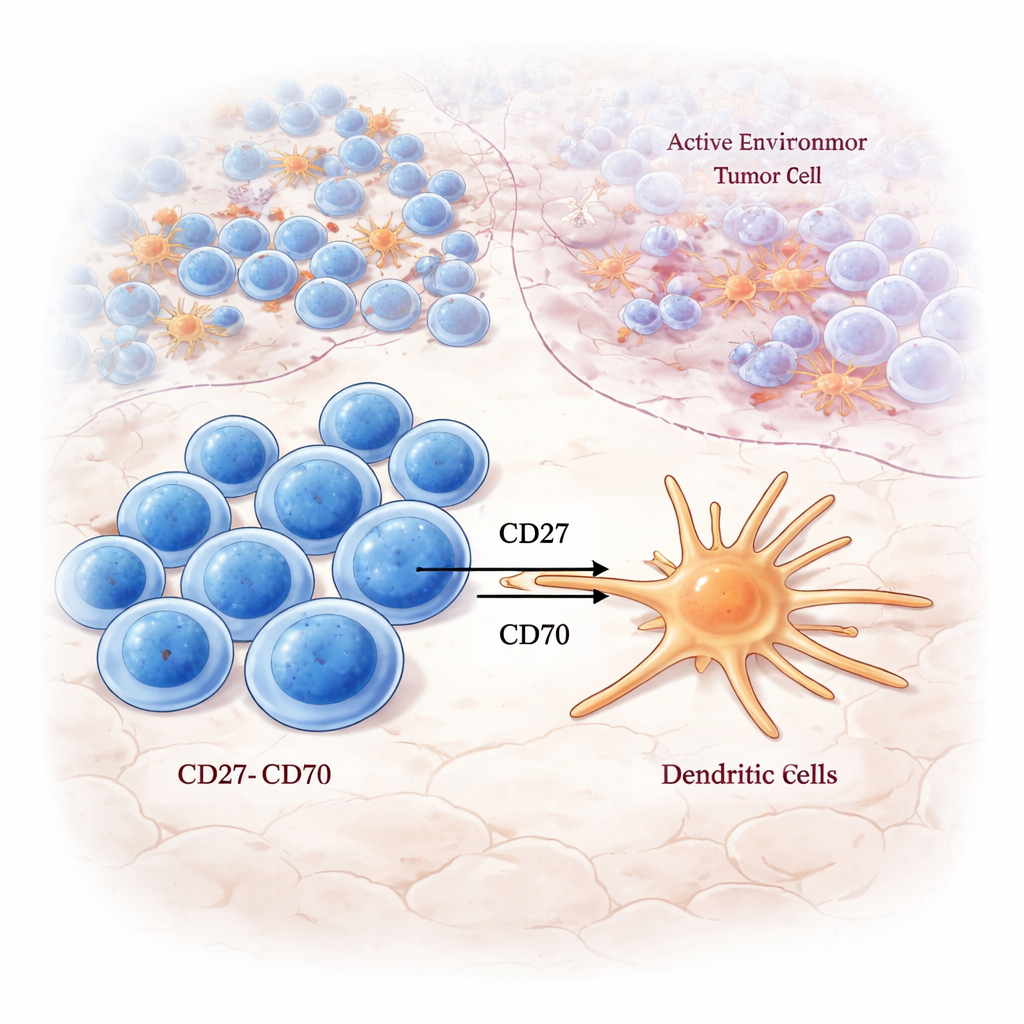
Où les cellules T naïves apprennent à combattre
En zoomant sur la LAR, les auteurs ont observé une forte activité des voies de signalisation centrales à l’activation des cellules T : signalisation du récepteur des cellules T, voies de costimulation et traitement des antigènes. Les cellules T CD8 naïves — qui n’ont pas encore pleinement acquis une spécificité d’attaque — étaient particulièrement liées à ces signaux d’activation dans la LAR, mais pas ailleurs. Par coloration multicolore, ils ont détecté des cellules T CD8 dans la LAR exprimant des marqueurs de renouvellement et de prolifération, ce qui suggère que cette région fait office de zone locale de formation et d’expansion où des cellules nouvellement prêtes à combattre la tumeur sont préparées.
Deux variantes de voisinage immunitaire
Toutes les LAR ne se valent pas. Lorsqu’ils ont regroupé les patients selon la composition cellulaire de leurs LAR, les chercheurs ont mis au jour deux profils. Dans les tumeurs « Groupe A », les LAR ressemblaient fortement à des ganglions lymphatiques classiques, riches en cellules B spécialisées et en cellules dendritiques, et les régions tumorales adjacentes à ces LAR étaient remplies de lymphocytes activés et prêts au combat. Dans le « Groupe B », les LAR étaient moins développées, et le tissu tumoral voisin contenait davantage de cellules T au repos, moins engagées. Une analyse computationnelle avancée des images tissulaires a confirmé que les cellules immunitaires activées se regroupaient physiquement près de ces LAR plus matures, suggérant que l’architecture locale peut orienter l’intensité de l’attaque immunitaire contre la tumeur.
Signaux de checkpoint dans l’espace
L’étude a aussi cartographié l’expression des « interrupteurs » immunitaires connus sous le nom de molécules checkpoint. Des paires stimulatrices comme CD27–CD70 étaient concentrées dans la LAR, en particulier dans les tumeurs du Groupe A, reliant des cellules T CD8 épuisées mais réactives vis-à-vis de la tumeur avec des cellules dendritiques susceptibles de renforcer davantage leur activité. En revanche, de nombreuses paires checkpoint inhibitrices, telles que TIGIT–NECTIN2 et LAG3–LGALS3, étaient enrichies dans la NCR, la zone la plus chargée en cellules cancéreuses. Cela suggère que même lorsque la signalisation du récepteur des cellules T est présente, le paysage checkpoint environnant peut faire pencher l’immunité locale vers l’attaque ou la suppression, selon la région de la tumeur.
Ce que cela signifie pour les patients
Pour un non-spécialiste, le message clé est que l’emplacement des cellules et des signaux immunitaires à l’intérieur d’une tumeur peut être aussi important que leur nombre. Ce travail montre que les cancers gastriques contiennent des voisinages immunitaires distincts, et que des régions robustes, semblables à des ganglions lymphatiques, près de la tumeur sont associées à des cellules T plus actives, mieux positionnées et à des résultats plus favorables. En apprenant à reconnaître et éventuellement à renforcer ces régions agrégées de lymphocytes, les thérapies futures pourraient être mieux adaptées — en choisissant des médicaments, des combinaisons ou même des approches de délivrance ciblée qui exploitent les points d’appui immunitaires internes de la tumeur.
Citation: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Mots-clés: cancer gastrique, microenvironnement tumoral, structures lymphoïdes tertiaires, transcriptomique spatiale, immunothérapie du cancer