Clear Sky Science · fr
Vieillissement divergent des glandes mammaires nullipares et parées révèle des cellules épithéliales hybrides IL33+
Comment la grossesse peut remodeler le risque de cancer du sein au cours de la vie
Pourquoi une grossesse précoce réduit-elle le risque vital d’un cancer du sein chez une femme, alors que le simple fait de vieillir l’augmente ? Cette étude utilise des souris pour scruter « l’écosystème » cellulaire du sein au fil du temps, en comparant des animaux n’ayant jamais eu de grossesse à d’autres qui en ont eu. En suivant l’évolution des cellules individuelles avec l’âge et la reproduction, les chercheurs mettent au jour un type cellulaire rare et changeant de forme qui pourrait aider à expliquer la protection à long terme conférée par la grossesse.
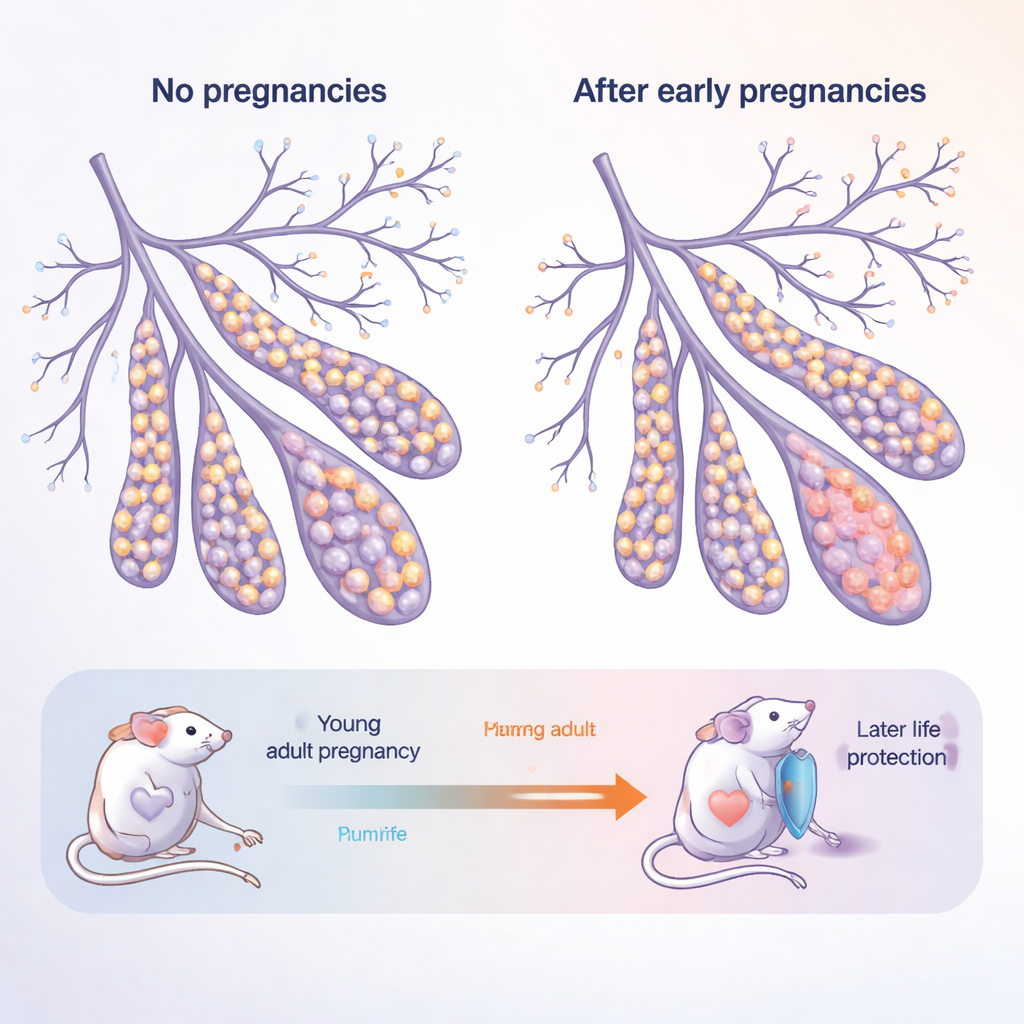
Le sein comme tissu vivant et changeant
La glande mammaire n’est pas un organe statique : elle croît et se remodèle de façon marquée à la puberté, pendant la grossesse, puis à la fin de la lactation. Elle est constituée de deux couches principales de cellules épithéliales qui tapissent les conduits : les cellules « luminales » internes en contact avec le lait et les hormones, et les cellules « basales » externes qui assurent la structure et abritent des cellules de type souche. Les auteurs ont étudié des souris jeunes adultes et des souris plus âgées, « post‑ménopausées », chacune soit nullipare (jamais enceinte) soit parée (ayant connu plusieurs grossesses). Ce dessin expérimental imite une femme donnant naissance dans la vingtaine puis vieillissant jusqu’à la cinquantaine et au‑delà.
Comment le vieillissement et la grossesse tirent le tissu dans des directions opposées
Chez les souris vieillissant sans jamais être enceintes, leurs glandes mammaires ont évolué vers une proportion accrue de cellules basales et une diminution des cellules luminales. Ces glandes plus âgées et jamais enceintes ont aussi produit beaucoup plus d’organoïdes — structures 3D miniatures cultivées à partir de cellules uniques — ce qui indique que leurs cellules étaient anormalement prompts à proliférer. En revanche, les souris ayant connu des grossesses présentaient un équilibre « normalisé » : l’augmentation liée à l’âge des cellules basales était atténuée et leurs cellules formaient moins d’organoïdes. Cela suggère que la grossesse laisse une empreinte durable qui modifie à la fois le choix de destinée des cellules et freine leur potentiel régénératif, potentiellement propice au cancer.
La découverte de cellules hybrides et changeantes
Pour aller plus loin, l’équipe a utilisé le séquençage d’ARN unicellulaire pour lire les gènes actifs dans des milliers de cellules mammaires individuelles. Parmi les populations attendues — cellules luminales, basales, immunitaires et stromales — ils ont trouvé un groupe rare qui ne s’intégrait pas clairement dans l’une ou l’autre couche principale. Ces cellules exprimaient des marqueurs des lignées luminales et basales, d’où le nom de cellules épithéliales « hybrides ». Fait marquant : ces hybrides s’accumulaient avec l’âge chez les souris jamais enceintes mais étaient beaucoup moins fréquents chez des souris d’âge égal ayant été enceintes. Les hybrides exprimaient fortement un gène appelé Il33, codant pour la molécule de signalisation IL‑33, ainsi que des marqueurs liés à des stades développementaux précoces et à une grande plasticité — la capacité à changer d’identité ou de comportement.
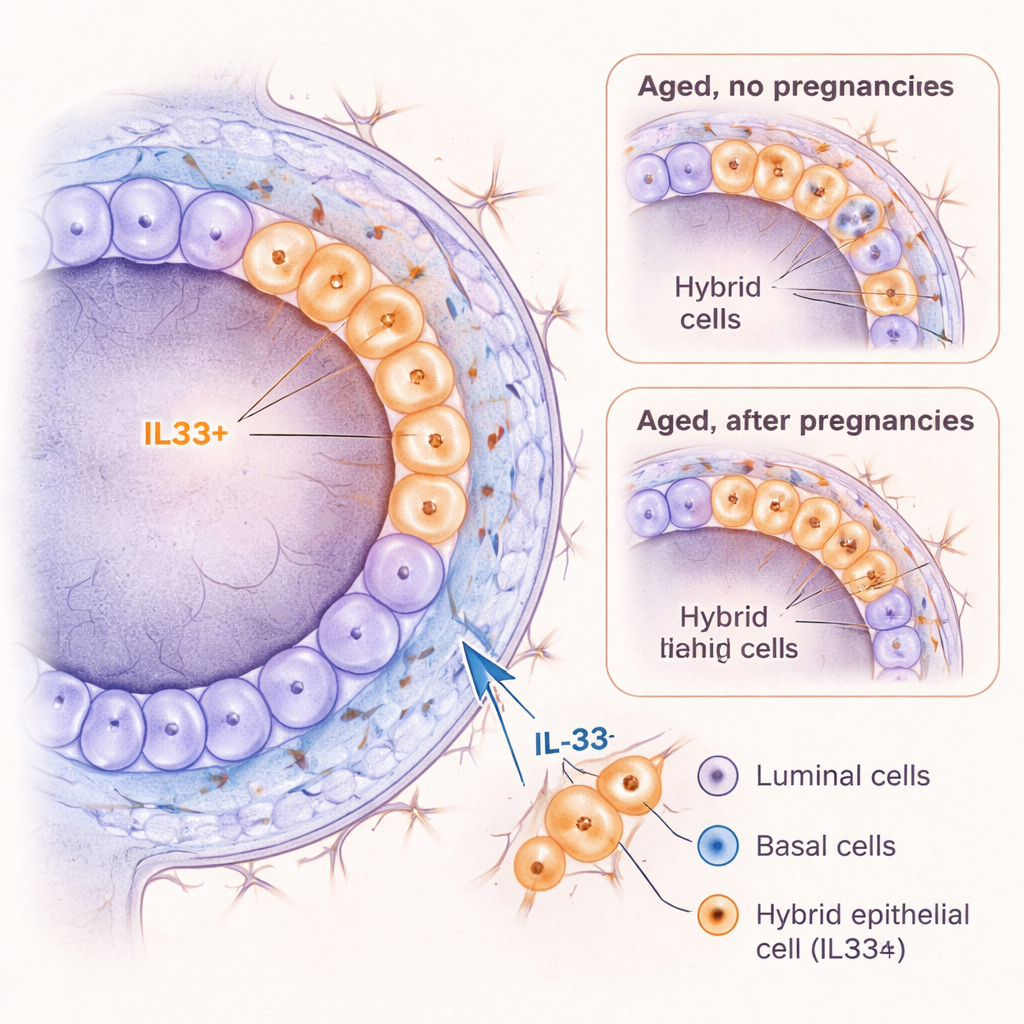
IL‑33 comme moteur d’états cellulaires à risque
Étant donné que IL‑33 a été associée à l’inflammation et au cancer dans d’autres organes, les chercheurs se sont demandé si elle pouvait activement pousser les cellules mammaires vers un état hybride. Lorsqu’ils ont traité des cellules mammaires de jeunes souris avec IL‑33 en culture 3D, les cellules de la couche basale ont formé davantage d’organoïdes, conservé une identité plus primitive et produit plus de cellules marquées par l’indicateur hybride KRT6A. Chez des souris jeunes vivantes, des injections brèves d’IL‑33 ont élargi les canaux, déclenché une poussée de division cellulaire, accompagné d’un pic transitoire de cellules hybrides KRT6A‑positives et d’un déplacement vers plus de cellules de type basale. Fait important, lorsque les cellules portaient une mutation liée au cancer (perte du gène suppresseur de tumeur Trp53), IL‑33 a encore renforcé leur croissance. Ensemble, ces résultats suggèrent qu’IL‑33 favorise un état cellulaire plastique et prolifératif qui pourrait être particulièrement vulnérable à la transformation cancéreuse.
Indices issus de tissus mammaires humains
Pour vérifier si des cellules similaires existent chez l’homme, les auteurs ont réanalysé plusieurs grandes bases de données unicellulaires issues de tissus mammaires humains normaux. Ils ont identifié une petite population de cellules épithéliales humaines qui, comme les hybrides de souris, présentaient à la fois des caractéristiques luminales et basales et exprimaient IL33 et des gènes associés. Les cellules IL33‑positives devenaient plus fréquentes avec l’âge dans plusieurs jeux de données. Dans des cellules mammaires humaines primaires cultivées en laboratoire, le traitement par IL‑33 augmentait la formation d’organoïdes, déplaçait le profil des cellules vers un phénotype plus basaloïde et enrichissait les cellules CD44‑positives — un marqueur souvent associé aux cellules immatures de type souche dans le cancer du sein. Bien que les échantillons humains disponibles n’aient pas permis de tester proprement comment une grossesse précoce modifie cette population, les parallèles avec les observations chez la souris sont frappants.
Ce que cela signifie pour la compréhension de la protection contre le cancer du sein
Pour un lecteur non spécialiste, le message central est que la grossesse semble recâbler la façon dont le tissu mammaire vieillit. Chez la souris, une grossesse précoce empêche l’accumulation de cellules hybrides riches en IL‑33 qui estompent la frontière entre les principales couches cellulaires du sein et se comportent de façon très flexible et pro‑proliférative. IL‑33 elle‑même peut pousser les cellules vers cet état risqué et changeant, en particulier lorsqu’il existe des mutations liées au cancer. En réduisant le nombre ou la persistance de ces cellules hybrides, la grossesse pourrait diminuer les chances qu’un tissu mammaire vieillissant contienne le « mauvais » type de cellule au « mauvais » moment — une cellule prête à basculer vers le cancer. Cette compréhension mécanistique pourrait à terme orienter des stratégies visant à imiter les effets protecteurs d’une grossesse précoce sans nécessiter une grossesse elle‑même.
Citation: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
Mots-clés: vieillissement du sein, grossesse et cancer du sein, cellules souches mammaires, signalisation IL-33, cellules épithéliales hybrides