Clear Sky Science · fr
Élargir la portée des cargaisons des conjugués anticorps–médicament en délivrant des médicaments porteurs d’hydroxy via des phosphoramidates auto-démolissants
Des missiles plus intelligents contre le cancer
Les médicaments anticancéreux peuvent être extrêmement puissants, mais ils agissent souvent comme un bombardement généralisé : ils touchent les tissus sains presque autant que les tumeurs. Les conjugués anticorps–médicament (ADCs) ont été conçus pour résoudre ce problème en attachant un médicament puissant à un anticorps qui cible les cellules cancéreuses, transformant le traitement en un missile guidé. Cet article explique un nouveau « verrou » chimique entre l’anticorps et le médicament qui rend ces missiles à la fois plus précis et plus flexibles, ouvrant la porte à bien plus de types de médicaments anticancéreux que ceux que peuvent transporter les ADCs actuels.
Pourquoi les médicaments ciblés d’aujourd’hui restent limités
Les ADCs sont composés de trois éléments : un anticorps qui reconnaît un marqueur sur les cellules cancéreuses, un médicament toxique (la « cargaison ») et un linker chimique qui les relie. La plupart des ADCs approuvés reposent sur seulement quelques types de cargaisons qui endommagent l’ADN ou bloquent la division cellulaire de façons similaires. Une raison majeure est le linker : il doit retenir fermement le médicament pendant que l’ADC circule dans le sang, puis le libérer proprement une fois à l’intérieur de la cellule tumorale. Les linkers existants fonctionnent bien uniquement avec certains groupes chimiques présents sur les médicaments, en particulier les amines, et peinent souvent avec les nombreux médicaments contenant des groupes alcool (–OH). Cela laisse de côté un grand nombre d’agents anticancéreux prometteurs parce qu’ils ne peuvent pas être délivrés de manière sûre ou efficace par les conceptions d’ADC actuelles.
Emprunter une astuce aux pilules antivirales
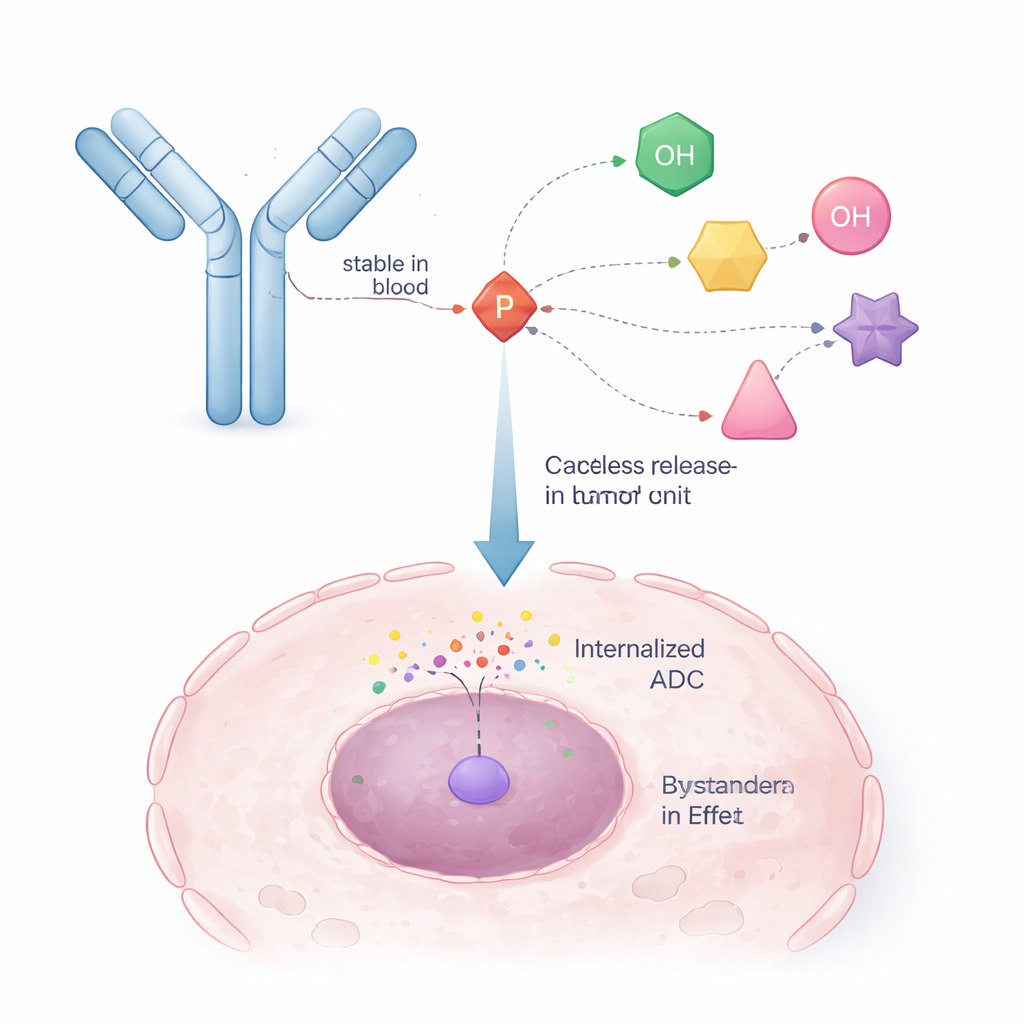
Les chercheurs se sont tournés vers une stratégie déjà éprouvée dans les antiviraux appelée ProTides. Dans ces médicaments, une unité chimique à base de phosphore masque temporairement le groupe phosphate chargé d’un médicament pour lui permettre d’entrer dans les cellules, puis se désassemble à l’intérieur pour libérer la forme active. Les auteurs ont réingénieré ce concept de sorte qu’un bras du noyau phosphore soit utilisé pour se lier à un anticorps, tandis que les autres bras portent le médicament anticancer. Cela crée un linker « auto-démolissant » : une fois qu’un déclencheur interne (par exemple une enzyme dans une cellule tumorale) coupe une petite partie de la structure, l’unité phosphore s’effondre de façon contrôlée et libère la molécule de médicament originale avec son groupe alcool restauré et non modifié.
Construire un verrou chimique polyvalent
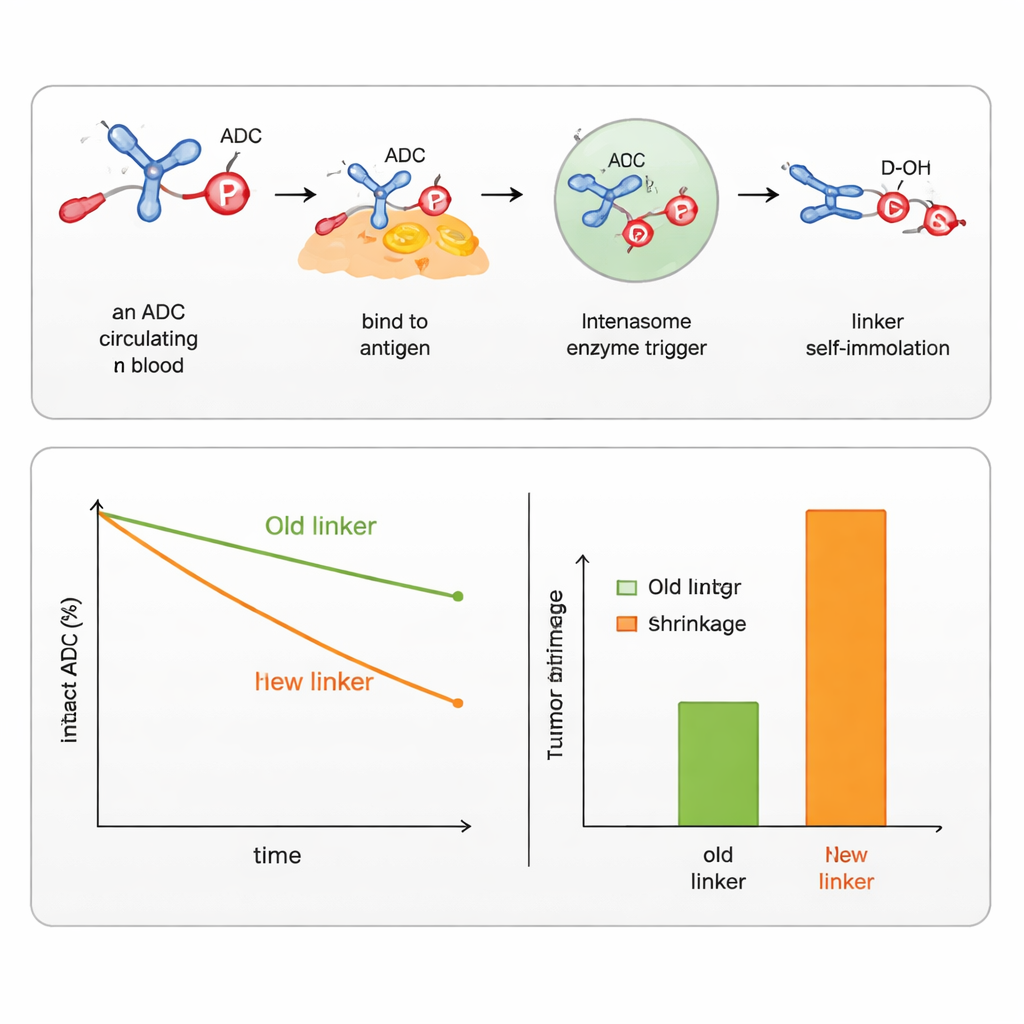
L’équipe a montré qu’en modifiant les groupes autour de l’atome de phosphore, ils pouvaient ajuster la stabilité du linker dans le sang et la vitesse à laquelle il se désassemble à l’intérieur des cellules. Ils ont conçu des versions qui répondent à plusieurs types de déclencheurs courants dans les cellules cancéreuses, y compris les estérases et les protéases (enzymes qui coupent des liaisons spécifiques), ainsi que des enzymes reconnaissant des groupes à base de sucres ou des conditions réductrices dans certains compartiments cellulaires. Avec ces conceptions, ils ont réussi à attacher et à libérer à la fois des alcools aromatiques (comme la chimiothérapeutique SN38) et des alcools aliphatiques (comme le DXd, la cargaison d’un ADC approuvé pour le cancer du sein). Comparés directement aux linkers commerciaux existants pour SN38 et DXd, les nouveaux linkers phosphoramidates ont maintenu les médicaments attachés plus longtemps en sérum, délivré plus de médicament aux tumeurs et produit un rétrécissement tumoral plus marqué chez la souris, tout en ayant moins d’impact sur les cellules saines.
Déverrouiller de nombreuses nouvelles cargaisons anticancéreuses
Pour tester l’universalité du linker, les chercheurs ont assemblé des ADCs transportant dix médicaments différents contenant tous au moins un groupe –OH mais agissant de façons très différentes à l’intérieur des cellules cancéreuses. Parmi eux figuraient des inhibiteurs de la synthèse de l’ADN, du repliement des protéines (HSP90), du métabolisme énergétique (NAMPT et DHODH) et de la traduction protéique, ainsi que des agents bien connus tels que le paclitaxel et la gemcitabine. Malgré la grande diversité de structures, ils ont pu fabriquer des ADCs homogènes avec un chargement élevé en médicament pour chacun. Dans des études cellulaires sur plusieurs types de cancers, la plupart de ces ADCs ont montré une puissance en nanomolaire voire en sous-nanomolaire et une sélectivité nette pour les cellules exprimant la cible de l’anticorps, confirmant que le linker pouvait libérer de manière fiable le médicament actif à l’intérieur des bonnes cellules.
La gemcitabine en vitrine
La gemcitabine est une chimiothérapie largement utilisée, mais sous sa forme conventionnelle elle est éliminée si rapidement de l’organisme que les patients doivent recevoir de fortes doses répétées, ce qui limite la quantité administrable en toute sécurité. En utilisant le linker phosphoramidate, les auteurs ont attaché la gemcitabine à un anticorps ciblant HER2 sur l’un ou l’autre des deux sites alcool et ont montré que les deux versions retrouvaient une activité complète une fois à l’intérieur des cellules cancéreuses. Dans des modèles murins de tumeurs HER2-positives, une seule dose de l’ADC à la gemcitabine — contenant environ mille fois moins de gemcitabine totale que les schémas posologiques habituels en médicament libre — a produit un contrôle tumoral fort et sélectif. Le comportement de l’ADC dans la circulation sanguine correspondait de près à celui de l’anticorps nu, et des doses élevées étaient bien tolérées chez le rat, suggérant une large marge de sécurité.
Ce que cela signifie pour les traitements futurs du cancer
Pour les non-spécialistes, le message principal est que ce travail apporte un nouveau connecteur chimique très adaptable qui permet aux anticorps de transporter un ensemble bien plus large de médicaments anticancéreux qu’auparavant, et de le faire de manière plus sûre. En garantissant que les médicaments restent attachés pendant la circulation et ne sont libérés proprement qu’après que l’ADC ait été internalisé dans une cellule cancéreuse, les linkers phosphoramidates améliorent la quantité de médicament atteignant la tumeur et réduisent les dommages collatéraux aux tissus sains. Tout aussi important, ils permettent de réaffecter comme thérapies ciblées des petites molécules puissantes existantes — aux formes et mécanismes très variés. Cela pourrait considérablement élargir le catalogue d’ADCs disponibles pour les patients et aider à combattre les tumeurs devenues résistantes à l’ensemble restreint de cargaisons d’aujourd’hui.
Citation: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Mots-clés: conjugués anticorps–médicament, administration de médicaments contre le cancer, liants auto-démolissants, chimie des phosphoramidates, chimiothérapie ciblée