Clear Sky Science · fr
Électrolyseur d’hydrogénation du CO2 sans membrane pour la gestion de la précipitation de sels dans la réduction électrochimique acide du CO2
Transformer la pollution climatique en carburant liquide utile
Le dioxyde de carbone (CO2) issu des centrales électriques et des usines est un facteur majeur du changement climatique, mais il constitue aussi une matière première bon marché et abondante. Les scientifiques s’efforcent de convertir le CO2 en produits chimiques utiles en utilisant de l’électricité d’origine renouvelable. Cette étude s’attaque à un obstacle pratique qui a discrètement limité ces technologies : l’accumulation de sels à l’intérieur des réacteurs de type industriel, qui étouffe progressivement les performances. Les chercheurs présentent un nouveau concept de réacteur sans membrane qui fonctionne de façon stable pendant des jours tout en convertissant efficacement le CO2 en acide formique, un liquide utilisable comme matière première chimique, conservateur ou vecteur d’énergie.
Pourquoi les dispositifs actuels s’encrassent
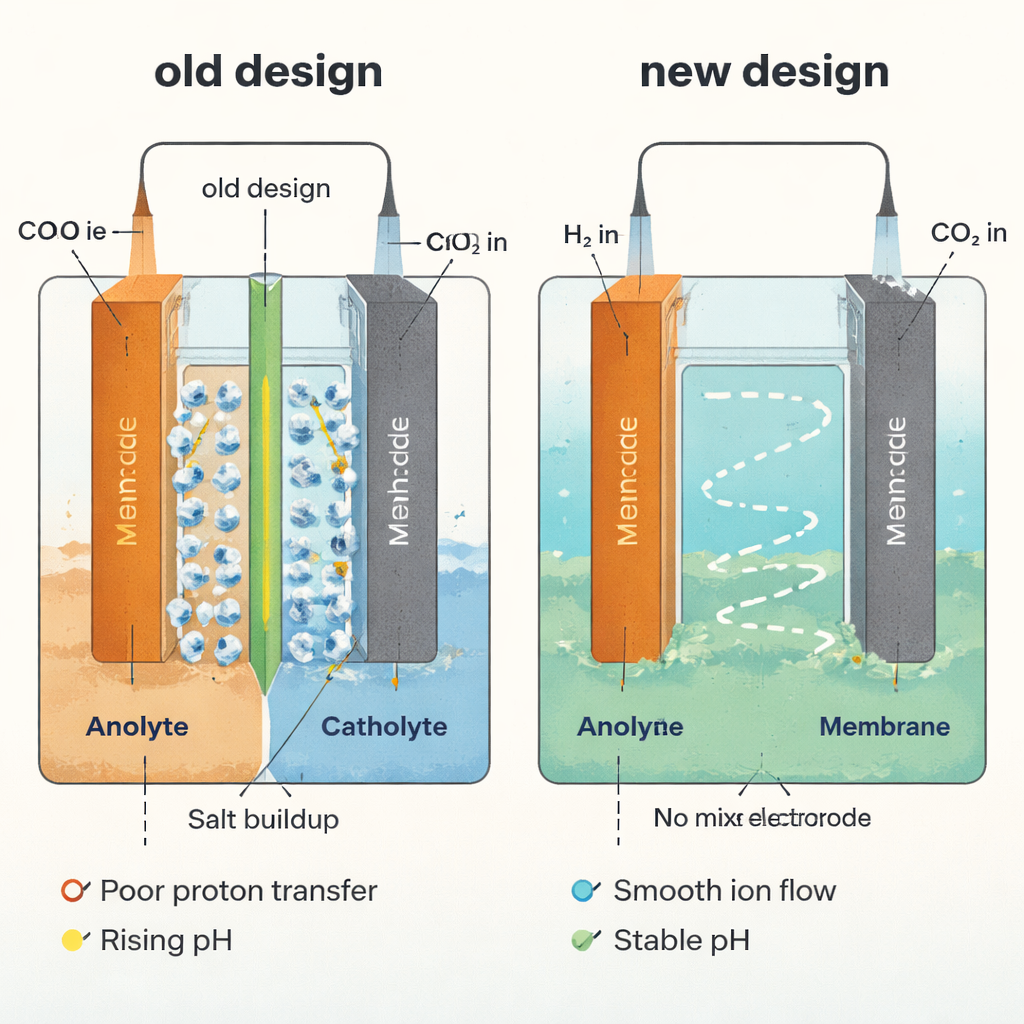
Beaucoup d’appareils de conversion du CO2 ressemblent à des piles à combustible compactes. Le CO2 est alimenté d’un côté (la cathode), où il est transformé en produits, tandis que l’eau est oxydée de l’autre côté (l’anode) pour fournir les charges positives nécessaires (protons). Une fine feuille polymère appelée membrane sépare ces deux côtés, laissant passer certains ions tout en gardant les liquides séparés. Dans des milieux alcalins ou neutres, une grande partie du CO2 réagit avec les hydroxyde pour former des sels de carbonate au lieu de produits utiles, gaspillant le carbone et nécessitant des recyclages énergivores. Les milieux acides peuvent éviter cela, mais le système dépend alors de la capacité de la membrane à fournir rapidement et uniformément des protons. Quand l’apport en protons est insuffisant, l’acidité locale à la cathode augmente, des carbonates et bicarbonates cristallisent, et des sels solides bloquent progressivement les voies gazeuses nécessaires pour que le CO2 atteigne le catalyseur.
Une nouvelle façon de déplacer les protons sans barrière
L’équipe a d’abord quantifié l’efficacité du transport des protons à travers les membranes dans des réacteurs acides typiques, en introduisant une mesure simple : le nombre de protons traversant la membrane par électron circulant dans le circuit. Par la théorie et des simulations informatiques, ils ont montré que les membranes réelles atteignent rarement un transfert protonique idéal. Des films plus épais, une sélectivité protonique moindre et certaines mélanges d’ions ralentissent le mouvement des protons et créent une acidité inégale entre les deux côtés. Les expériences l’ont confirmé : dans une cellule standard à membrane, le catholyte (le liquide à la cathode) est passé d’un milieu fortement acide à quasi neutre en quelques heures, favorisant la formation de carbonates et la précipitation de sels profondément à l’intérieur de l’électrode à diffusion de gaz.
Hydrogénation du CO2 sans membrane
Pour contourner entièrement le goulot d’étranglement de la membrane, les chercheurs l’ont retirée et ont laissé un seul liquide partagé s’écouler devant les deux électrodes. Cela a stabilisé le pH, mais a engendré un nouveau problème : l’acide formique précieux produit à la cathode pouvait être détruit à une anode conventionnelle effectuant la réaction d’évolution de l’oxygène, qui fonctionne à une tension relativement élevée où de nombreuses molécules organiques s’oxydent. La solution a été de remplacer l’évolution de l’oxygène par la réaction d’oxydation de l’hydrogène — en pratique « consumer » l’hydrogène en protons à très basse tension. Dans cet électrolyseur d’hydrogénation du CO2 sans membrane, l’hydrogène est fourni à l’anode, le CO2 à la cathode, et le liquide en écoulement mélange rapidement les protons et les hydroxyde produits de chaque côté, empêchant tout gradient de pH durable et réduisant fortement l’accumulation de sels.
Un catalyseur intelligent et des performances à long terme
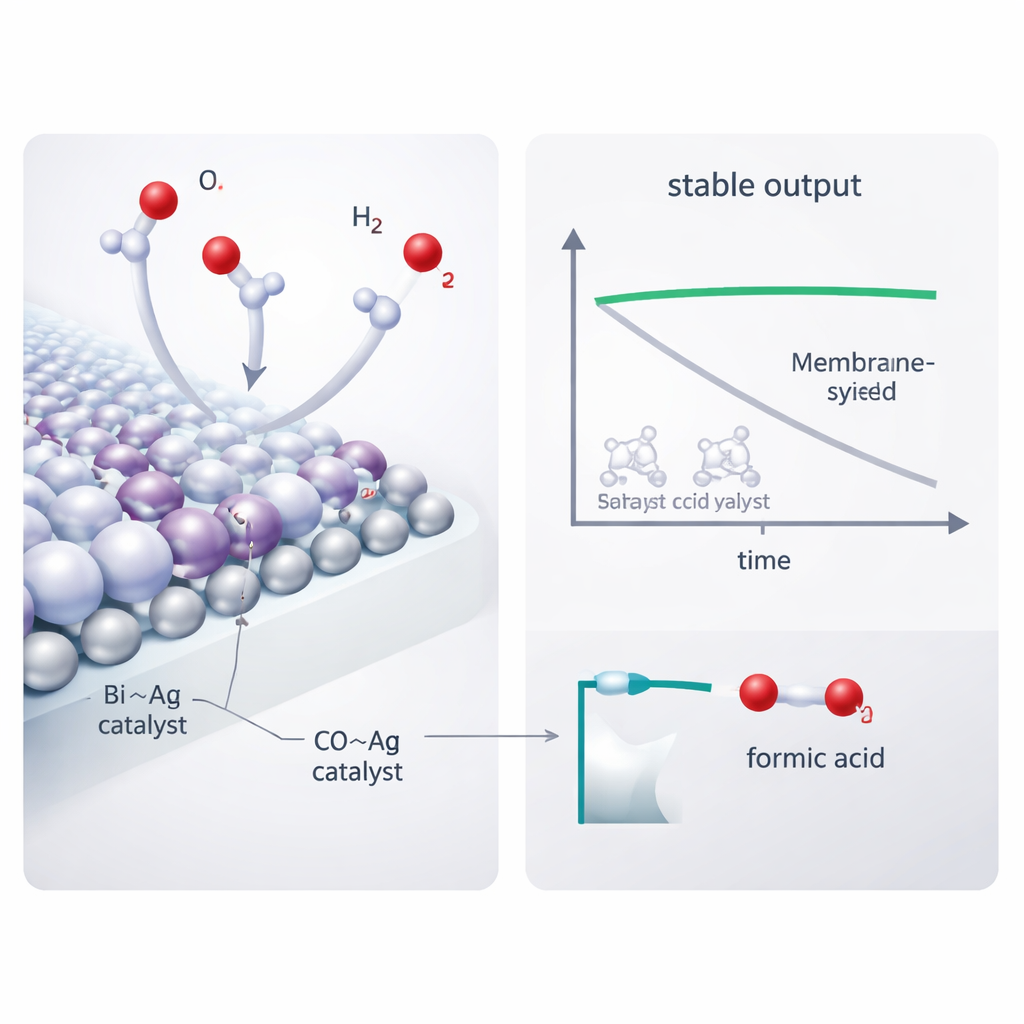
Au cœur de la cathode, les auteurs ont développé un catalyseur bismuth–argent (Bi–Ag) qui combine l’aptitude du bismuth à former du formiate avec l’excellente conductivité électrique de l’argent. La microscopie et la spectroscopie ont révélé des nanoparticules d’argent décorant des nanosheets de bismuth et des interactions électroniques subtiles entre les deux métaux qui améliorent l’adsorption et l’activation du CO2. En solution acide, ce catalyseur a converti le CO2 en acide formique avec plus de 90 % d’efficacité sur une large plage de courant. Placé dans le réacteur sans membrane couplé à l’hydrogène, il a délivré plus de 90 % d’efficacité à 100 milliampères par centimètre carré en n’utilisant que 1,7 volt — sensiblement inférieur aux conceptions concurrentes — et a fonctionné de façon stable pendant 208 heures. Seules des traces de carbonate ont été détectées dans l’électrode après plusieurs jours d’opération, montrant que le problème de précipitation gênant a été largement supprimé.
Du dispositif de laboratoire à l’amélioration pratique du CO2
Au-delà de la démonstration de faisabilité, l’équipe a poussé le concept vers une pertinence pratique. En réduisant la hauteur du canal liquide entre les électrodes, ils ont diminué la résistance électrique et maintenu de hautes performances à des tensions plus faibles. Ils ont atteint une efficacité de conversion du CO2 en un seul passage allant jusqu’à 77 %, ce qui signifie que la majeure partie du CO2 entrant dans la cellule était transformée en produit en une seule fois. Des modèles économiques suggèrent que la suppression de la membrane, la réduction de la consommation d’énergie et l’obtention d’une forte utilisation du carbone peuvent réduire sensiblement le coût de production d’acide formique, même si des économies supplémentaires dépendront d’une électricité moins chère, d’une meilleure séparation du produit hors du liquide et d’un fonctionnement à des courants plus élevés. Dans l’ensemble, ce travail montre une voie pratique pour transformer le CO2 résiduel en un produit chimique liquide utile tout en contournant un problème clé de durabilité qui a affecté les conceptions de réacteurs antérieures.
Citation: Da, Y., Fan, L., Wang, W. et al. Membrane-free CO2 hydrogenation electrolyzer for salt precipitation management in acidic electrochemical CO2 reduction. Nat Commun 17, 1872 (2026). https://doi.org/10.1038/s41467-026-68600-3
Mots-clés: électro-réduction du CO2, acide formique, électrolyseur sans membrane, oxydation de l’hydrogène, utilisation du carbone