Clear Sky Science · fr
Cyanation C–H régiodivergente et énantiosélective des amines secondaires contrôlée par le ligand
Pourquoi modifier de petites liaisons compte pour de grands médicaments
De nombreux médicaments à succès contiennent de petites unités azotées appelées amines. Des changements subtils dans la façon dont les atomes sont reliés autour de ces amines peuvent transformer un médicament peu actif en un traitement puissant et précis — ou en quelque chose d’inactif voire nocif. Cet article décrit une nouvelle méthode pour modifier ces blocs d’amines à volonté, permettant aux chimistes de choisir exactement où sur la molécule réagir et quelle forme image‑miroir produire, deux paramètres cruciaux pour concevoir des médicaments plus sûrs et plus efficaces.
Choisir un emplacement sur une molécule encombrée
Les amines dans les médicaments présentent souvent plusieurs liaisons carbone‑hydrogène (C–H) très similaires qui se comportent normalement presque de la même manière. Les chimistes souhaiteraient remplacer un seul de ces hydrogènes par un groupe utile, comme un groupe « cyano » (–CN), sans perturber le reste de la molécule. C’est difficile car les réactions classiques tendent à viser le site le plus réactif dicté par la structure, pas le choix du chimiste. Ici, les auteurs travaillent sur des amines secondaires simples et flexibles portant deux chaînes carbonées différentes sur l’azote. Ils montrent qu’à partir de la même amine, ils peuvent diriger la réaction vers l’un de deux positions voisines — soit à côté d’un petit groupe N‑méthyl (le site dit α′) soit un carbone plus loin sur l’autre chaîne (le site β) — simplement en changeant le ligand entourant un catalyseur au cuivre.
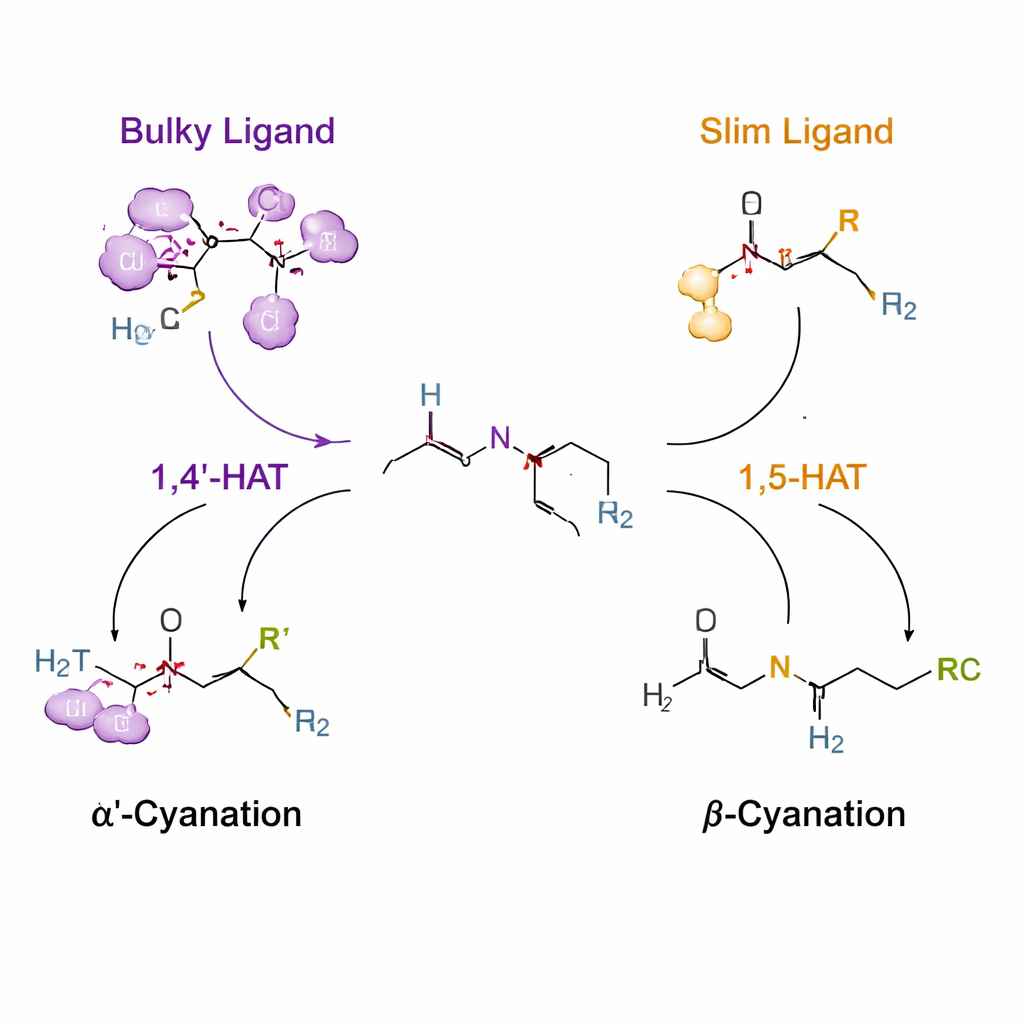
Utiliser des « sauts » d’hydrogène contrôlés pour guider la réactivité
Le point clé repose sur un processus appelé transfert d’atome d’hydrogène (HAT), où un radical centré sur l’azote, de courte durée de vie, arrache un hydrogène d’un carbone voisin. Habituellement, de tels radicaux préfèrent une certaine distance, favorisant une « portée » à six membres connue sous le nom de 1,5‑HAT. Les auteurs fixent une poignée temporaire d’urée et de chlore sur l’amine de sorte que, sous catalyse cuivrée, ce radical azoté se forme et puisse capter un hydrogène soit de la position α′ soit de la position β. En concevant des ligands — des molécules organiques qui enrobent le cuivre — ils reconfigurent l’environnement du radical. Un ligand très encombrant (appelé L14) pousse le système vers une étape inhabituelle de type 1,4′‑HAT qui cible le groupe N‑méthyl, donnant une cyanation α′ sélective. Des ligands plus fins (comme L8) laissent passer la voie conventionnelle 1,5‑HAT, orientant la réaction vers la position β à la place.
Du contrôle de la position au contrôle de la « main »
Au‑delà du choix du site de réaction, l’équipe souhaite aussi contrôler la chiralité, essentielle car de nombreux médicaments existent sous formes gauches et droites qui se comportent différemment dans l’organisme. Pour y parvenir, ils introduisent des ligands chiraux — des molécules qui ont elles‑mêmes une forme « manuelle » — dans le complexe de cuivre. Deux de ces ligands, L24 et L41, donnent une forte préférence pour une image‑miroir lorsque la réaction installe un groupe cyano en position β, incluant à la fois des sites benzyliques (à côté d’anneaux aromatiques) et allyliques (à côté de doubles liaisons C=C). Sur une large variété d’amines de départ, la méthode fournit des produits β‑cyanés avec une excellente sélectivité de site et d’énantiosélectivité, et fonctionne à l’échelle gramme, montrant que le procédé est pratique et robuste pour la synthèse.
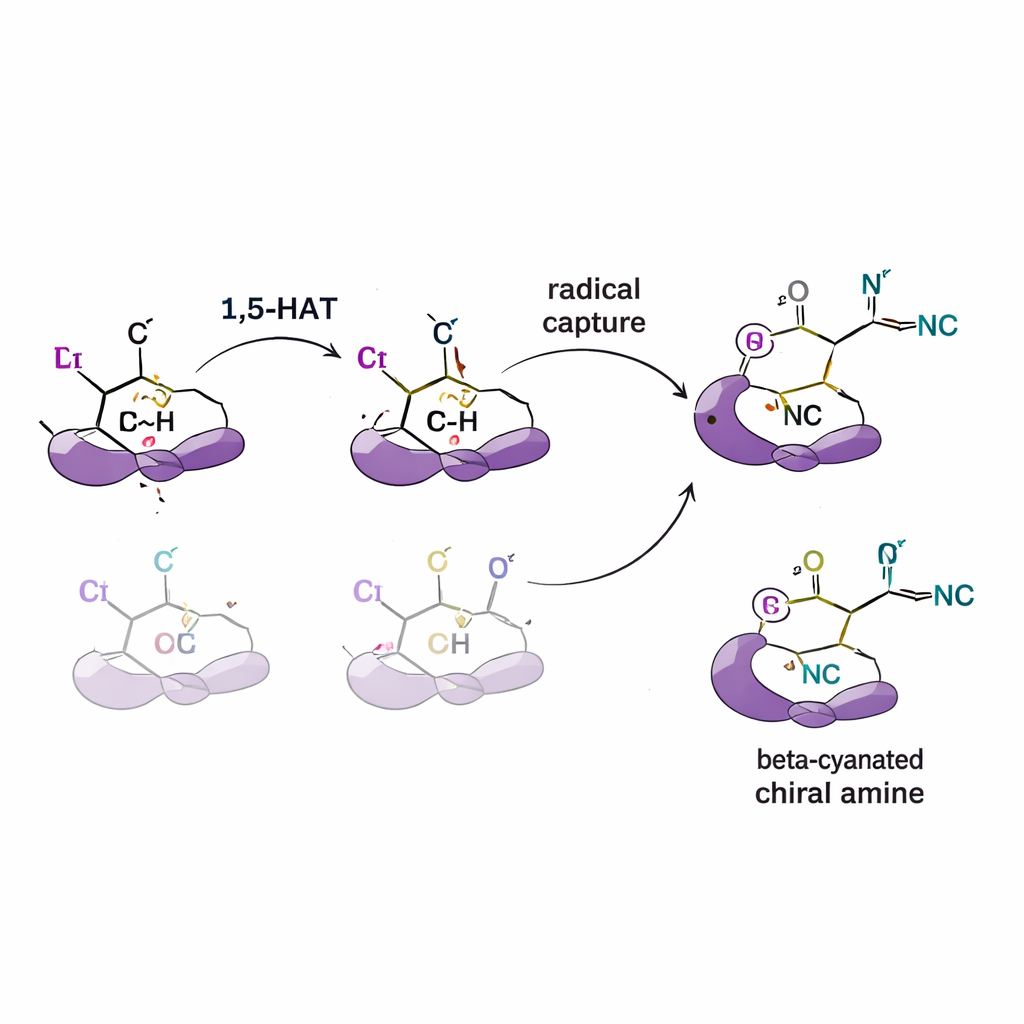
Tester le mécanisme derrière la sélectivité
Pour comprendre l’origine de ce contrôle, les auteurs réalisent une série d’expériences mécanistiques. En ajoutant des « pièges » à radicaux, ils confirment que des intermédiaires radicaux réactifs sont bien impliqués. En utilisant des substrats où certains hydrogènes sont remplacés par du deutérium (une forme plus lourde de l’hydrogène), ils détectent des effets d’isotope cinétique qui indiquent que l’étape de transfert d’hydrogène est l’étape lente et déterminante de la sélectivité. Des expériences de marquage montrent aussi que l’hydrogène se déplace en une seule étape irréversible, plutôt que d’aller et venir entre les positions. Des simulations complémentaires (théorie de la fonctionnelle de la densité) soutiennent ces observations, indiquant que la forme et l’encombrement du ligand modifient l’énergie des voies concurrentes de transfert d’hydrogène et la façon dont le radical se combine ensuite avec le cuivre et le cyanure pour donner une image‑miroir favorisée.
Ce que cela signifie pour la conception de médicaments
Dans l’ensemble, ce travail introduit une stratégie flexible pour ré‑ingénierie des groupes d’amines courants en deux sites étroitement liés, à la demande, avec un contrôle fin de la chiralité. En ne changeant que le ligand d’un catalyseur au cuivre, les chimistes peuvent choisir de placer un groupe cyano sur une petite unité N‑méthyl ou sur le carbone voisin d’une autre chaîne latérale, et cela sur de nombreuses molécules complexes de type médicament. Comme les groupes cyano sont des étapes précieuses vers de nombreuses autres fonctions, cette approche « choisir‑le‑site » et « choisir‑la‑main » devrait faciliter l’exploration et l’optimisation de nouveaux médicaments construits à partir des mêmes squelettes d’amine de base.
Citation: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Mots-clés: fonctionnalisation des amines, transfert d'atome d'hydrogène, catalyse au cuivre, cyanation énantiosélective, chimie médicinale