Clear Sky Science · fr
Localisations génomiques doubles et fonctions de régulation génique de MBD-2 avec et sans NuRD chez Caenorhabditis elegans qui est dépourvu de méthylation de l’ADN
Comment de minuscules vers réécrivent les règles du contrôle génétique
Nos cellules utilisent des marques chimiques sur l’ADN et les protéines pour se rappeler quels gènes doivent être activés ou réprimés. L’une des marques les plus connues, la méthylation de l’ADN, fait défaut chez certains animaux — et pourtant ils se développent et se reproduisent normalement. Cet article examine comment un petit ver, Caenorhabditis elegans, gère la régulation des gènes sans méthylation de l’ADN, révélant un système de secours étonnamment flexible qui pourrait changer notre façon de penser l’épi génétique.
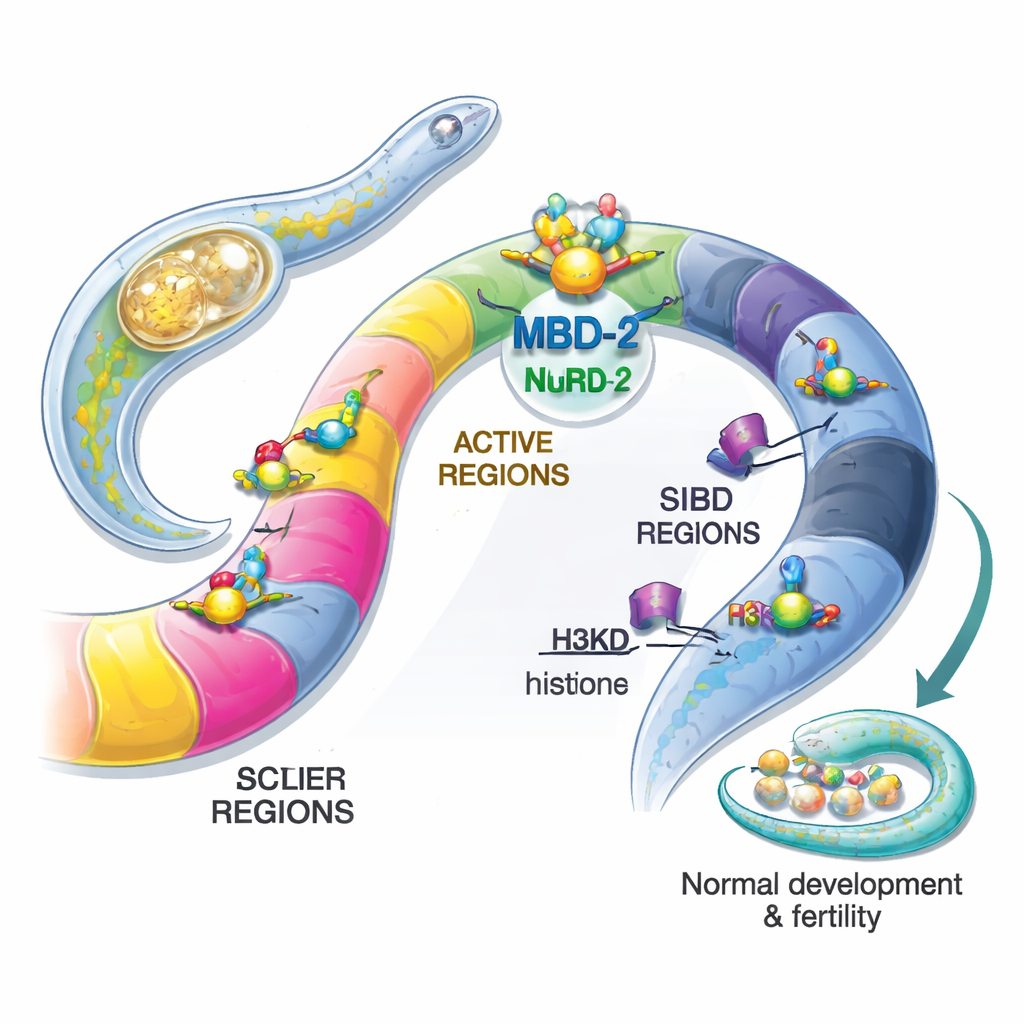
Une marque d’ADN manquante soulève une grande question
Chez les mammifères, une marque chimique appelée 5‑méthylcytosine (5mC) aide à silencer des gènes pendant le développement, l’inactivation du chromosome X et la défense contre les éléments mobiles. Des protéines nommées MBD2 et MBD3 lisent ces marques et recrutent une grande machinerie protéique, le complexe NuRD, qui peut remodeler et inactiver des régions de chromatine. Étonnamment, de nombreux invertébrés, dont C. elegans et la mouche du vinaigre, ont perdu la 5mC et les enzymes qui l’écrivent — mais ont conservé une protéine de type MBD2/3. Cela pose un casse‑tête : pourquoi conserver un “lecteur de méthylation de l’ADN” dans un génome qui n’utilise plus cette marque, et que fait‑il à la place ?
Une protéine échafaudage indispensable aux vers
Les auteurs se sont concentrés sur la version de la protéine chez le ver, appelée MBD‑2. Contrairement à ses homologues mammifères, MBD‑2 du ver a perdu le domaine canonique de liaison à la méthylation qui reconnaît la 5mC, mais conserve des régions flexibles et en hélice qui peuvent se fixer à d’autres protéines. En marquant MBD‑2 par fluorescence, l’équipe a montré qu’elle siège dans les noyaux de presque toutes les cellules tout au long de la vie du ver, ce qui concorde avec un rôle large dans la régulation des gènes. Par génie génétique, ils ont ensuite créé des vers dépourvus de MBD‑2, ou ne contenant que la protéine sans sa région en hélice qui médie le contact avec NuRD. Les deux mutations ont provoqué de graves problèmes : individus de petite taille, mobilité réduite, malformations des organes reproducteurs et forte stérilité. Cela démontre que MBD‑2 est essentiel au développement normal et à la fertilité, même en l’absence de méthylation de l’ADN.
Reconstruire la machine NuRD dans un monde sans méthylation
Pour savoir si MBD‑2 du ver fonctionne toujours avec NuRD, les auteurs ont purifié MBD‑2 marqué à partir d’extraits de ver et identifié ses partenaires par spectrométrie de masse. La plupart des composants connus du NuRD étaient présents, confirmant que MBD‑2 sert d’échafaudage central dans ce complexe, comme le font MBD2/3 chez les mammifères. Lorsque la région en hélice était supprimée, beaucoup de ces interactions disparaissaient, surtout celles avec des protéines remodelant les nucléosomes. Parallèlement, un séquençage à grande échelle de l’ARN a révélé que plus d’un quart de tous les gènes du ver changeaient d’activité chez les mutants MBD‑2, avec beaucoup plus de gènes s’activant que s’éteignant. Ce schéma indique que MBD‑2, souvent avec NuRD, agit généralement comme un répresseur pour maintenir silencieux des gènes inappropriés, tout en aidant également à maintenir l’activité correcte d’un sous‑ensemble de gènes fortement exprimés.
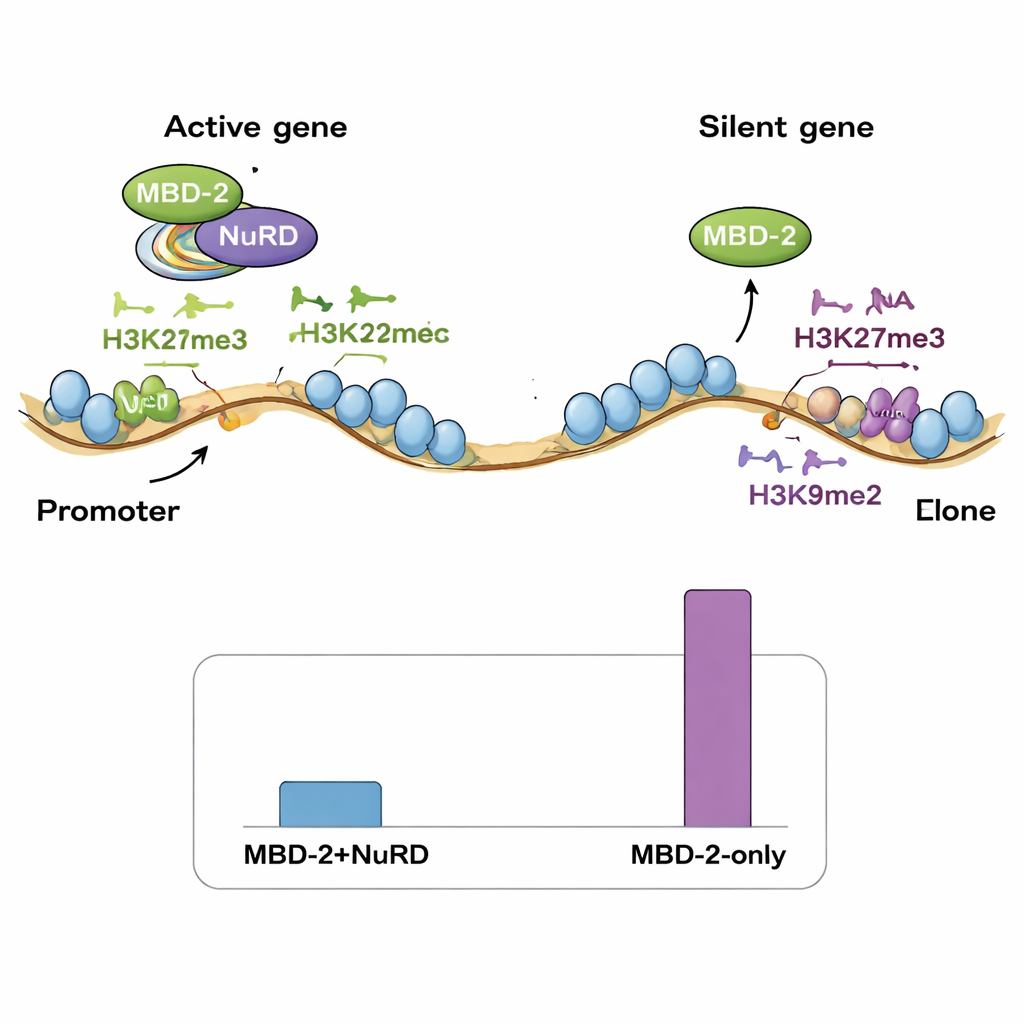
Deux modes de liaison sur le génome
Puis, l’équipe a cartographié où MBD‑2 se situe le long du génome par ChIP‑seq, et a comparé ces emplacements avec des cartes existantes des composants du NuRD et de diverses marques d’histones. De manière surprenante, seule une petite fraction des sites de MBD‑2 chevauchait étroitement les protéines NuRD et les marques de chromatine ouverte et active. La grande majorité des sites de MBD‑2 se trouvaient ailleurs, sur les “bras” chromosomiques riches en marques d’histones répressives telles que H3K27me3 et H3K9me2/3. En d’autres termes, MBD‑2 présente un double comportement : sur une minorité de sites, il voyage avec NuRD pour affiner les gènes actifs, mais sur beaucoup d’autres sites il se lie de manière indépendante dans des régions déjà silencieuses. Le schéma de sa liaison au sein des gènes importe aussi — lorsque MBD‑2 s’accumule près des sites de démarrage des gènes, la perte de la protéine tend à activer ces gènes, tandis que sa liaison plus profonde dans les corps géniques est souvent associée à une réduction d’expression lorsque MBD‑2 est supprimé.
Un secours évolutif pour l’absence de méthylation de l’ADN
Les auteurs proposent que, chez les espèces ayant perdu la méthylation de l’ADN, les marques d’histones répressives — en particulier H3K27me3 — aient pu s’étendre pour occuper un créneau régulatoire similaire. MBD‑2 du ver semble avoir été réaffecté : au lieu de lire la 5mC sur l’ADN, il s’associe désormais à des régions de la chromatine marquées par des modifications spécifiques des histones, tout en ancrant toujours le complexe NuRD via ses domaines d’interaction protéique conservés. Ce travail montre qu’un outillage ancien d’extinction génique peut être reconfiguré au cours de l’évolution : la marque chimique sur l’ADN peut disparaître, mais la machinerie protéique associée survit en se tournant vers des signaux alternatifs. Pour les non‑spécialistes, le message clé est que la régulation des gènes est remarquablement adaptable — les cellules peuvent perdre une marque épigénétique majeure et pourtant conserver un contrôle complexe de milliers de gènes en s’appuyant davantage sur d’autres marques de chromatine et sur les rôles d’échafaudage polyvalents de protéines comme MBD‑2.
Citation: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Mots-clés: épigénétique, chromatine, régulation des gènes, C. elegans, modification des histones