Clear Sky Science · fr
Une enzyme mono‑nucléaire non‑héminique hautement dynamique pour la biosynthèse en deux étapes des isonitriles
Comment les bactéries fabriquent des outils chimiques exotiques
Les isonitriles sont de petits groupes chimiques puissants qui fonctionnent comme des couteaux suisses : ils peuvent capter des métaux, réagir de multiples façons et servent souvent de « ogive » pour des antibiotiques et des toxines naturels très actifs. Certaines bactéries pathogènes, dont l’agent de la tuberculose Mycobacterium tuberculosis, greffent des isonitriles sur des molécules grasses pour mieux voler les métaux à leur hôte. Cet article examine comment l’une de leurs enzymes, appelée Rv0097, réalise cette chimie particulièrement exigeante en deux étapes soigneusement chorégraphiées.
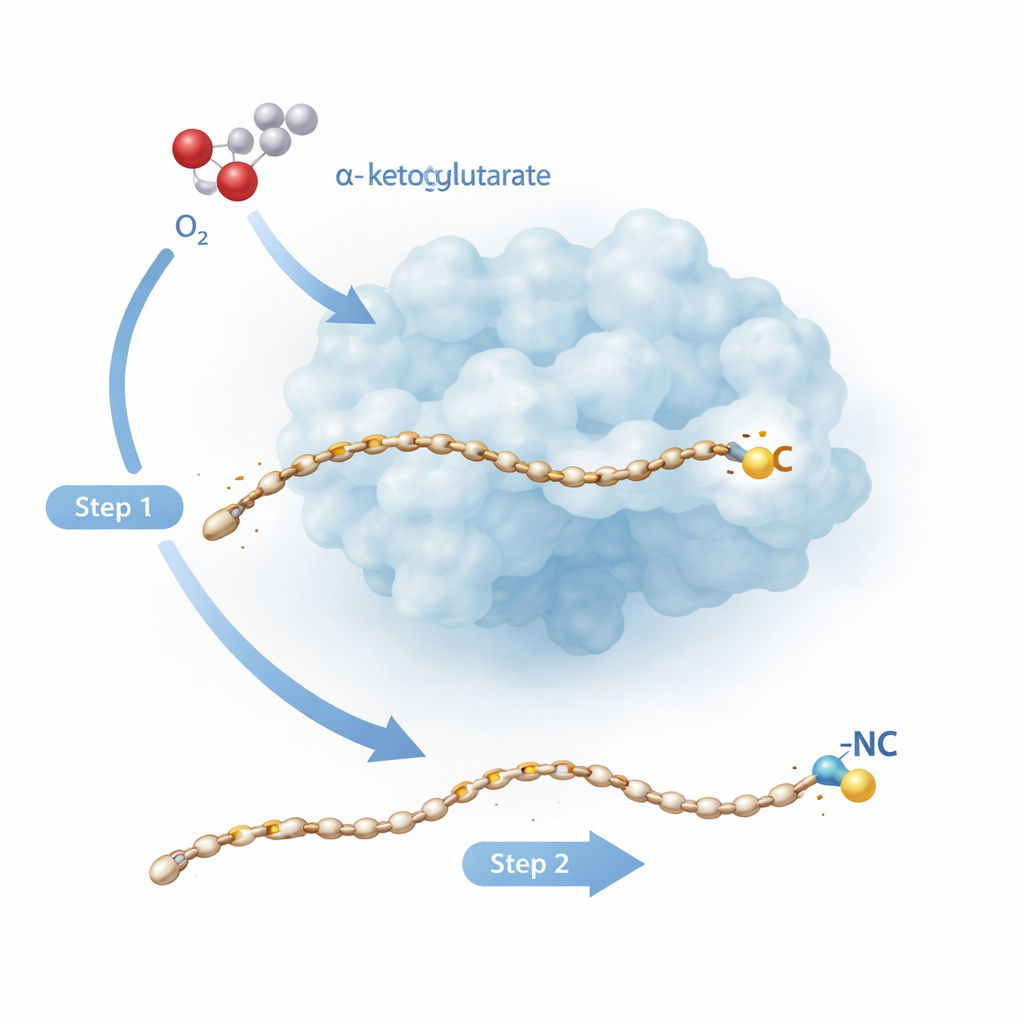
Une transformation moléculaire en deux temps
Rv0097 appartient à une grande famille d’enzymes dépendantes du fer qui effectuent en général des tâches plus simples, comme ajouter de l’oxygène à un seul site d’une molécule. Ici, la mission est plus ardue : à partir d’un bloc de construction « glycyl–acide gras », l’enzyme doit créer un tout nouveau groupe isonitrile, dont les deux atomes clés — le carbone et l’azote — proviennent du même fragment glycinate. Des travaux antérieurs sur une enzyme apparentée, ScoE, ont suggéré que cela ne peut pas se faire en une seule étape. Deux « demi‑cycles » réactionnels distincts sont nécessaires, chacun alimenté par une espèce fer–oxygène formée lorsque l’enzyme clive une molécule auxiliaire, l’α‑cétoglutarate, et la combine avec l’oxygène de l’air. La nouvelle étude se penche sur l’enzyme tuberculeuse Rv0097 pour observer, à résolution atomique, comment une enzyme peut enchainer ces deux étapes radicalaires sur le même substrat sans perdre le contrôle.
Figurer l’enzyme en pleine action
À l’aide de la cristallographie aux rayons X, les chercheurs ont capturé seize clichés haute résolution de Rv0097 dans différents états : vide, lié à son substrat gras (une molécule à dix carbones appelée CADA), lié à l’α‑cétoglutarate auxiliaire, et dans des combinaisons mimant des intermédiaires réactionnels fugaces. Ces structures montrent que Rv0097 a une personnalité double. Au repos, son site actif est pour l’essentiel fermé, avec un acide aminé clé (la phénylalanine 102) basculant entre deux orientations qui maintiennent la poche pour la longue queue grasse sèche et prête à des interactions hydrophobes. Quand CADA se lie, ce résidu se verrouille dans une orientation unique et la « tête » polaire du substrat est ancrée par des chaînes latérales chargées tandis que sa queue huileuse s’insère dans un tunnel bien ajusté. La mutation de cette paire de résidus régulatrice (F102 et une glycine voisine, G204) obstrue soit la poche soit laisse entrer trop d’eau, réduisant fortement l’activité et modifiant les longueurs de chaîne préférées de l’enzyme.
Des capots mobiles et des boucles dynamiques
Au‑delà de la poche du substrat, Rv0097 se comporte comme une petite machine aux portes mobiles. L’équipe a observé des conformations « ouvertes » et « fermées » dans lesquelles deux régions en forme de capot s’écartent ou se referment au‑dessus du site actif. L’ouverture expose le centre ferreux et crée une voie d’entrée pour l’α‑cétoglutarate et le substrat ; la fermeture protège la chimie de l’eau environnante une fois la réaction lancée. Deux boucles de surface flexibles, appelées boucle His et boucle Arg d’après les résidus histidine et arginine qu’elles portent, jouent le rôle d’une porte supplémentaire. Dans certaines structures, ces boucles basculent vers l’intérieur pour que l’arginine saisisse l’α‑cétoglutarate ; dans d’autres, elles s’écartent, apparemment en créant un canal latéral par lequel les fragments auxiliaires usés (succinate et dioxyde de carbone) peuvent sortir et un nouvel α‑cétoglutarate peut entrer pour la seconde étape — tandis que l’intermédiaire dérivé du substrat reste maintenu en place.
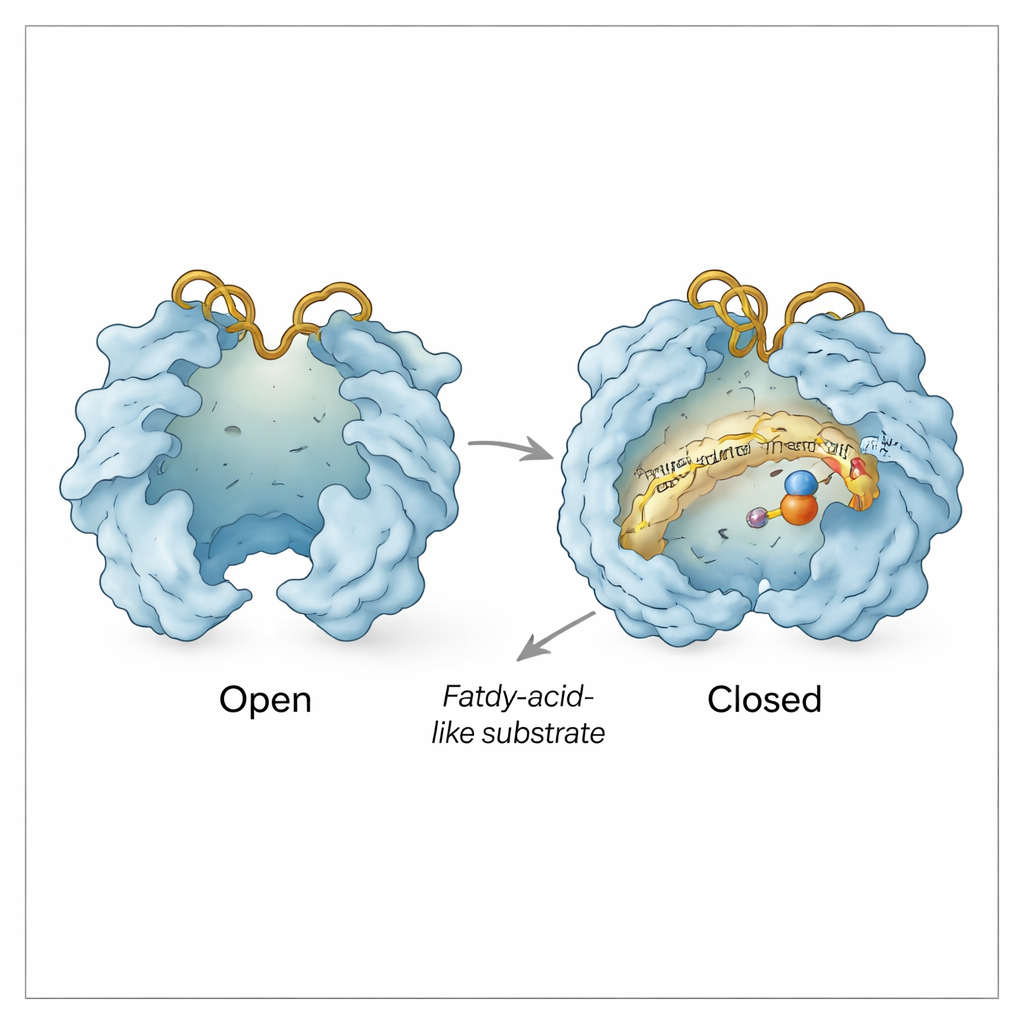
Protéger un intermédiaire fragile
Des essais biochimiques étayent ce tableau structural. La première moitié de la réaction convertit le CADA en un intermédiaire imine hautement réactif qui se décomposerait rapidement s’il dérivait en solution. En piégeant chimiquement son produit de dégradation, les auteurs montrent que la majeure partie de cet intermédiaire n’est détectée que lorsque l’enzyme est encore présente, ce qui implique qu’il reste lié et protégé à l’intérieur de Rv0097 entre les deux demi‑réactions. Les structures expliquent comment : un repositionnement subtil des boucles His et Arg, combiné à de petits déplacements de résidus voisins, semble sceller l’intermédiaire dans une cavité abritée tout en permettant à de petites molécules comme l’α‑cétoglutarate, le succinate et le dioxyde de carbone d’échanger via des canaux contrôlés.
Pourquoi c’est important pour la tuberculose et au‑delà
Pris ensemble, ces résultats révèlent Rv0097 comme une chaîne de montage monoproétique hautement dynamique qui utilise deux fois de suite la chimie à base de fer sur le même substrat sans jamais libérer un produit dangereux à mi‑parcours. Pour les bactéries de la tuberculose, cette précision sous‑tend la fabrication de molécules décorées d’isonitriles qui les aident à obtenir des métaux essentiels dans l’organisme, et des études génétiques indiquent que cette voie est importante pour leur survie pendant l’infection. Pour les chimistes et les concepteurs de médicaments, le travail offre une feuille de route pour détourner des enzymes apparentées afin de fabriquer de nouveaux composés contenant des isonitriles, et suggère que cibler les capots et verrous mobiles de Rv0097 pourrait être une voie pour développer de nouveaux antibiotiques.
Citation: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Mots-clés: biosynthèse des isonitriles, enzyme non‑héminique à fer, Mycobacterium tuberculosis, dynamique enzymatique, produits naturels chélatant les métaux