Clear Sky Science · fr
Dérégulation de l’homéostasie du fer sensibilise le cancer du pancréas à l’électroporation irréversible
Retourner l’électricité et le fer contre un cancer mortel
Le cancer du pancréas est l’un des cancers les plus difficiles à traiter, et même des thérapies locales agressives échouent souvent à empêcher une récidive. Cette étude explore une nouvelle manière d’améliorer et de sécuriser une procédure existante — l’électroporation irréversible, qui élimine les tumeurs au moyen de courtes impulsions électriques puissantes. En perturbant astucieusement la façon dont les cellules cancéreuses gèrent le fer, les chercheurs montrent qu’ils peuvent pousser les cellules survivantes vers une forme de mort destructrice, ce qui pourrait réduire le risque de retour de la tumeur.
Pourquoi les impulsions électriques seules ne suffisent pas
L’électroporation irréversible (IRE) traite les tumeurs en insérant de fins électrodes dans ou autour du cancer et en délivrant des impulsions rapides à haute tension. Ces impulsions créent des trous permanents dans les membranes cellulaires, tuant de nombreuses cellules cancéreuses et déclenchant une réponse immunitaire. Mais le champ électrique n’est pas parfaitement uniforme. Des zones recevant des impulsions légèrement plus faibles peuvent laisser des cellules cancéreuses en vie, et ces survivantes peuvent ensemencer une nouvelle tumeur. En examinant attentivement des cellules de cancer du pancréas et des tumeurs murines exposées à un champ électrique sous-létal, l’équipe a constaté que, au lieu de mourir par un processus dépendant du fer appelé ferroptose, ces cellules déclenchaient un vaste programme de défense antioxydante. Des gènes protecteurs clés, y compris ceux qui neutralisent les dommages liés au fer, étaient surexprimés, permettant aux cellules de résister et de se remettre.
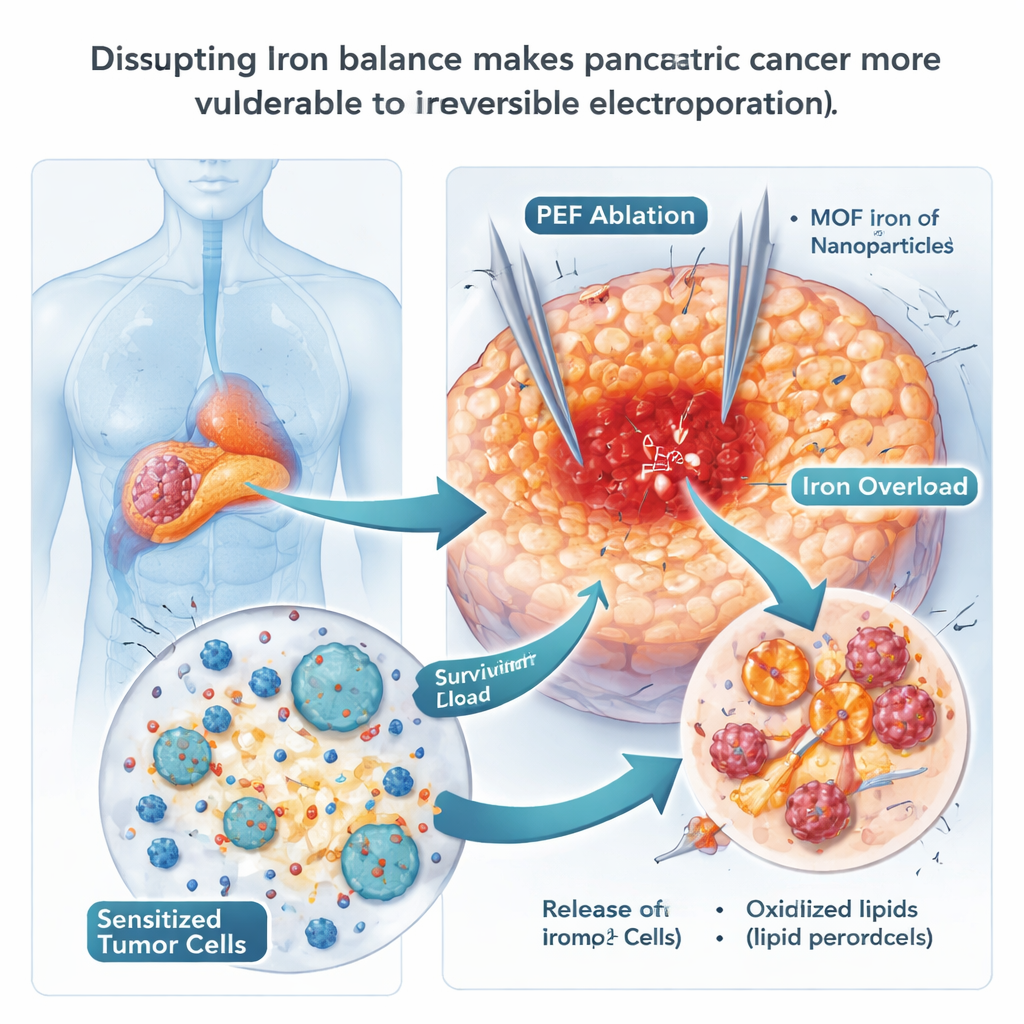
Utiliser des nanoparticules de fer pour pousser les cellules vers la destruction
Comme la ferroptose dépend du fer, les scientifiques ont testé si des nanoparticules riches en fer pouvaient pousser les cellules cancéreuses au-delà du point de non-retour. Ils ont utilisé des particules spécialement conçues à base de structures métal–organiques contenant du fer (MOF-Fe), qui libèrent rapidement du fer à l’intérieur des compartiments acides des cellules. En culture, les cellules de cancer du pancréas ayant internalisé ces particules accumulaient du fer libre et des lipides membranaires oxydés, signes classiques de la ferroptose, et formaient beaucoup moins de colonies. Chez la souris, la combinaison MOF-Fe + IRE retardait la repousse tumorale plus longtemps que chaque traitement pris isolément, et les tumeurs présentaient davantage de signes de dommages oxydatifs. Cependant, cet avantage était temporaire : au bout d’environ trois semaines, les tumeurs recommençaient à rebondir, suggérant que le cancer avait trouvé un moyen de s’adapter à la surcharge en fer.
Cibler le « coffre » à fer de la cellule
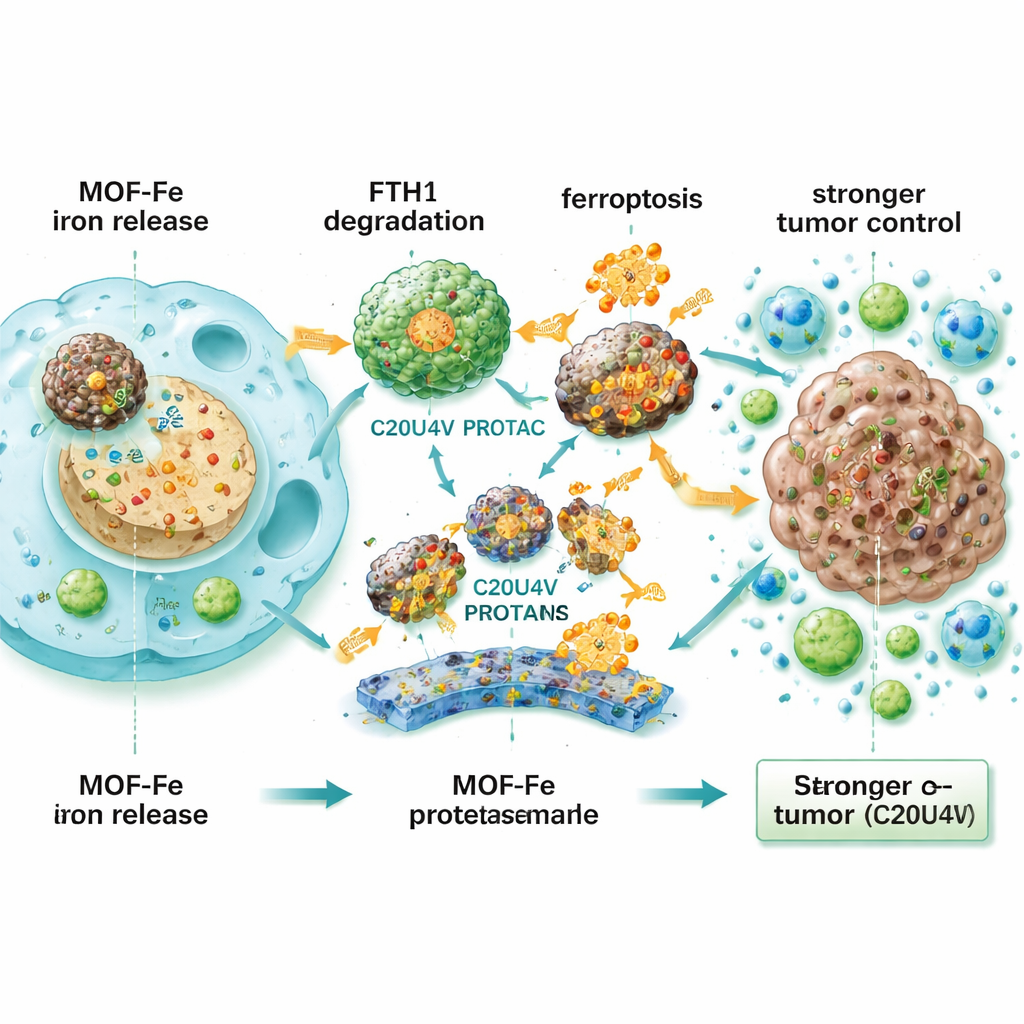
Pour comprendre cette résistance, l’équipe a analysé les protéines dont l’abondance changeait après le traitement par MOF-Fe. Un élément ressortait : la chaîne lourde de la ferritine 1 (FTH1), composante du complexe de stockage du fer de la cellule — l’équivalent moléculaire d’un coffre-fort résistant au feu pour le fer excédentaire. Quand les niveaux de FTH1 étaient augmentés expérimentalement, les cellules cancéreuses devenaient plus résistantes à la ferroptose ; quand FTH1 était réduit, elles devenaient plus vulnérables. Cela désignait FTH1 comme un bouclier central contre la mort induite par le fer. Les chercheurs ont alors conçu une molécule sur mesure, C20U4V, composée d’acide arachidonique (un lipide fortement oxydable) lié à une charpente « PROTAC » qui dirige des protéines spécifiques vers la machinerie d’élimination cellulaire. En présence de MOF-Fe, C20U4V se liait à la ferritine et la recrutait pour qu’elle soit marquée puis détruite, réduisant fortement les niveaux de FTH1 et empêchant la cellule de verrouiller en sécurité le fer.
Des boîtes de culture aux mini-tumeurs et aux souris
Lorsque MOF-Fe et C20U4V étaient combinés, les cellules de cancer pancréatique présentaient un stress oxydatif accru, des lipides membranaires davantage endommagés, des mitochondries plus mal en point et une capacité de régénération très réduite. Cette synergie se retrouvait également dans des organoïdes tridimensionnels dérivés de patients — de minuscules structures tumorales cultivées à partir de tissus humains — où l’association médicamenteuse réduisait nettement la taille et le nombre des organoïdes. Comme C20U4V est lipophile et peu soluble dans l’eau, l’équipe l’a encapsulé dans de petites micelles sensibles aux espèces réactives de l’oxygène (M-C20U4V) qui circulent dans le sang et peuvent libérer le médicament dans les tissus tumoraux stressés et endommagés. Dans des modèles murins portant des tumeurs pancréatiques sous la peau et au sein du pancréas, une combinaison triple d’IRE, MOF-Fe et M-C20U4V a réduit les tumeurs beaucoup plus efficacement et prolongé la survie par rapport à tout traitement simple ou double. Les tumeurs traitées montraient moins de cellules en division, davantage de marqueurs de ferroptose et une infiltration accrue de cellules T et d’autres cellules immunitaires, indiquant que la stratégie tue non seulement les cellules cancéreuses directement mais aide aussi le système immunitaire à reconnaître et attaquer la tumeur.
Ce que cela pourrait signifier pour les patients
Pour le non-spécialiste, l’idée clé est simple : les tumeurs pancréatiques échappent souvent après l’ablation par impulsions électriques parce que certaines cellules cancéreuses survivent et s’adaptent rapidement. Ce travail montre que charger ces cellules en fer tout en neutralisant leur « coffre-fort » à fer peut les contraindre à un état d’autodestruction auquel elles ont du mal à résister. Bien que cette approche soit encore expérimentale et doive faire l’objet d’essais approfondis pour en vérifier la sécurité et la faisabilité chez l’homme, elle suggère que moduler finement la gestion d’un élément aussi fondamental que le fer dans les tumeurs pourrait transformer un traitement local imparfait en un coup plus décisif contre l’un des cancers les plus meurtriers.
Citation: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Mots-clés: cancer du pancréas, électroporation irréversible, ferroptose, nanoparticules de fer, thérapie PROTAC