Clear Sky Science · fr
Identification de Chlamydia pneumoniae et activation de l’inflammasome NLRP3 dans la rétine de la maladie d’Alzheimer
Pourquoi des germes dans l’œil importent pour la mémoire
La maladie d’Alzheimer est généralement vue comme un problème de plaques et d’amas anormaux dans le cerveau. Cette étude suggère qu’une bactérie courante responsable de pneumonies, Chlamydia pneumoniae, pourrait se loger discrètement dans le tissu photosensible à l’arrière de l’œil — la rétine — et contribuer à l’inflammation et aux lésions nerveuses observées dans la maladie d’Alzheimer. Parce que la rétine peut être imagée de manière non invasive, ce travail laisse entrevoir que des examens oculaires pourraient un jour aider à détecter une maladie cérébrale liée à une infection et orienter un traitement précoce.
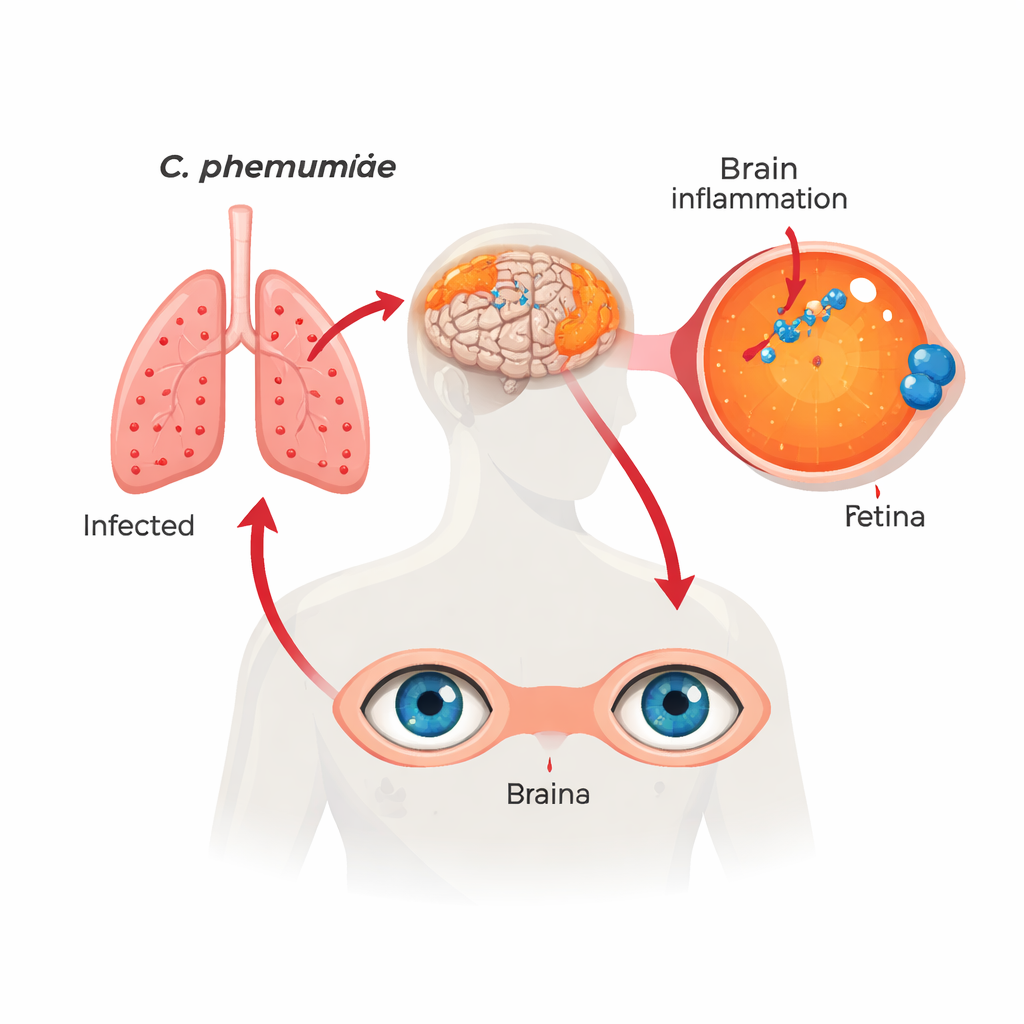
Une infection familière à un endroit inattendu
Les chercheurs ont examiné des rétines et des échantillons cérébraux appariés provenant de plus de 100 personnes décédées qui avaient des capacités cognitives normales, un déficit cognitif léger ou une démence due à Alzheimer. En utilisant plusieurs techniques indépendantes — y compris des anticorps spécifiques, des sondes génétiques, des méthodes de coloration et des tests ADN — ils ont trouvé des signes clairs de Chlamydia pneumoniae à l’intérieur des cellules rétiniennes. Ces « inclusions » bactériennes étaient les plus fréquentes et abondantes chez les personnes atteintes d’Alzheimer, moins présentes chez celles avec un déficit léger, et les moins nombreuses chez les sujets restés cognitivement normaux. La quantité de bactéries dans la rétine reflétait étroitement celle trouvée dans le cerveau, suggérant que l’œil et le cerveau participent à la même infection de longue durée.
Liens entre bactéries, plaques et capacités cognitives
Détecter le germe n’était que la première étape ; la question clé était de savoir si cela avait une incidence sur la maladie. L’équipe a mesuré les marqueurs classiques de l’Alzheimer dans les mêmes tissus. Ils ont observé qu’une charge bactérienne plus élevée dans la rétine allait de pair avec davantage de dépôts d’amyloïde‑bêta — la protéine adhésive qui forme les plaques — ainsi que certaines formes anormales de la protéine tau. Les personnes dont le cerveau présentait plus de signal bactérien avaient aussi plus d’enchevêtrements des fibres nerveuses, une pathologie d’Alzheimer plus sévère et une atrophie cérébrale plus marquée. Sur le plan clinique, celles avec une plus grande charge bactérienne rétinienne obtenaient en moyenne de moins bons scores aux tests de mémoire et de cognition et présentaient une démence plus avancée. Les porteurs de la variante APOE ε4, un facteur de risque génétique majeur pour l’Alzheimer, hébergeaient davantage la bactérie tant dans la rétine que dans le cerveau, ce qui suggère une interaction gène–infection.
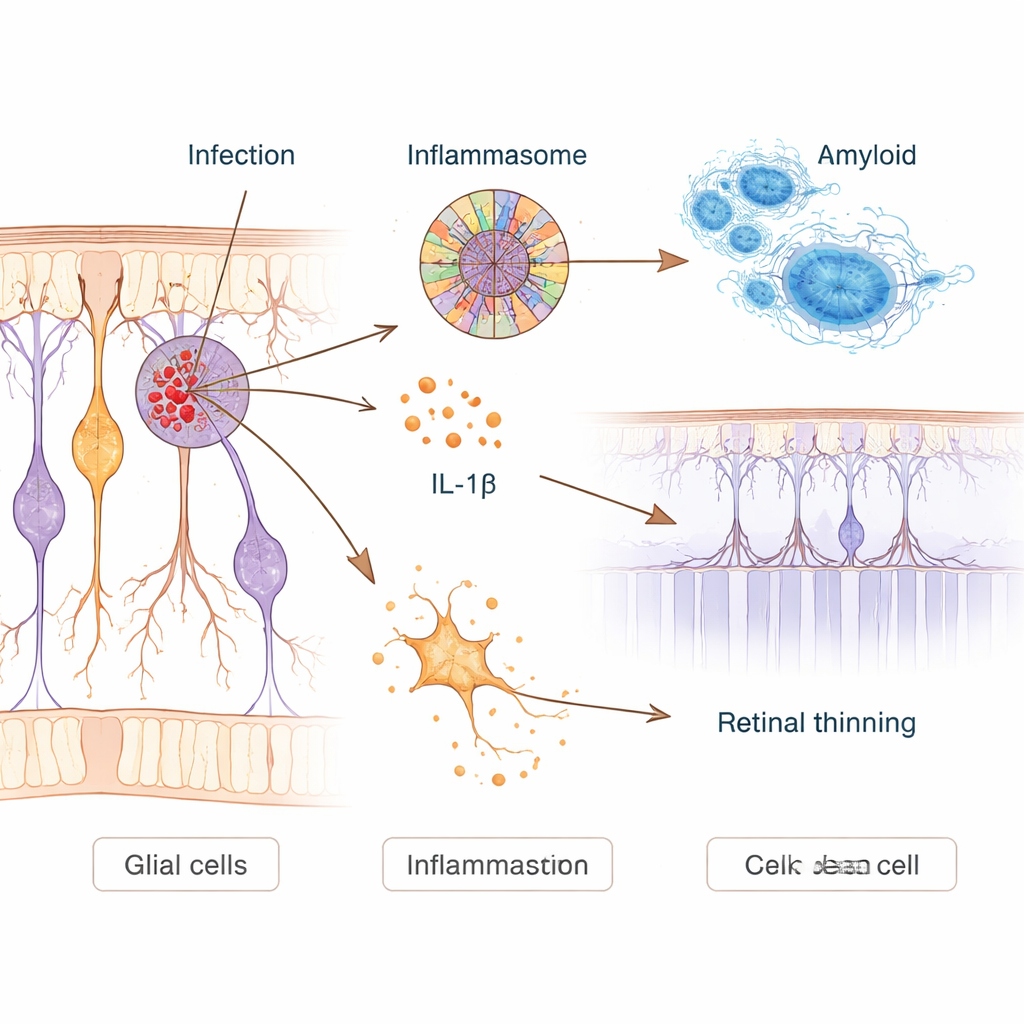
Comment l’infection peut déclencher une inflammation toxique
Pour explorer causalité et effets, les scientifiques ont infecté des cellules d’allure nerveuse humaines en culture et des souris modèles de l’Alzheimer avec Chlamydia pneumoniae. Dans les neurones en culture, l’infection a augmenté la production d’amyloïde‑bêta et activé un système d’alarme moléculaire appelé inflammasome NLRP3. Ce système agit comme un fil déclencheur cellulaire : une fois activé, il libère des messagers inflammatoires tels que l’interleukine‑1β et peut percer les membranes cellulaires, entraînant une forme explosive de mort cellulaire. Les neurones infectés présentaient des signes nets de dégâts membranaires et d’activation de ces voies. Chez la souris, une unique administration nasale de la bactérie suffisait à lui permettre d’atteindre le cerveau, où elle augmentait les plaques amyloïdes, activait les cellules immunitaires et détériorait la performance aux tâches de mémoire et d’orientation visuelle plusieurs mois plus tard.
Les cellules immunitaires rétiniennes sous pression
Dans les yeux humains, l’équipe a cartographié la manière dont l’infection interagit avec les cellules de soutien locales qui protègent normalement les neurones. Les astrocytes en étoile et les cellules de Müller, ainsi que la microglie — les cellules « nettoyeuses » résidentes du cerveau et de la rétine — se concentraient autour des sites infectés. Les signatures chimiques de l’inflammasome NLRP3 et de ses voies de mort en aval étaient fortement élevées dans les rétines de personnes atteintes d’Alzheimer, et commençaient déjà à augmenter chez celles présentant un déficit cognitif léger. De nombreuses cellules infectées portaient des marqueurs tant de la mort « pyroptotique » inflammatoire que de l’apoptose plus familière. Bien que davantage de microglies soient recrutées dans les rétines d’Alzheimer, chaque bactérie semblait être contactée ou engloutie par moins de microglies que dans les yeux sains, ce qui suggère que le système de nettoyage devient surchargé ou déficient à mesure que la maladie progresse.
Lire la santé du cerveau grâce à l’œil
Parce que la rétine est accessible à l’imagerie haute résolution chez les personnes vivantes, les chercheurs se sont demandés si des mesures rétiniennes liées à Chlamydia pneumoniae pouvaient aider à prédire le statut Alzheimer. Ils ont utilisé des modèles d’apprentissage automatique pour combiner les niveaux d’infection rétinienne avec des marqueurs tels que les dépôts d’amyloïde‑bêta, l’inflammation et l’amincissement local des tissus. Certaines combinaisons — en particulier la présence de bactéries rétiniennes associée à l’amyloïde — distinguaient les patients Alzheimer des témoins avec une grande précision et suivaient le stade de la maladie ainsi que les scores cognitifs. Bien que des travaux supplémentaires et des études plus vastes soient nécessaires, les résultats suggèrent qu’un test simple basé sur l’œil pourrait un jour révéler non seulement les changements classiques de l’Alzheimer mais aussi une composante infectieuse cachée, ouvrant la voie à un usage précoce d’antibiotiques ou de médicaments qui atténuent l’inflammasome chez les personnes à risque.
Ce que cela pourrait signifier pour les patients
Pour le grand public, le message clé est que la maladie d’Alzheimer n’est peut‑être pas seulement provoquée par des protéines déraillant ; des infections de longue date pourraient alimenter un feu qui couve. Cette étude apporte des preuves solides qu’une bactérie respiratoire commune peut s’installer dans la rétine et le cerveau, déclencher une inflammation dommageable et aggraver la perte de mémoire chez des individus susceptibles. Si de futurs essais cliniques confirment que traiter de telles infections ou bloquer la voie de l’inflammasome ralentit le déclin, l’imagerie rétinienne de routine et des thérapies ciblées pourraient devenir partie intégrante d’une approche plus proactive et personnalisée pour prévenir ou retarder la démence.
Citation: Gaire, B.P., Koronyo, Y., Vit, JP. et al. Identification of Chlamydia pneumoniae and NLRP3 inflammasome activation in Alzheimer’s disease retina. Nat Commun 17, 771 (2026). https://doi.org/10.1038/s41467-026-68580-4
Mots-clés: Maladie d’Alzheimer, rétine, Chlamydia pneumoniae, neuroinflammation, amyloïde-bêta