Clear Sky Science · fr
Les HIF soutiennent un circuit de régulation transcriptionnelle de l'expression d'EPAS1 dans le carcinome rénal à cellules claires
Pourquoi le cancer du rein mérite qu'on s'y attarde
Le carcinome rénal à cellules claires est la forme la plus fréquente de cancer du rein, et de nombreux patients reçoivent aujourd'hui des médicaments qui bloquent une protéine appelée HIF‑2α. Ces traitements peuvent réduire la taille des tumeurs, mais ils ne sont pas également efficaces pour tous. Cette étude pose une question simple mais importante : qu'est-ce qui conduit certaines tumeurs rénales à produire autant de HIF‑2α, et la compréhension de ce « interrupteur » peut‑elle nous aider à prédire qui bénéficiera le plus du traitement et à concevoir de nouvelles thérapies ?
Le capteur d'oxygène qui part à la dérive
Les cellules rénales saines utilisent une protéine de sécurité appelée VHL pour garder les facteurs de détection d'oxygène, connus sous le nom de HIF, sous contrôle strict. Quand l'oxygène est abondant, VHL marque les protéines HIF pour leur destruction, les empêchant d'activer des gènes qui favorisent la formation de vaisseaux sanguins et la division cellulaire. Dans le cancer rénal à cellules claires, VHL est généralement perdu ou altéré. En conséquence, un membre de la famille HIF, HIF‑2α (codé par le gène EPAS1), échappe à la destruction et s'accumule. Des travaux antérieurs ont montré qu'une forte activité de HIF‑2α est liée à une croissance tumorale plus rapide et à un pronostic plus défavorable, et que bloquer HIF‑2α peut ralentir ou arrêter les tumeurs chez certains patients. Cependant, les étapes moléculaires qui augmentent l'activité du gène EPAS1 dans les tumeurs rénales n'étaient pas bien comprises.
Un interrupteur d'ADN caché pour un gène du cancer
En utilisant des échantillons tumoraux de patients, des données unicellulaires et des modèles cellulaires cancéreux, les auteurs montrent que l'ARN messager de HIF‑2α est nettement plus élevé dans les tumeurs rénales à cellules claires que dans le tissu rénal normal ou d'autres types de tumeurs rénales. Ils examinent ensuite la région EPAS1 du génome à la recherche de marques chimiques et structurales signalant de l'ADN régulateur actif. Cela révèle un enhancer puissant — une sorte d'interrupteur génique à longue distance — situé à environ 70 000 nucléotides en amont d'EPAS1 et spécifiquement actif dans les tumeurs à cellules claires. Dans les cellules tumorales, la chromatine à cet enhancer est ouverte, décorée de marques d'activation et se replie physiquement pour entrer en contact avec le promoteur d'EPAS1, tandis que dans les cellules tubulaires rénales normales cette région est en grande partie silencieuse. L'activité de cet enhancer corrèle avec des niveaux plus élevés d'EPAS1 dans de larges jeux de données sur le cancer. 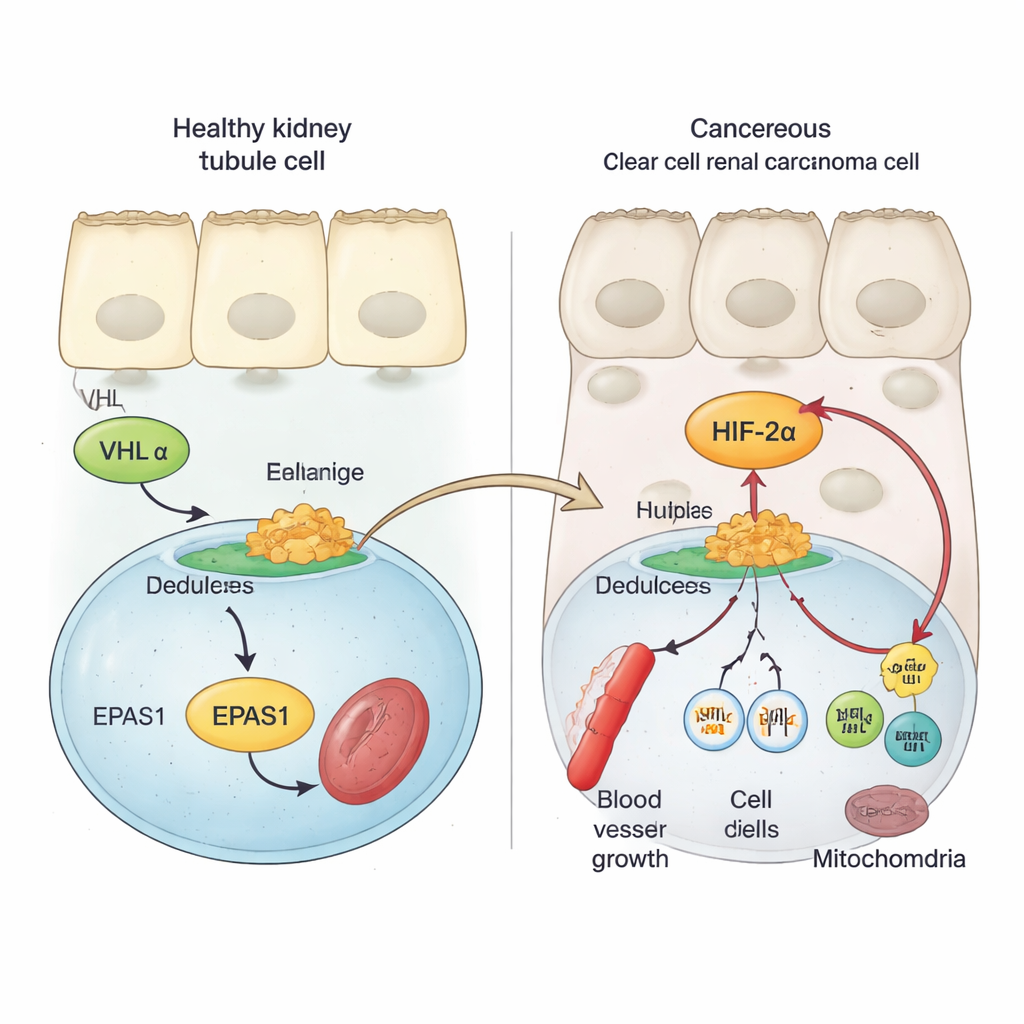
Une boucle auto‑renforçante pilotée par des facteurs d'identité rénale
L'étude montre que les protéines HIF font plus que répondre à l'hypoxie : elles contribuent en fait à stimuler leur propre production. Lorsque les chercheurs rétablissent VHL ou retirent une protéine partenaire clé des HIF (HIF‑1β), les niveaux d'EPAS1 chutent et l'enhancer devient moins accessible. Le cartographie directe des contacts protéine–ADN montre que HIF se lie à deux régions enhancers en amont d'EPAS1, y compris l'enhancer spécifique aux cellules claires. Dans les cellules tumorales rénales, cet enhancer est également occupé par PAX8 et HNF‑1β, des facteurs de transcription qui participent à l'identité des cellules rénales et sont connus pour soutenir la croissance tumorale. Perturber PAX8 ou HNF‑1β, ou muter leurs sites de liaison au sein de l'enhancer, réduit l'ARN et la protéine HIF‑2α et affaiblit l'activité de l'enhancer. Ensemble, ces résultats révèlent un circuit autorégulateur : HIF‑2α, en coopération avec des facteurs de lignée rénale, augmente l'activité d'un enhancer d'EPAS1, qui à son tour stimule la production de davantage de HIF‑2α.
Risque génétique et comportement tumoral convergent sur le même circuit
La région EPAS1 a longtemps été repérée dans des études pangénomiques comme un point chaud du risque de cancer du rein, certaines variantes héréditaires étant liées à des taux de cancer plus élevés et à des mutations de VHL dans les tumeurs. En combinant des données génétiques et des mesures d'expression génique, les auteurs montrent que les individus portant la version à haut risque d'une variante clé d'EPAS1 ont tendance à présenter des niveaux plus élevés de HIF‑2α dans leurs tumeurs — et même dans les cellules tubulaires rénales normales lorsque HIF est stabilisé expérimentalement. Cela suggère que des différences d'ADN héritées peuvent régler la sensibilité de l'enhancer, préparant certains reins à augmenter davantage HIF‑2α une fois que VHL est perdu. Des expériences dans des cellules de glioblastome montrent que le même enhancer peut aussi être mobilisé dans certains cancers cérébraux, laissant entendre que ce module régulateur peut être réutilisé dans d'autres cancers où HIF‑2α joue un rôle important. 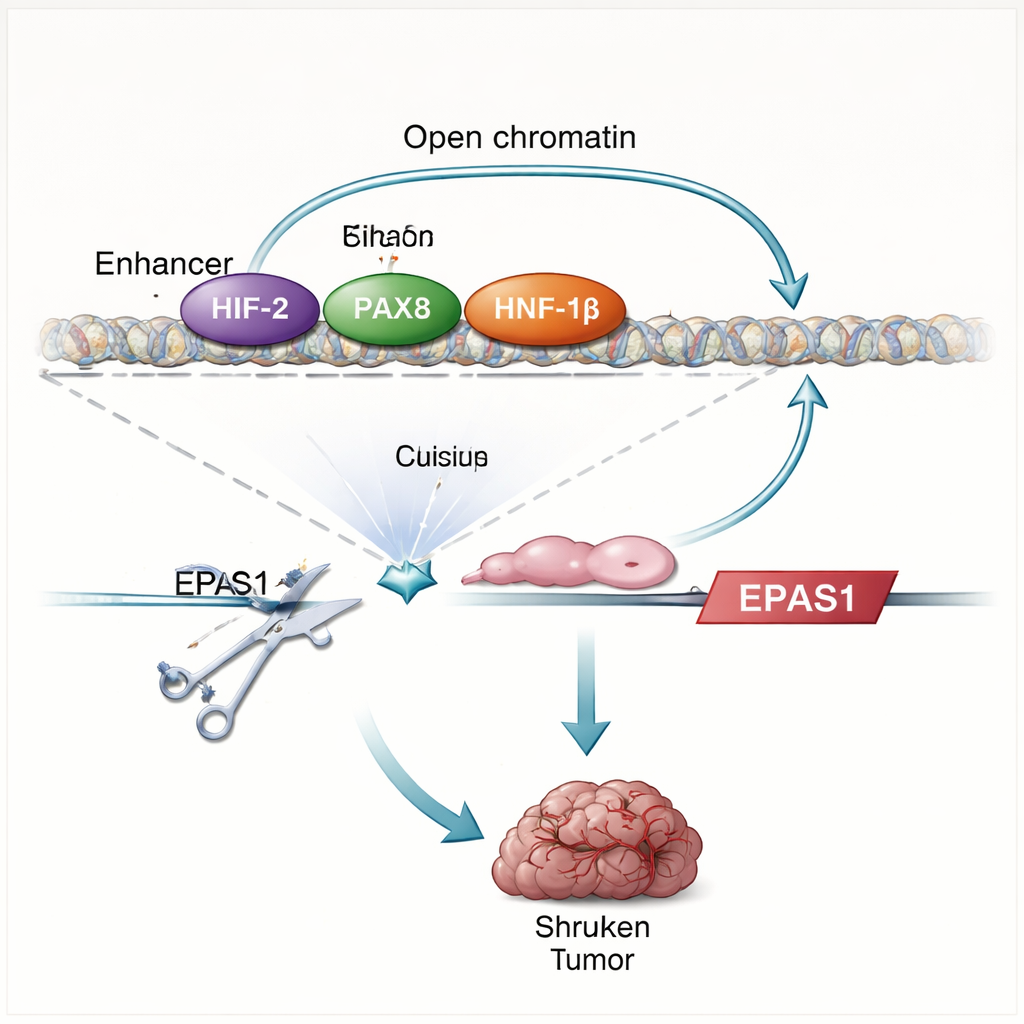
Briser la boucle pour arrêter la croissance tumorale
Pour tester l'importance de cet enhancer, l'équipe utilise l'édition génomique CRISPR pour endommager les motifs de liaison de HIF qu'il contient dans des lignées cellulaires de cancer du rein et des cellules tumorales fraîches de patients. Cette coupure réduit l'ARN de HIF‑2α d'environ un tiers à la moitié, diminue les niveaux de gènes cibles bien connus de HIF‑2α tels que CCND1 et VEGFA, et affaiblit le programme génique global d'hypoxie. Lorsque les cellules éditées sont implantées chez la souris, elles échouent en grande partie à former des tumeurs, contrairement aux cellules témoins. Le profil des changements d'expression après la perturbation de l'enhancer reflète étroitement les effets du blocage direct de HIF‑2α par un médicament clinique, soulignant que cet élément d'ADN unique est un moteur majeur de la voie HIF‑2α dans ces cancers.
Ce que cela signifie pour les patients et les thérapies
Pour un public non spécialiste, le message clé est que les auteurs ont mis au jour un interrupteur d'ADN auto‑amplificateur qui maintient activée une protéine promotrice du cancer majeure, HIF‑2α, dans les tumeurs rénales à cellules claires. Cet interrupteur dépend à la fois de la perte du frein de sécurité VHL et de protéines auxiliaires spécifiques du rein, et il est influencé par des variantes génétiques héritées. Parce que l'enhancer est fortement actif dans de nombreuses tumeurs à cellules claires et qu'il est étroitement lié à l'intensité de la voie HIF‑2α, mesurer son activité — ou le cibler directement — pourrait aider à identifier les patients qui bénéficieront le plus des inhibiteurs actuels de HIF‑2α et offrir de nouvelles façons d'éteindre cette voie lorsque les tumeurs deviennent résistantes aux médicaments.
Citation: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Mots-clés: carcinome rénal à cellules claires, HIF-2α, enhancer d'EPAS1, mutation de VHL, génétique du cancer du rein