Clear Sky Science · fr
Réaction CuAAC interrompue atroposélective utilisant des diaryliodoniums cycliques
Pourquoi cette nouvelle chimie compte
Les chimistes s'appuient depuis longtemps sur une réaction de « click » simple pour assembler rapidement et proprement des blocs moléculaires, une astuce qui soutient tout, de la découverte de médicaments aux matériaux autoréparants. Cet article décrit une savante variante de cette réaction click classique qui permet de construire des molécules tridimensionnelles plus complexes avec une main- figure précise — des structures très recherchées en médecine moderne et dans les matériaux avancés.
Donner une nouvelle fonction à une réaction click classique
Le point de départ est la cycloaddition azide–alcyne catalysée par le cuivre, souvent appelée simplement CuAAC. Elle relie deux petits composants — un azide et un alcyne — en un cycle à cinq membres appelé triazole, sous des conditions douces et avec une fiabilité remarquable. Traditionnellement, une fois que le cuivre aide à former l'anneau de triazole, la réaction s'arrête là. Ces dernières années, cependant, les chimistes ont appris à « interrompre » ce processus, en capturant un intermédiaire cuivre–triazole éphémère avec un troisième partenaire pour construire des produits plus élaborés. Jusqu'à présent, ces interruptions n'ont pas permis de contrôler de manière générale la main molecular (chiralité), limitant leur utilité pour fabriquer des molécules chirales sophistiquées.
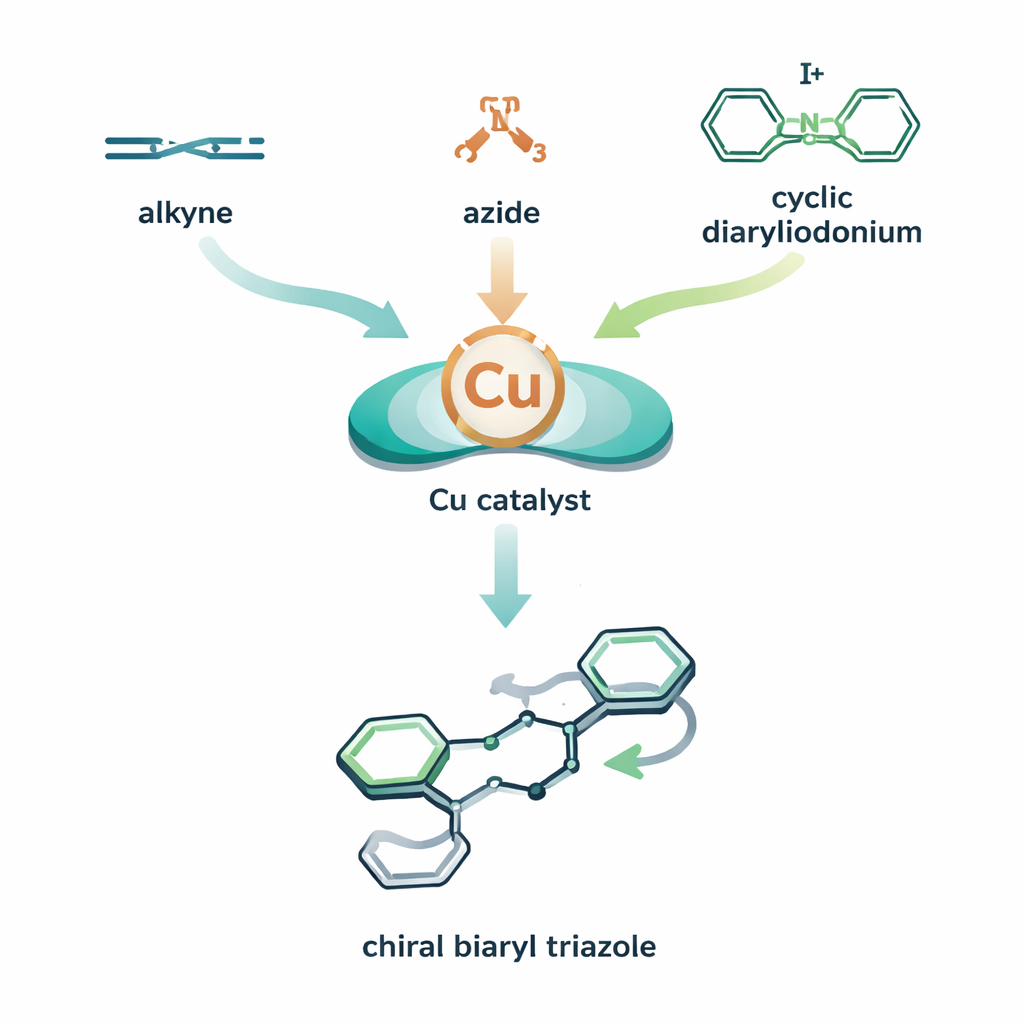
Un puzzle moléculaire en trois pièces avec une torsion
Les auteurs combinent deux cycles réactionnels à base de cuivre en un seul processus orchestré. Dans leur conception, un catalyseur au cuivre aide d'abord l'alcyne et l'azide à former un intermédiaire cuivre–triazole. Avant que cet intermédiaire ne soit neutralisé, un troisième composant — une molécule cyclique riche en iode et très réactive appelée diaryliodonium cyclique — est introduit. Le cuivre s'insère dans cet anneau puis l'ouvre, greffant l'un de ses noyaux aromatiques sur le triazole. Le résultat est un triazole biaryle : deux systèmes d'anneaux reliés autour d'une liaison qui peut agir comme un axe chiral, à la manière d'une hélice pouvant tourner vers la gauche ou la droite. En associant le cuivre à un ligand chiral soigneusement choisi, l'équipe oriente le processus de sorte qu'une torsion se forme beaucoup plus que l'autre, obtenant une forte atroposélectivité (contrôle de la « main » axiale formée).
Tester la souplesse et la robustesse de la méthode
Pour évaluer la généralité possible de cette réaction, les chercheurs ont fait varier systématiquement chacun des trois blocs de construction. Ils ont montré que de nombreux alcynes différents, y compris ceux portant des noyaux électronriches, électroattracteurs et hétéroaromatiques, peuvent participer tout en donnant de bons rendements et une nette préférence pour une forme chirale. Certaines substitutions volumineuses amélioraient la sélectivité mais pouvaient réduire le rendement, révélant un compromis entre encombrement stérique et efficacité. Les partenaires azides donnaient les meilleurs résultats lorsqu'ils provenaient d'esters simples, d'amides ou de positions benzyliques, et une gamme de tels azides a fourni des produits chiralement enrichis. Le composant diaryliodonium cyclique a également pu être ajusté : certaines substitutions préservaient à la fois rendement et sélectivité, tandis que d'autres, en particulier près du centre iodé réactif, ralentissaient la réaction ou en diminuaient les performances. Dans l'ensemble, l'étude a livré une large collection de nouveaux triazoles biaryles atropoisomères accessibles en une seule étape.
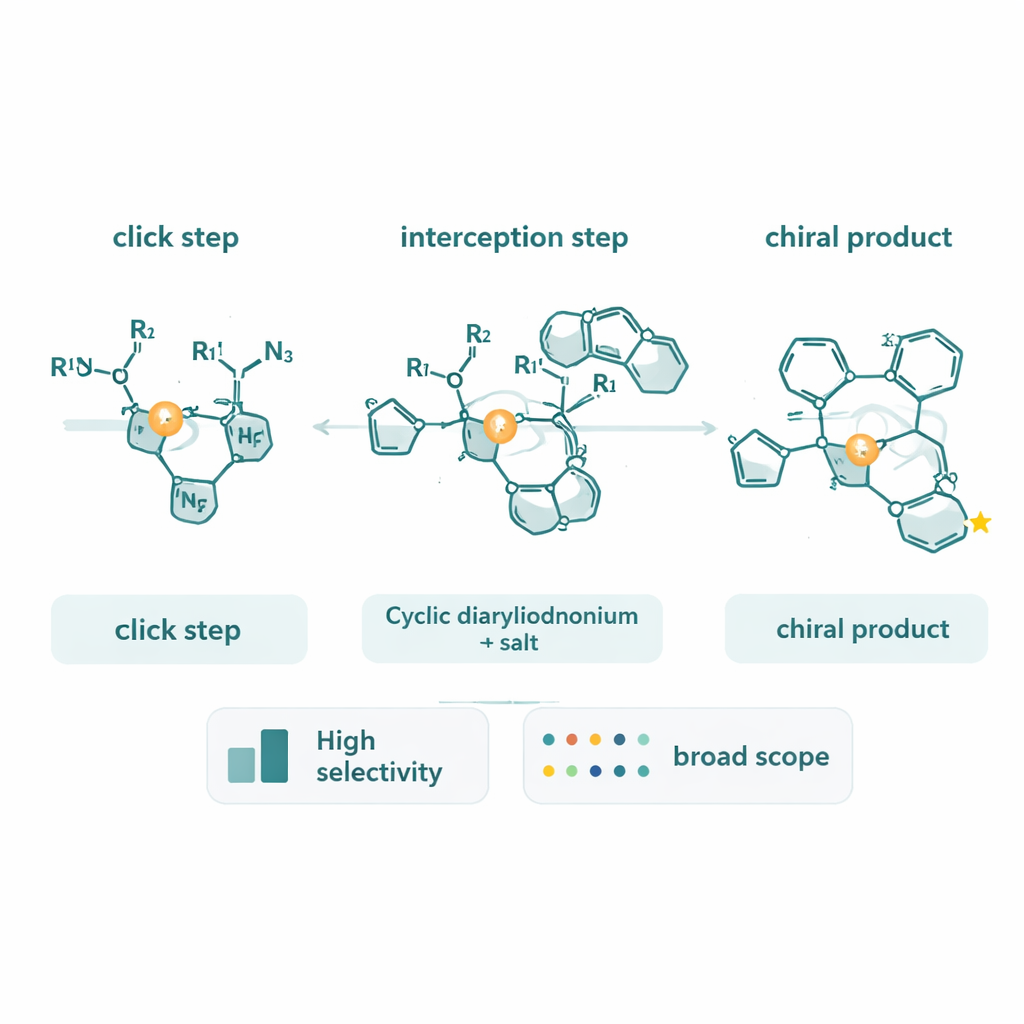
Regarder sous le capot de la réaction
Au-delà de la synthèse de nouvelles molécules, l'équipe a consacré des efforts importants à élucider le mécanisme réel de la réaction. En utilisant des alcynes marqués au deutérium, ils ont observé un effet isotope cinétique inverse inhabituel, ce qui indique une étape limitante en vitesse où le carbone de l'alcyne change son caractère de liaison plutôt que de simplement rompre une liaison C–H. Des analyses calorimétriques de l'avancement de la réaction ont montré que la vitesse dépend fortement des concentrations d'alcyne et d'azide, mais seulement faiblement de celle du diaryliodonium cyclique. Ces mesures soutiennent un scénario dans lequel la formation et la transformation du complexe cuivre–triazole, et son addition oxydative dans l'anneau de diaryliodonium, déterminent ensemble le rythme de la réaction. Ils ont également constaté que les produits triazoles chiraux peuvent se lier au cuivre et ralentir le catalyseur, suggérant des pistes pour optimiser davantage le système.
Ce que cela implique pour la suite
En termes simples, les chercheurs ont appris à une réaction click bien connue un nouveau tour : au lieu de simplement assembler deux pièces, elle aide désormais à unir trois composants en molécules complexes en forme d'hélice tout en sélectionnant presque exclusivement une torsion préférentielle. Cela fournit une voie évolutive vers des triazoles biaryles chiraux, des structures précieuses comme candidats médicaments, catalyseurs et matériaux fonctionnels. Les éclairages mécanistiques — notamment la façon dont l'intermédiaire clé est intercepté et comment le produit peut empoisonner le catalyseur — offrent une feuille de route pour concevoir des versions encore plus efficaces et sélectives de cette chimie. Pour les non-spécialistes, l'idée principale est qu'un outil moléculaire de type « Lego » déjà puissant vient de devenir plus polyvalent, permettant aux chimistes de construire des formes plus complexes et plus utiles avec un contrôle fin de leur configuration tridimensionnelle.
Citation: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Mots-clés: chimie click, catalyse au cuivre, biaryle chiral, atropoisomère, triazole