Clear Sky Science · fr
Biomarqueurs de réponse au palbociclib en néoadjuvant associé à l’anastrozole dans le cancer du sein résumé hormonal‑résistant ER‑positif/HER2‑négatif : essai de phase 2
Pourquoi cette recherche compte pour les patientes et leurs proches
De nombreuses femmes atteintes d’une forme fréquente de cancer du sein répondent d’abord bien aux traitements bloquant les hormones, pour voir ensuite leurs tumeurs devenir résistantes et recommencer à croître. Cette étude pose une question urgente : ajouter un médicament plus récent qui bloque le cycle cellulaire à l’hormonothérapie standard peut‑il aider dans ces cas difficiles, et peut‑on repérer dans la tumeur des signes avant‑coureurs indiquant qui bénéficiera — ou non — du traitement ?
Un examen des cancers du sein récalcitrants
L’essai s’est concentré sur les cancers du sein récepteurs d’oestrogène positifs, HER2‑négatifs, le sous‑type le plus fréquent. Les 34 patientes avaient déjà reçu une hormonothérapie préopératoire standard (un inhibiteur de l’aromatase) mais présentaient encore une activité de prolifération tumorale, ce qui classait le cancer comme « résistant endocrine ». Les chercheur·e·s ont ensuite traité ces patientes avant chirurgie par la combinaison de l’anastrozole (hormonothérapie) et du palbociclib (bloqueur du cycle cellulaire). Ils ont mesuré la vitesse de division des cellules tumorales à l’aide d’un marqueur appelé Ki67. Si Ki67 chute à des niveaux très bas après deux semaines, on parle d’« arrêt complet du cycle cellulaire », indiquant que la division des cellules cancéreuses a été efficacement interrompue.
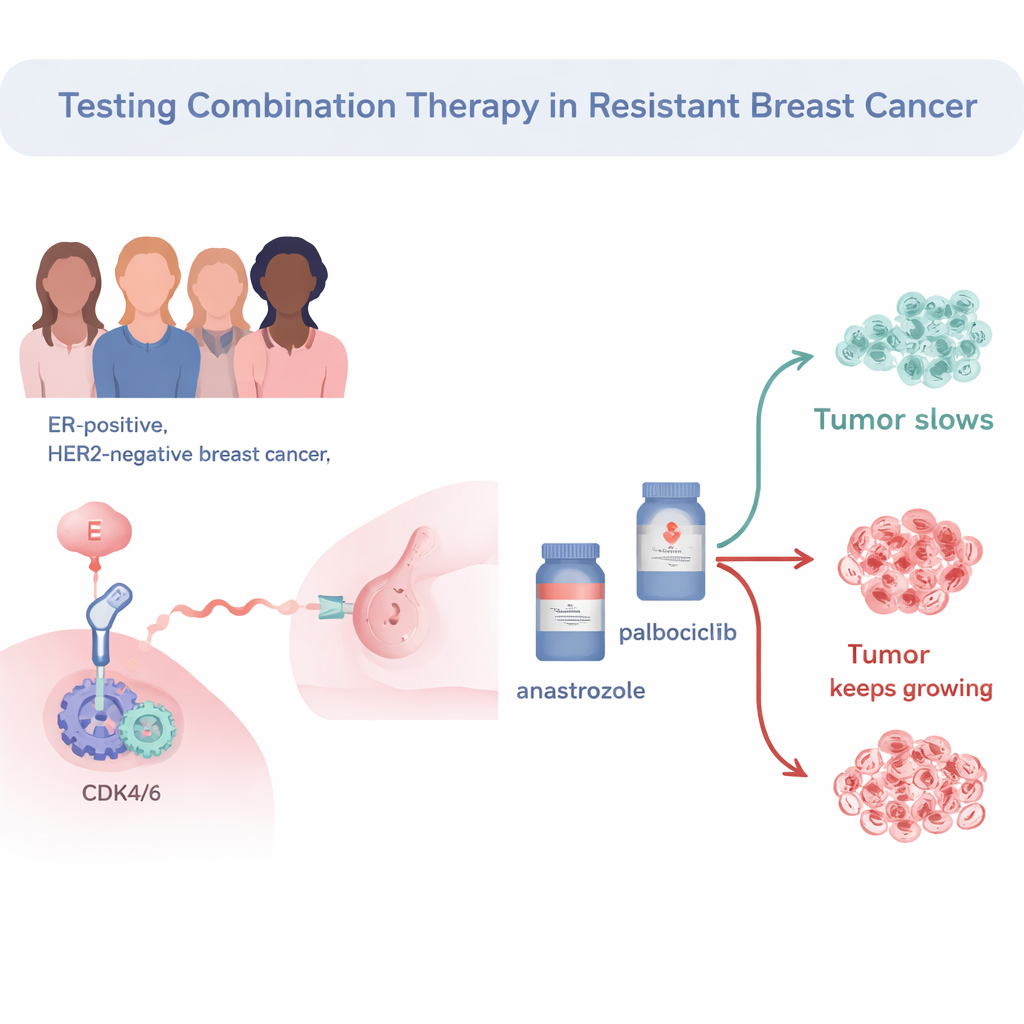
Qui a répondu à la combinaison médicamenteuse ?
Parmi les 33 patientes dont les tumeurs ont pu être évaluées complètement, 57,6 % ont atteint l’arrêt complet du cycle cellulaire après seulement deux semaines de traitement combiné. Avec un seuil plus modeste — classer les tumeurs comme « sensibles » si Ki67 tombait en dessous de 10 % — environ deux tiers des tumeurs étaient considérées comme réactives. Les patientes dont les tumeurs restaient très actives selon Ki67 avaient tendance à présenter des cancers plus agressifs : grade plus élevé, taille plus importante et niveaux initiaux de Ki67 plus élevés. Elles étaient aussi plus susceptibles d’appartenir aux sous‑types moléculaires dits « non‑luminaux », qui se comportent généralement de façon plus agressive que les tumeurs « luminales A » classiques, dépendantes des hormones.
Qu’est‑ce qui rend certaines tumeurs résistantes au traitement ?
L’équipe est allée au‑delà des simples taux de réponse et a analysé en profondeur les échantillons tumoraux par séquençage de l’ADN, séquençage de l’ARN et profilage protéique. Les tumeurs résistantes n’étaient pas définies par une seule mutation ; elles présentaient plutôt un schéma de « surtension » des circuits. Par rapport aux tumeurs sensibles, les cancers résistants affichaient une signalisation du récepteur aux œstrogènes affaiblie mais une activité renforcée dans des voies favorisant la division et la croissance cellulaires, telles que les gènes du cycle cellulaire, la voie de croissance mTOR, et plusieurs réseaux inflammatoires et liés à l’interféron. Ils présentaient également des niveaux accrus de « freins » immunitaires, appelés points de contrôle immunitaire, incluant des gènes comme IDO1 et PD‑L1 qui aident les tumeurs à échapper aux défenses de l’organisme.
Des voies biologiques vers de potentielles nouvelles thérapies
Pour vérifier si ces voies hyperactives pouvaient être exploitées contre le cancer, les chercheur·e·s ont créé des modèles cellulaires en laboratoire devenus résistants aux inhibiteurs CDK4/6 comme le palbociclib. Ces cellules résistantes présentaient la même signature d’activation accrue du cycle cellulaire et de la signalisation interféron/inflammatoire observée dans les tumeurs des patientes. Lorsqu’elles ont été exposées à des médicaments bloquant la signalisation JAK‑STAT — une voie clé en aval de l’interféron — un médicament, le pacritinib, s’est montré particulièrement efficace pour ralentir la croissance des cellules résistantes et des organoïdes tumoraux dérivés de patientes. Cela suggère que l’association d’inhibiteurs CDK4/6 avec certains médicaments ciblant JAK pourrait être une stratégie prometteuse pour les patientes dont les cancers ont contourné les combinaisons actuelles.
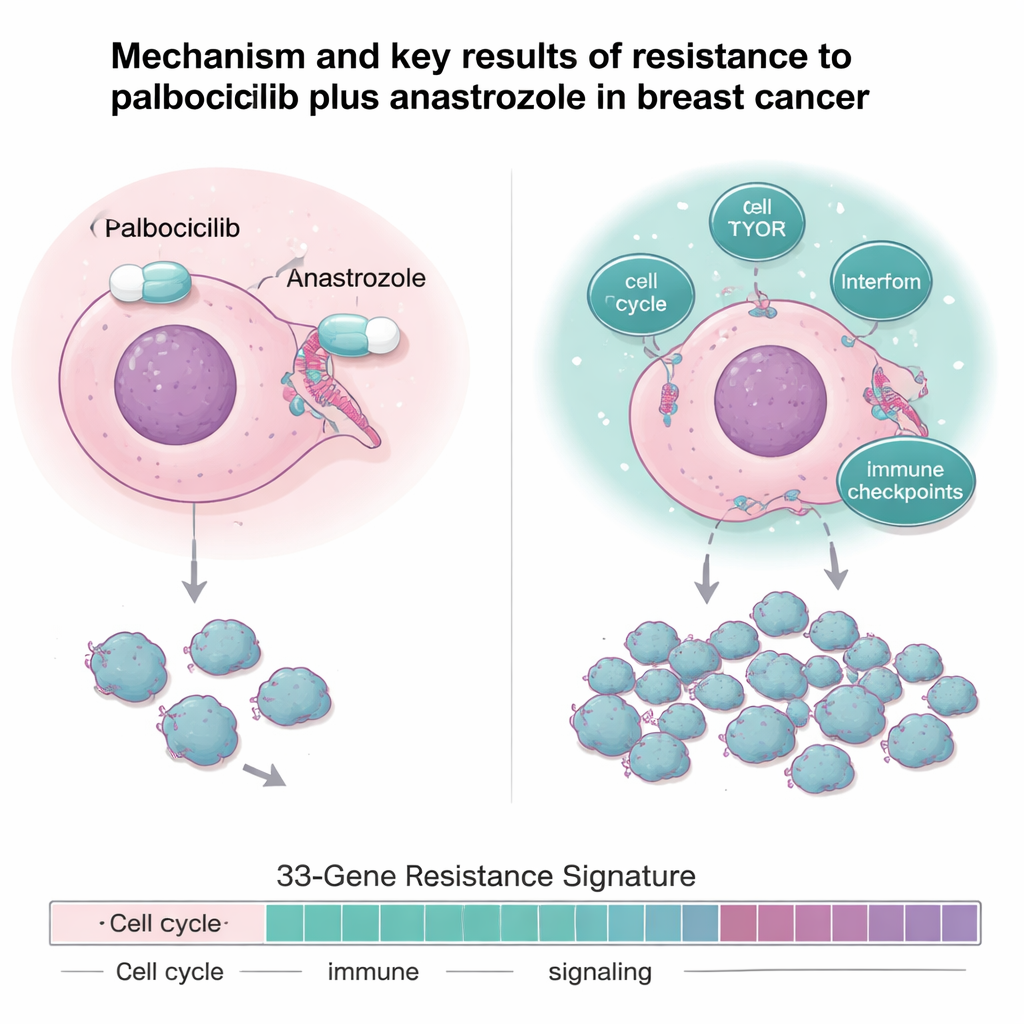
Une empreinte génique qui prédit l’issue
En comparant tumeurs sensibles et résistantes dans deux essais apparentés, les investigateur·rice·s ont construit une « signature de résistance » de 33 gènes regroupant des gènes impliqués dans la division cellulaire, la réparation de l’ADN, la signalisation de croissance, le métabolisme et les réponses immunitaires/inflammatoires. Cette empreinte génique distinguait très précisément tumeurs sensibles et résistantes dans l’essai. Fait important, lorsqu’on a appliqué le même profil de 33 gènes à un groupe indépendant de 151 patientes atteintes d’un cancer du sein métastatique traité en pratique courante par des inhibiteurs CDK4/6 plus hormonothérapie, celles dont les cancers obtenaient un score élevé pour la signature de résistance ont eu un délai médian de progression plus court et une survie globale plus courte. Autrement dit, ce profil de 33 gènes, mesuré avant traitement, pourrait repérer les patientes moins susceptibles de bénéficier longtemps des schémas standards à base de CDK4/6.
Ce que cela signifie pour la prise en charge future
Pour les personnes confrontées à un cancer du sein ER‑positif résistant aux hormones, cette étude apporte à la fois des éléments rassurants et une feuille de route. Elle montre que l’ajout de palbociclib à l’anastrozole peut encore arrêter la croissance tumorale dans plus de la moitié des cas résistants. Mais elle révèle aussi que certaines tumeurs s’appuient sur des voies alternatives de croissance et des mécanismes liés à l’immunité, ce qui les rend plus difficiles à contrôler. La nouvelle signature de 33 gènes et la découverte que des médicaments ciblant JAK comme le pacritinib peuvent freiner les cellules résistantes ouvrent la voie à une prise en charge plus personnalisée : identifier tôt celles qui risquent de ne pas répondre aux combinaisons standard et les orienter plus rapidement vers des essais évaluant de nouveaux partenaires médicamenteux ciblant directement les voies de survie alternatives du cancer.
Citation: Kong, T., Mabry, A., Highkin, M. et al. Biomarkers of response to neoadjuvant palbociclib plus anastrozole in endocrine-resistant estrogen receptor-positive/HER2-negative breast cancer: a phase 2 trial. Nat Commun 17, 949 (2026). https://doi.org/10.1038/s41467-026-68570-6
Mots-clés: Cancer du sein ER‑positif, Inhibiteurs CDK4/6, Résistance endocrine, Biomarqueurs tumoraux, palbociclib anastrozole