Clear Sky Science · fr
Une analyse multimodale démêle les associations génétiques et microbiennes entre la maladie inflammatoire chronique de l’intestin et d’autres maladies immunitaires dans un cadre populationnel harmonisé
Pourquoi certaines maladies immunitaires se présentent en groupe
De nombreuses personnes atteintes d’une maladie inflammatoire chronique de l’intestin (MICI) – une inflammation prolongée de l’intestin – développent également d’autres affections liées au système immunitaire, comme l’arthrite, le psoriasis ou la sclérose en plaques. Les cliniciens observent ces recoupements quotidiennement, mais il était jusqu’ici difficile de déterminer dans quelle mesure ils sont dus à des gènes communs, à l’environnement quotidien ou aux microbes qui vivent dans nos intestins. Cette étude utilise des données nationales danoises, de larges jeux de données génétiques et des profils du microbiote intestinal pour démêler pourquoi certaines maladies immunitaires ont tendance à se regrouper et pourquoi la maladie de Crohn et la rectocolite hémorragique, les deux principales formes de MICI, ne se comportent pas toujours de la même manière.
Suivre les trajectoires de maladie au sein des familles
Les chercheurs ont commencé par cartographier un arbre généalogique gigantesque de la population danoise moderne en utilisant les données du registre civil qui relient parents, enfants et frères et sœurs. En se focalisant sur plus de deux millions et demi de frères et sœurs nés entre 1910 et 2010, ils ont examiné la fréquence de survenue de la maladie de Crohn ou de la rectocolite hémorragique en association avec 23 autres maladies inflammatoires médiées par le système immunitaire, dont la polyarthrite rhumatoïde, le psoriasis, le diabète de type 1, la sclérose en plaques et le lupus. Ils ont constaté que la maladie de Crohn et la rectocolite hémorragique se transmettent fortement au sein des familles, mais avec des « compagnons » différents. Par exemple, les deux maladies intestinales étaient clairement liées dans les familles au psoriasis, à l’arthrite psoriasique, à la polyarthrite rhumatoïde et à la spondylarthrite ankylosante, tandis que la rectocolite hémorragique — mais pas la maladie de Crohn — montrait des liens familiaux notables avec des affections comme la sarcoïdose et le lupus.
Plongée dans les gènes partagés
Les schémas familiaux peuvent refléter des gènes partagés, un environnement partagé, ou les deux. Pour séparer ces influences, l’équipe s’est tournée vers des études d’association pangénomique, qui analysent des centaines de milliers de marqueurs génétiques à travers le génome dans de larges groupes de patients. Ils ont quantifié la part de risque génétique de la maladie de Crohn et de la rectocolite hémorragique qui est partagée avec d’autres maladies immunitaires. Comme attendu, les deux affections intestinales partageaient une assise génétique solide. Au‑delà de ce noyau, cependant, leurs affinités génétiques divergeaient. La maladie de Crohn montrait un recoupement génétique positif avec l’asthme, le psoriasis, l’arthrite psoriasique et la polyarthrite rhumatoïde, tandis que la rectocolite hémorragique partageait davantage de risque génétique avec le diabète de type 1 et la cholangite biliaire primitive, une maladie du foie. De manière frappante, les deux types de MICI présentaient des corrélations génétiques négatives avec la sclérose en plaques, et la rectocolite hémorragique aussi avec le lupus, ce qui suggère que certains variants génétiques qui augmentent la probabilité d’inflammation intestinale peuvent en réalité protéger contre certaines maladies neurologiques ou immunitaires systémiques.
Écouter « l’accent » microbien de l’intestin
Les gènes ne racontent qu’une partie de l’histoire. Les auteurs ont aussi rassemblé des données de microbiote fécal provenant de milliers de personnes dans le monde, retraitant toutes les lectures de séquençage 16S rRNA de façon harmonisée afin que les souches bactériennes puissent être comparées entre études. Pour sept maladies immunitaires, ils ont construit des « profils microbiotes de maladie » — des synthèses statistiques de la manière dont des centaines de variantes bactériennes diffèrent entre patients et témoins sains. La comparaison de ces profils a révélé que la maladie de Crohn et la rectocolite hémorragique partagent des perturbations microbiennes globalement similaires, et que les deux se recoupent fortement avec la polyarthrite rhumatoïde et la maladie cœliaque. Pourtant, la rectocolite hémorragique présentait aussi des similitudes de microbiome avec la sclérose en plaques et la maladie de Graves même lorsque le recoupement génétique avec ces affections était faible ou négatif. Ce décalage entre gènes et microbes souligne le rôle puissant de l’environnement et du mode de vie — notamment les médicaments, l’alimentation et l’exposition aux antibiotiques — dans la formation de signatures microbiennes communes à des maladies immunitaires apparemment éloignées.
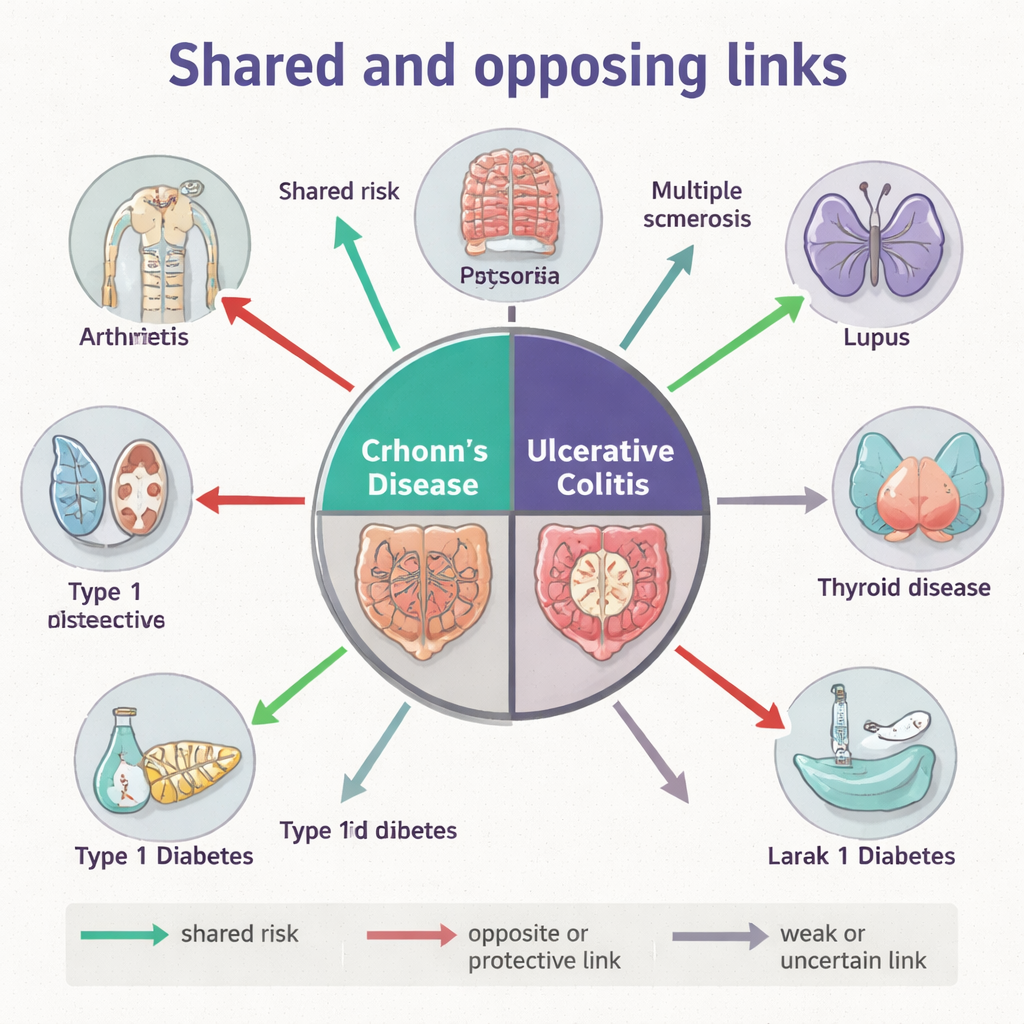
Ce que cela signifie pour les patients et les médecins
Pris ensemble, les couches familiale, génétique et microbienne révèlent que la maladie de Crohn et la rectocolite hémorragique ne sont pas des étiquettes interchangeables mais des membres distincts de la famille des maladies immunitaires. Certaines affections, comme le psoriasis et certaines formes d’arthrite, montrent des connexions cohérentes à travers les trois couches, ce qui laisse entrevoir une biologie profondément partagée. D’autres, comme la sclérose en plaques et le lupus, affichent une relation presque de type « pousse‑tire », où les effets génétiques et les profils microbiens vont en sens opposé. Ces nuances aident à expliquer pourquoi les personnes atteintes de MICI peuvent présenter des constellations très différentes d’autres problèmes immunitaires et pourquoi un même médicament peut aider dans une maladie mais être inefficace ou nuisible dans une autre.
Perspectives : vers des soins plus individualisés
Pour un lectorat non spécialisé, le message clé est que les maladies immunitaires ne surviennent pas isolément. Cette étude montre que la probabilité de développer une combinaison particulière d’affections dépend d’un mélange changeant de gènes hérités, d’antécédents familiaux et de la vie microscopique de l’intestin. Elle soutient l’idée que la maladie de Crohn et la rectocolite hémorragique doivent être étudiées et traitées comme des entités liées mais distinctes, avec une attention soigneuse au profil immunitaire et à l’histoire familiale de chaque patient. À l’avenir, la combinaison de scores de risque génétique et de signatures du microbiome pourrait aider les médecins à mieux prédire quelles affections immunitaires additionnelles une personne atteinte de MICI pourrait développer et à concevoir des stratégies de prévention et de traitement réellement personnalisées plutôt qu’universelles.
Citation: Vestergaard, M.V., Alfaro-Núñez, A., Sazonovs, A. et al. Multimodal analysis disentangles the genetic and microbial associations between inflammatory bowel disease and other immune-mediated diseases across a harmonized population framework. Nat Commun 17, 1849 (2026). https://doi.org/10.1038/s41467-026-68564-4
Mots-clés: maladie inflammatoire de l’intestin, comorbidité auto-immune, microbiote intestinal, corrélation génétique, maladie de Crohn et rectocolite hémorragique