Clear Sky Science · fr
Briser la paroi cellulaire pour une livraison efficace d’ADN aux diatomées
Les algues comme mini‑usines vertes
Les diatomées — des algues microscopiques qui dérivent dans les océans — produisent discrètement environ un cinquième du carbone organique de la planète, contribuant à nourrir les réseaux trophiques marins et à séquestrer le dioxyde de carbone. Les scientifiques cherchent à transformer ces organismes robustes et à croissance rapide en mini‑usines vertes capables de fabriquer carburants, aliments et produits chimiques de spécialité. Mais un obstacle majeur subsiste : il est étonnamment difficile d’introduire de nouveaux ADN dans les cellules de diatomées de manière fiable. Cette étude s’attaque directement à ce problème pratique, décrivant de nouvelles façons de faire passer des instructions génétiques et des outils d’édition du génome à travers la paroi externe résistante des diatomées.
Assouplir la coquille des microbes marins
Les travaux portent sur la diatomée modèle Phaeodactylum tricornutum, prisée des laboratoires parce que son génome est bien cartographié et qu’elle dispose déjà de quelques outils génétiques de base. Les auteurs ont émis l’hypothèse que la paroi cellulaire, la première barrière physique que doit franchir tout ADN, constituait un goulot d’étranglement clé. En traitant les cellules avec une enzyme appelée alcalase, ils ont partiellement ou complètement retiré cette paroi, créant des « spheroplastes » et « protoplastes » fragiles et bien plus faciles à pénétrer. Lorsqu’ils ont ensuite utilisé l’électroporation — de brefs impulsions électriques qui ouvrent des pores temporaires — le nombre de transformants réussis a considérablement augmenté, d’environ deux ordres de grandeur par rapport aux méthodes antérieures. De très faibles quantités d’ADN, aussi faibles qu’un nanogramme, suffisaient à récupérer des cellules modifiées. 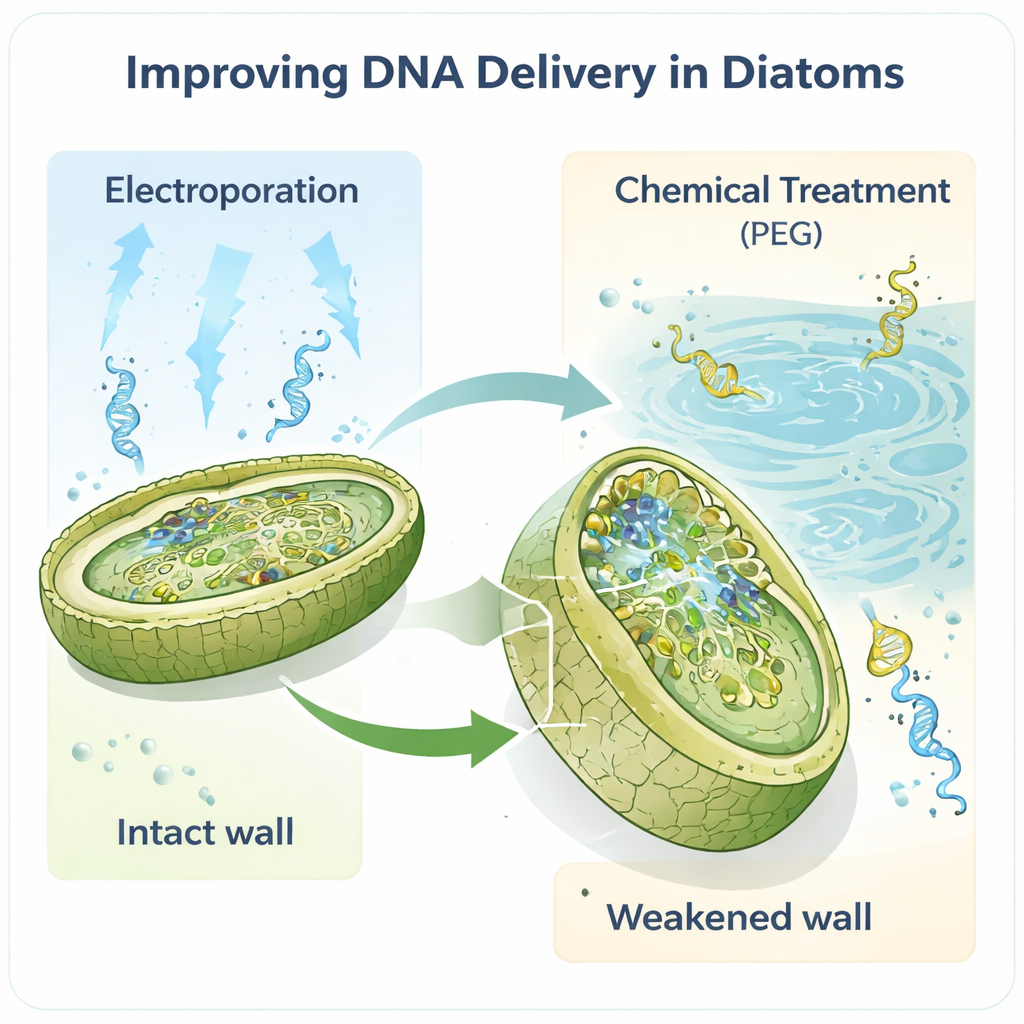
Livraison rapide d’ADN sans détour par des bactéries
Les méthodes traditionnelles de modification des diatomées reposent souvent sur des « coursiers » bactériens pour transporter de larges molécules d’ADN circulaires, appelées épiosomes, vers les algues. Bien que efficaces, ces approches sont lentes, techniquement exigeantes et peuvent déstabiliser des constructions d’ADN fragiles. Les nouveaux protocoles montrent que l’électroporation et une méthode chimique au polyéthylène glycol (PEG) affinée peuvent transférer les épiosomes directement dans les diatomées, en contournant l’étape bactérienne. Fait remarquable, des épiosomes allant jusqu’à 55,6 kilobases ont été délivrés et récupérés intacts. Les mêmes stratégies ont également fonctionné dans une seconde espèce, Thalassiosira pseudonana, qui possède une paroi plus fortement minéralisée, suggérant qu’il s’agit d’une boîte à outils d’application générale plutôt que d’une astuce propre à une seule espèce.
Laisser la cellule fabriquer ses propres cercles génétiques
En étudiant le comportement de l’ADN électroporé à l’intérieur des cellules, l’équipe a découvert un talent surprenant : les diatomées peuvent assembler elles‑mêmes des fragments d’ADN. Des segments linéaires d’épiosomes pénétraient dans la cellule et étaient réparés en cercles soit par des jonctions « non homologues » imparfaites, soit par une réparation plus précise guidée par recouvrement dite « par homologie ». Les auteurs ont baptisé ce processus « assemblage in vivo chez la diatomée », ou DIVA. En concevant des fragments chevauchants, ils ont poussé les cellules à assembler deux, trois ou quatre morceaux en épiosomes complets avec des taux de réussite élevés, incorporant parfois de petites cassettes synthétiques ajoutant des marqueurs fluorescents ou de nouvelles fonctions. Cette capacité transforme le noyau de la diatomée en un atelier miniature d’ADN, pouvant remplacer des étapes d’assemblage laborieuses habituellement réalisées dans la levure ou E. coli.
Éditer les génomes uniquement avec des complexes protéiques
Au‑delà de l’ajout d’épiosomes, les chercheurs ont montré qu’ils pouvaient livrer des complexes protéine‑ARN CRISPR–Cas9 prêts à l’emploi directement dans les cellules de diatomées en utilisant leur méthode d’électroporation optimisée. En ciblant un gène appelé PtAPT, qui contrôle la sensibilité à un analogue toxique de l’adénine, ils ont généré des milliers de mutants résistants sans introduire d’ADN supplémentaire dans le génome. Beaucoup de ces mutants présentaient de petites insertions ou délétions au site ciblé ; certains avaient même capturé des fragments d’ADN « transporteur » ajoutés pour amortir le choc électrique. L’équipe a ensuite co‑livré des complexes CRISPR et des épiosomes en une seule étape, constatant qu’environ une colonie sur dix portait à la fois une modification génomique et un épiosome sélectionnable — un moyen efficace de repérer des changements génétiques autrement invisibles. 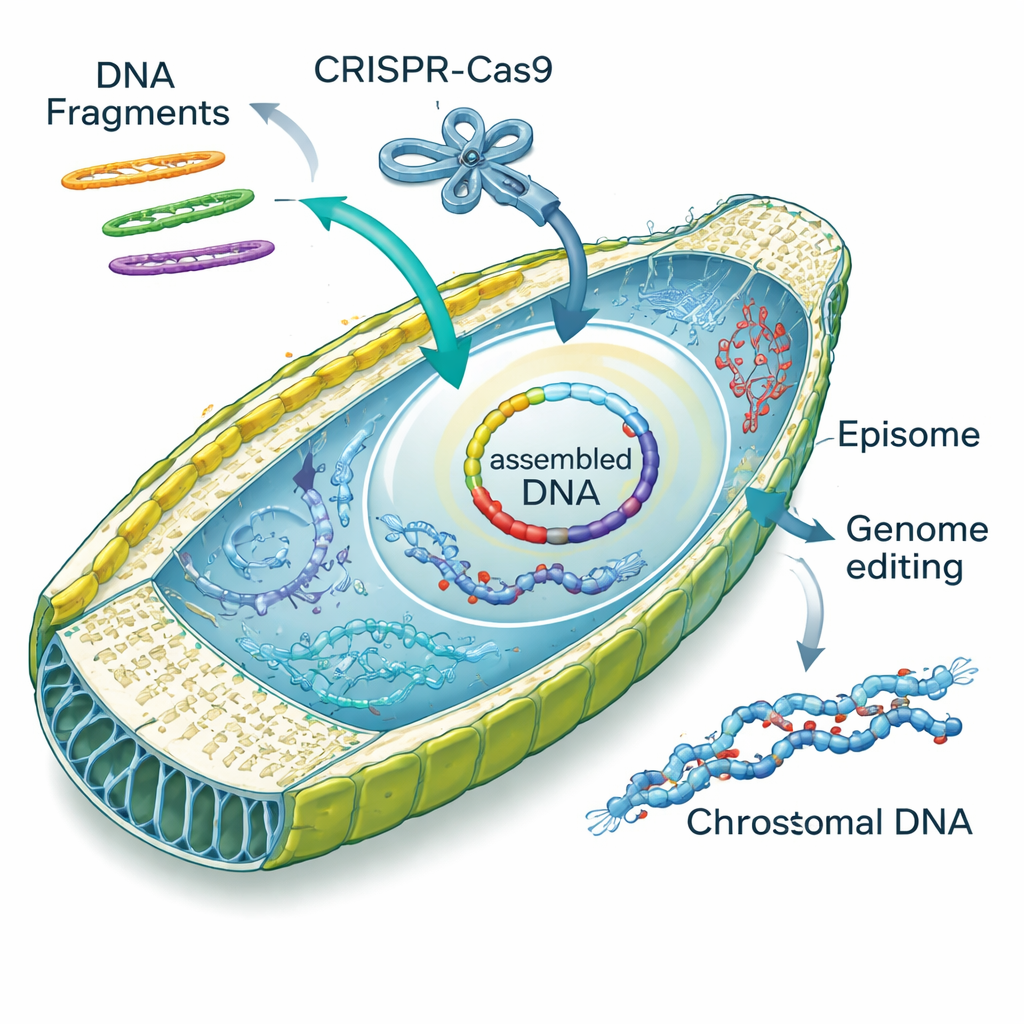
Vers des diatomées conçues pour un avenir durable
Pour les non‑spécialistes, le message clé est que les diatomées se rapprochent beaucoup de l’état d’organismes pratiques et programmables. En brisant ou en assouplissant délicatement la paroi cellulaire, les auteurs ont transformé un processus capricieux et peu productif en une chaîne robuste qui utilise de petites quantités d’ADN, fonctionne avec de grandes constructions génétiques et permet même à la cellule d’assembler et d’éditer son propre ADN. Ces avancées raccourcissent la trajectoire entre une séquence conçue sur ordinateur et une souche vivante testée. À long terme, de tels outils pourraient accélérer les efforts visant à construire des diatomées dotées de chromosomes entièrement synthétiques et à exploiter ces microbes océaniques pour des carburants plus propres, une chimie respectueuse du climat et de nouvelles découvertes biologiques.
Citation: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Mots-clés: biotechnologie des diatomées, transformation génétique, édition du génome CRISPR, biologie synthétique, ingénierie des microalgues