Clear Sky Science · fr
Structures de la télomérase humaine liée à des nucléotides à plusieurs étapes de son cycle d’ajout de répétitions d’ADN télomérique
Pourquoi les extrémités de nos chromosomes comptent
À chaque division cellulaire, les capuchons protecteurs aux extrémités de nos chromosomes — appelés télomères — raccourcissent un peu. S’ils deviennent trop courts, les cellules cessent de se diviser ou fonctionnent mal, contribuant au vieillissement et aux maladies. Une machinerie moléculaire appelée télomérase peut reconstruire ces capuchons et est anormalement active dans la plupart des cancers. Cette étude révèle, avec un niveau de détail sans précédent, comment la télomérase humaine saisit et allonge les télomères étape par étape, fournissant des indices sur la manière dont nous pourrions un jour ajuster cette enzyme dans les troubles liés à l’âge et le cancer.
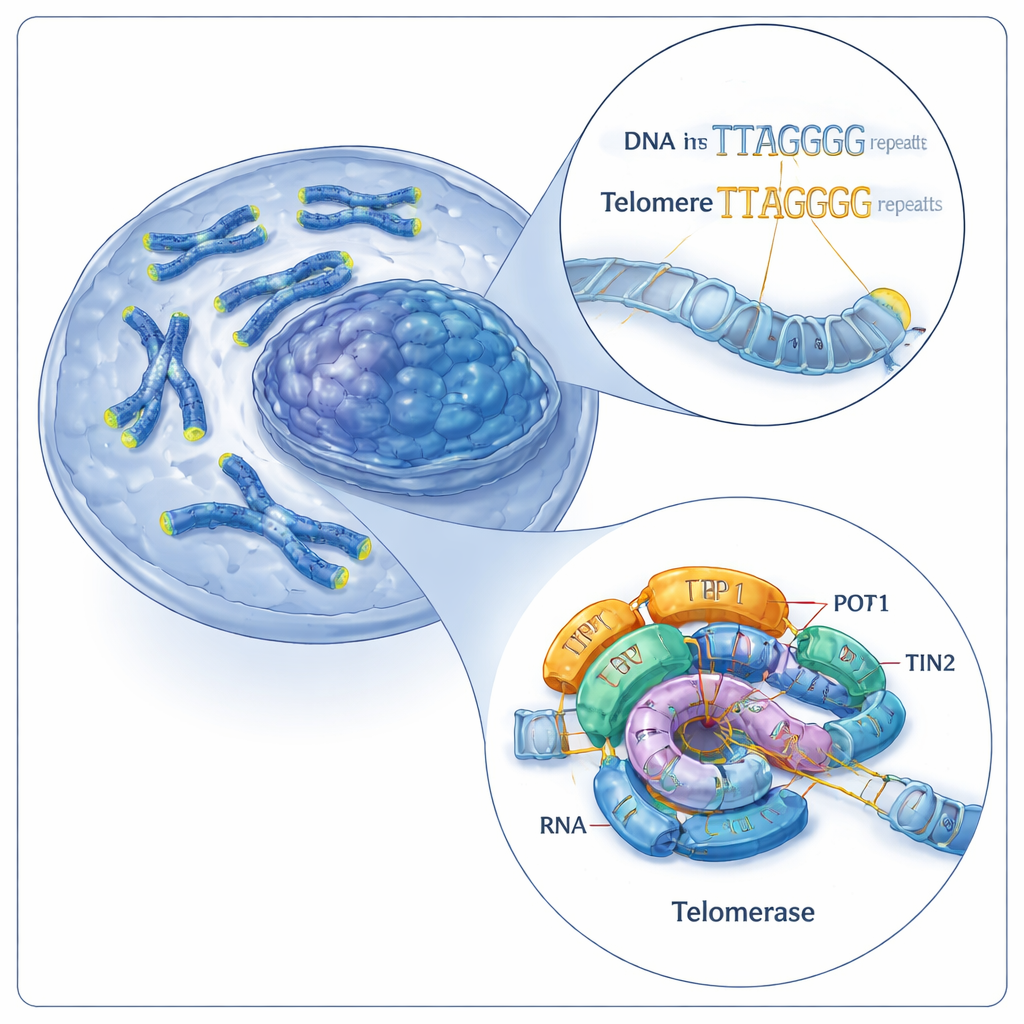
L’équipe de réparation des capuchons chromosomiques
Les télomères sont constitués de courtes séquences d’ADN répétées (chez l’humain, un motif de six lettres : TTAGGG). La télomérase allonge les télomères en ajoutant d’autres répétitions à l’extrémité des chromosomes. Elle le fait à l’aide de deux éléments principaux : une protéine appelée télomérase reverse transcriptase (TERT) et une molécule d’ARN intégrée (hTR) qui sert de matrice. Ensemble, ces composants forment un cœur catalytique, assisté par des protéines accessoires connues sous le nom de shelterin, dont un trio appelé TPP1–POT1–TIN2. Des travaux antérieurs n’avaient visualisé la télomérase humaine que dans un seul état de fonctionnement, laissant une question majeure en suspens : comment cette machine ajoute-t-elle de nouvelles répétitions sans se détacher de l’ADN ?
Congeler la télomérase en action
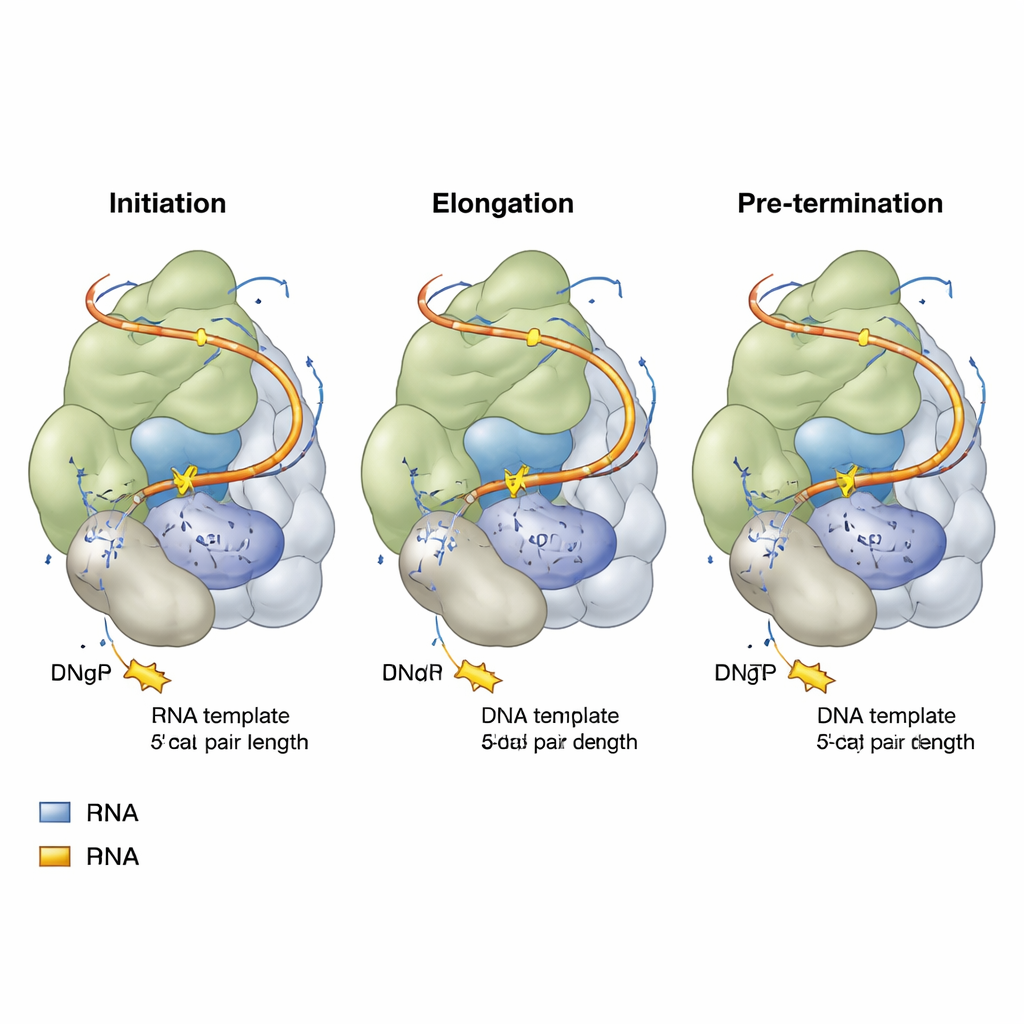
Les chercheurs ont reconstruit la télomérase humaine dans des cellules humaines puis l’ont assemblée avec des fragments d’ADN télomérique conçus et des analogues de nucléotides non réactifs — des molécules qui ressemblent aux lettres de l’ADN mais ne peuvent pas être incorporées complètement. À l’aide de la cryo‑microscopie électronique à haute résolution, ils ont capturé des instantanés de la télomérase à trois étapes clés de son cycle d’ajout de répétitions : le départ (initiation), le milieu de la copie (élongation) et juste avant la fin d’une répétition (pré‑termination). Chaque instantané montrait le cœur catalytique de la télomérase entourant un court hybride ADN‑ARN, avec un nucléotide entrant en position dans le site actif, prêt à être ajouté à la chaîne d’ADN en croissance.
Une petite fermeture éclair qui contrôle un grand processus
Dans les trois états, un thème surprenant est apparu : l’hybride ADN‑ARN à l’intérieur de la télomérase reste essentiellement de la même longueur — seulement quatre paires de bases, temporairement étendues à cinq quand un nouveau nucléotide arrive. Un acide aminé spécifique de TERT, surnommé une « tête de fermeture éclair », marque systématiquement la fin de cet hybride court et empêche son allongement. À mesure que de nouvelles lettres d’ADN sont ajoutées, une paire de bases à l’extrémité opposée fond, de sorte que l’hybride ne dépasse jamais cette fenêtre étroite de quatre à cinq paires. Ce design compact facilite probablement la séparation et le repositionnement des brins, permettant à l’enzyme d’avancer et de commencer la répétition suivante sans lâcher complètement l’ADN. De subtiles différences dans les lettres d’ADN et d’ARN qui occupent cet hybride expliquent pourquoi certaines séquences d’extrémité télomérique se lient plus fortement à la télomérase que d’autres.
Linkers d’ARN flexibles et éléments mobiles
La matrice ARN à l’intérieur de la télomérase ne flotte pas librement ; elle est attachée par des segments flexibles de part et d’autre, appelés linkers de matrice 5′ et 3′. Lorsque la télomérase progresse de l’initiation à la pré‑termination, le linker en amont (5′) est tendu comme un élastique, atteignant finalement un état complètement étiré qui aide à signaler la fin d’une répétition. Pendant ce temps, le linker en aval (3′) bombe vers l’extérieur et se rapproche d’une autre structure ARN (la tige‑boucle P6.1) et de régions protéiques voisines. Si ces linkers deviennent trop courts ou trop longs, ou si P6.1 est altérée, la capacité de la télomérase à ajouter répétition après répétition chute fortement. De manière importante, certaines régions protéiques — le domaine TEN et un insert spécifique à la télomérase appelé coin TRAP — jouent le rôle de guides réglables, contactant à la fois l’ADN et ces linkers ARN. Des mutations qui réduisent le volume du coin TRAP peuvent en fait rendre l’enzyme plus processive, ce qui suggère que ce coin agit normalement comme une barrière contrôlée qui cadence le mouvement de la matrice.
Nouvelles perspectives sur une cible thérapeutique
En combinant des instantanés structuraux avec des tests fonctionnels de mutations ciblées, l’étude propose un modèle mécanique détaillé expliquant comment la télomérase humaine allonge de manière répétée les télomères. L’enzyme maintient un hybride ADN‑ARN très court, utilise un résidu en forme de fermeture éclair pour imposer cette longueur, et s’appuie sur des linkers ARN flexibles et des éléments protéiques mobiles pour avancer la matrice et garder l’ADN ancré pendant de multiples cycles de copie. Pour les non‑spécialistes, le message clé est que la télomérase ne fonctionne pas comme une machine de copie statique mais comme un dispositif finement ajusté, à ressorts, dont la géométrie et les éléments mobiles déterminent combien et à quelle efficacité elle peut maintenir les télomères. Comprendre cette chorégraphie ouvre la voie à des médicaments susceptibles soit d’atténuer la télomérase dans les cancers, soit de stabiliser sa fonction dans les maladies du vieillissement prématuré.
Citation: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Mots-clés: télomérase, télomères, cryo-EM, stabilité du génome, biologie du cancer