Clear Sky Science · fr
La méthylation de l’ADN et les lncRNA contrôlent la réplication asynchrone de l’ADN dans des domaines géniques imprintés spécifiques
Pourquoi le calendrier de copie de l’ADN cellulaire compte
À chaque division cellulaire, il faut copier l’intégralité de l’ADN, mais toutes les régions ne sont pas dupliquées au même moment. Certaines portions sont copiées tôt, d’autres plus tard, suivant un « emploi du temps » précis du génome. Cet article examine pourquoi, dans quelques grappes de gènes particulières qui conservent la trace parentale, les copies maternelles et paternelles sont répliquées à des moments différents. Comprendre ce timing inhabituel éclaire la façon dont des marques chimiques sur l’ADN et des ARN longs non codants (lncRNA) organisent localement le génome et peuvent influencer le développement et les maladies.
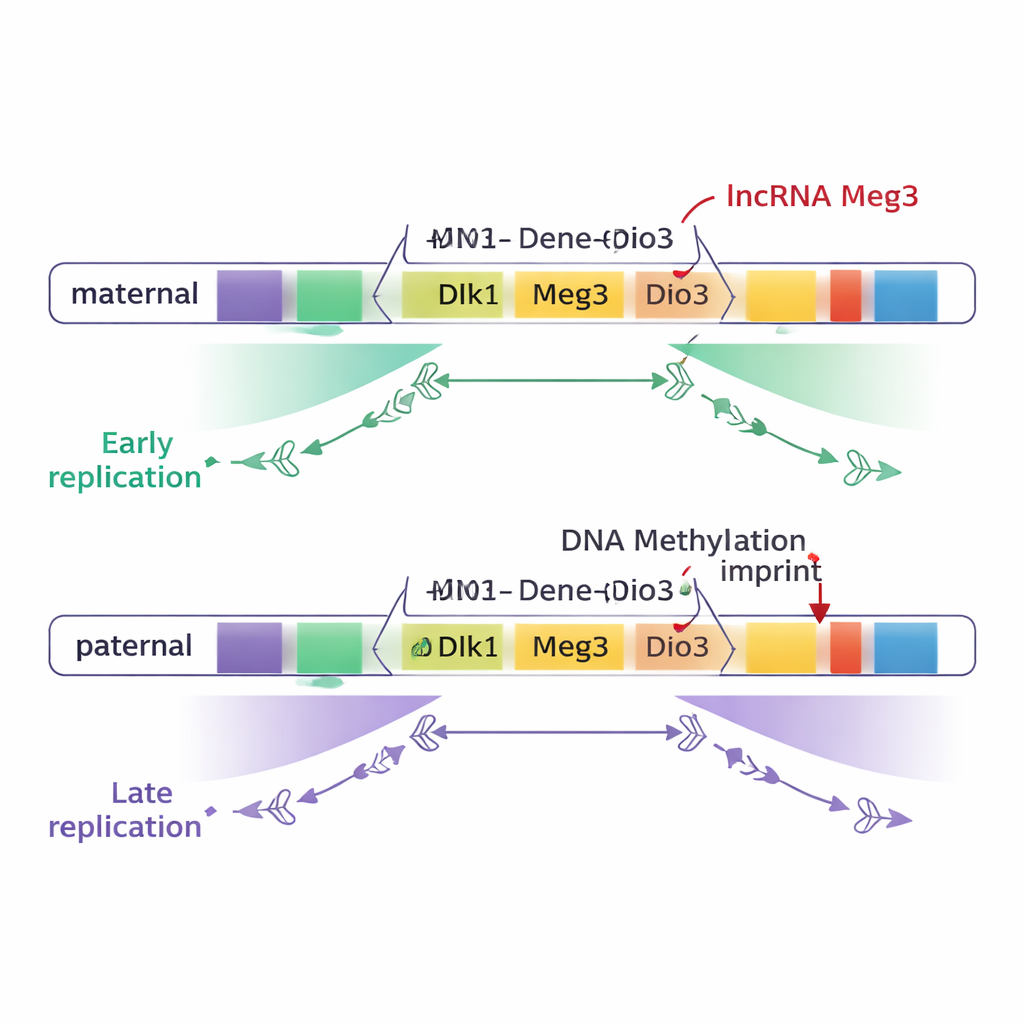
Souvenirs parentaux inscrits sur l’ADN
Chez les mammifères, un petit nombre de domaines géniques « imprintés » se comportent différemment selon qu’ils sont hérités de la mère ou du père. Cet effet lié à l’origine parentale est contrôlé par la méthylation de l’ADN — de minuscules marques chimiques ajoutées à des régions spécifiques appelées régions différentièlement méthylées (DMR) — et par des modifications de la compaction chromosomique. Les auteurs ont étudié des cellules souches embryonnaires de souris, qui ressemblent à des cellules embryonnaires très précoces. Ils ont comparé des cellules ne contenant que des génomes maternels, que des génomes paternels, et des hybrides normaux portant un génome de chaque parent. En suivant le moment où des fragments d’ADN étaient copiés au cours du cycle cellulaire, ils ont cartographié la chronologie de réplication à l’échelle du génome et se sont focalisés sur des régions imprintées connues.
Deux régions imprintées font exception
La majeure partie du génome, y compris la plupart des domaines imprintés, est copiée au même moment sur les chromosomes maternels et paternels. Cependant, deux grands domaines imprintés se détachent : le domaine Dlk1–Dio3 sur le chromosome 12 et la région Snrpn sur le chromosome 7. Dans ces zones, une vaste portion d’ADN — environ trois quarts de million de paires de bases pour Dlk1–Dio3 — était copiée tôt sur un chromosome parental et tard sur l’autre. Fait essentiel, cette différence dépendait de l’origine parentale et non du fond génétique : la copie maternelle de gènes clés tels que Dlk1 et du gène lncRNA Meg3 répliquait systématiquement tôt, tandis que les copies paternelles le faisaient plus tard.
La méthylation de l’ADN règle l’interrupteur temporel
Pour tester la cause de cette différence de timing, les chercheurs ont modifié des cellules souches pour effacer ou imposer le schéma normal de méthylation aux DMR des deux chromosomes parentaux. Lorsque les deux copies parentales des DMR du domaine Dlk1–Dio3 étaient méthylées, toute la région se répliquait tard sur les deux chromosomes. Quand la méthylation était largement supprimée sur les deux copies, la même région se répliquait tôt sur les deux. Des expériences similaires sur Snrpn ont aussi éliminé les différences de timing. Ces résultats montrent que la méthylation spécifique à un parent est essentielle pour créer le contraste de réplication tôt-vers-tard entre chromosomes maternel et paternel, du moins dans ces deux domaines.
Un ARN long affine la réplication précoce
La méthylation de l’ADN n’explique toutefois pas tout. Le domaine Dlk1–Dio3 produit également un long ARN non codant appelé Meg3, qui fait partie d’un grand « polycistron » d’ARN. Sur le chromosome maternel, des DMR non méthylés permettent l’expression de Meg3 ; sur le chromosome paternel, la méthylation la réprime. En réalisant des délétions précises qui éteignaient Meg3 tout en laissant intacte la méthylation de l’ADN, les auteurs ont montré que la perte de l’ARN Meg3 provoquait le déplacement de portions spécifiques du domaine maternel d’une réplication précoce vers une réplication plus tardive. Autrement dit, l’ARN Meg3 favorise la copie précoce de tronçons voisins du chromosome maternel, ajoutant une seconde couche de contrôle en plus de la méthylation de l’ADN.
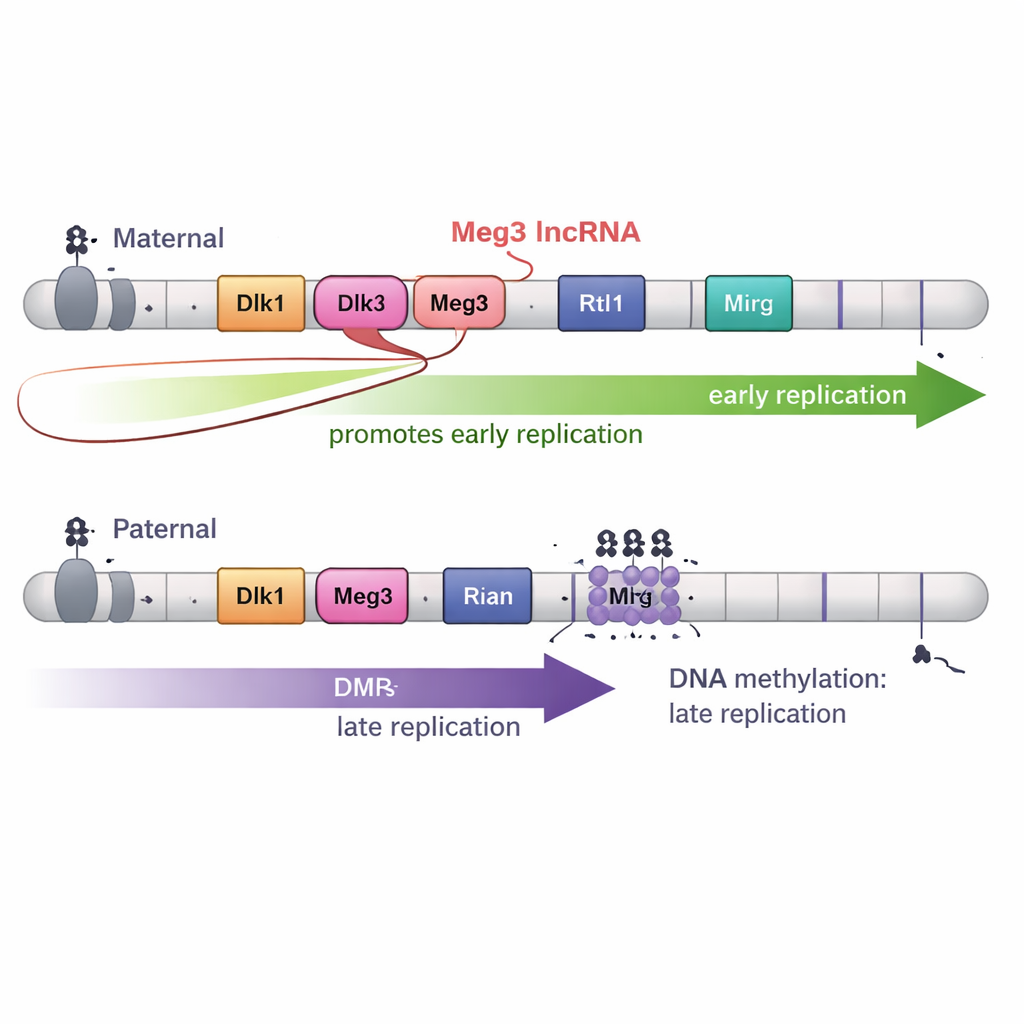
La 3D et le développement apportent d’autres nuances
Étant donné que le repliement du génome est souvent lié à la chronologie de réplication, l’équipe a aussi cartographié l’architecture chromosomique 3D avec une grande résolution. De façon surprenante, dans le domaine Dlk1–Dio3, les frontières des domaines 3D ne correspondaient pas aux limites des régions répliquées tôt et tard. Même lorsque les schémas de méthylation étaient modifiés et que le timing de réplication changeait, les unités de repliement de base — les domaines d’association topologique — évoluaient différemment. Enfin, quand les cellules souches ont été différenciées en progéniteurs neuronaux, les différences marquées de timing entre copies maternelles et paternelles ont en grande partie disparu, bien que les marques d’imprinting et de nombreux aspects de la structure 3D aient été préservés. Cela suggère que des signaux liés au développement peuvent supplanter le schéma spécial tôt-vers-tard observé dans les cellules souches.
Ce que cela signifie en termes simples
Cette étude montre que, dans quelques voisinages géniques particuliers qui conservent la mémoire parentale, le calendrier de copie de l’ADN est contrôlé par une combinaison de marques chimiques sur l’ADN et d’ARN longs non codants. La méthylation de l’ADN aux régions de contrôle imprintées fixe un timing fondamental tôt-ou-tard pour chaque chromosome parental, et le lncRNA Meg3 incite en plus l’ADN maternel proche à être copié plus tôt. Ces effets agissent en grande partie indépendamment du repliement chromosomique en 3D. Au cours du développement, à mesure que les cellules se spécialisent, ce timing inhabituel s’estompe, ce qui indique qu’il s’agit d’une caractéristique de l’état pluripotent des cellules souches. Dans l’ensemble, le travail explique comment les « souvenirs » épigénétiques parentaux et les ARN non codants peuvent localement outrepasser l’emploi du temps habituel de réplication du génome.
Citation: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Mots-clés: impression génomique, méthylation de l’ADN, chronologie de réplication, ARN long non codant, cellules souches embryonnaires