Clear Sky Science · fr
Activation microbienne du GLP-2R atténue l'inflammation gastro-intestinale
Pourquoi une protéine compatible avec l'intestin compte
Alors que le monde cherche des moyens durables de nourrir une population croissante, les scientifiques regardent au-delà des fermes et des champs vers de grands réservoirs d'acier où l'on cultive des microbes pour l'alimentation. Cette étude examine si une de ces protéines dérivées de microbes peut faire plus que simplement nous nourrir. Les chercheurs se sont demandé : une protéine issue de bactéries inoffensives peut-elle à la fois satisfaire les besoins alimentaires et protéger activement l'intestin contre l'inflammation, un problème central dans des affections comme la maladie inflammatoire de l'intestin et les lésions intestinales induites par la chimiothérapie ?
Un nouveau type de protéine issue des microbes
La protéine au centre de ce travail provient d'une bactérie du sol appelée Methylococcus capsulatus Bath (McB). Plutôt que d'être consommée sous forme de bactéries vivantes, McB est transformée en lysat microbien — essentiellement un produit en poudre de cellules bactériennes brisées — commercialisé sous le nom FeedKind®. Des souris ont reçu des régimes dans lesquels ce lysat apportait la majeure partie des protéines, soit dans un régime simple, soit dans un régime « complexe » plus proche de l'alimentation humaine. L'équipe a ensuite suivi comment ce régime modifiait la composition des microbes intestinaux, les cellules immunitaires qui patrouillent l'intestin, et la résistance de l'intestin à différents types de lésions.
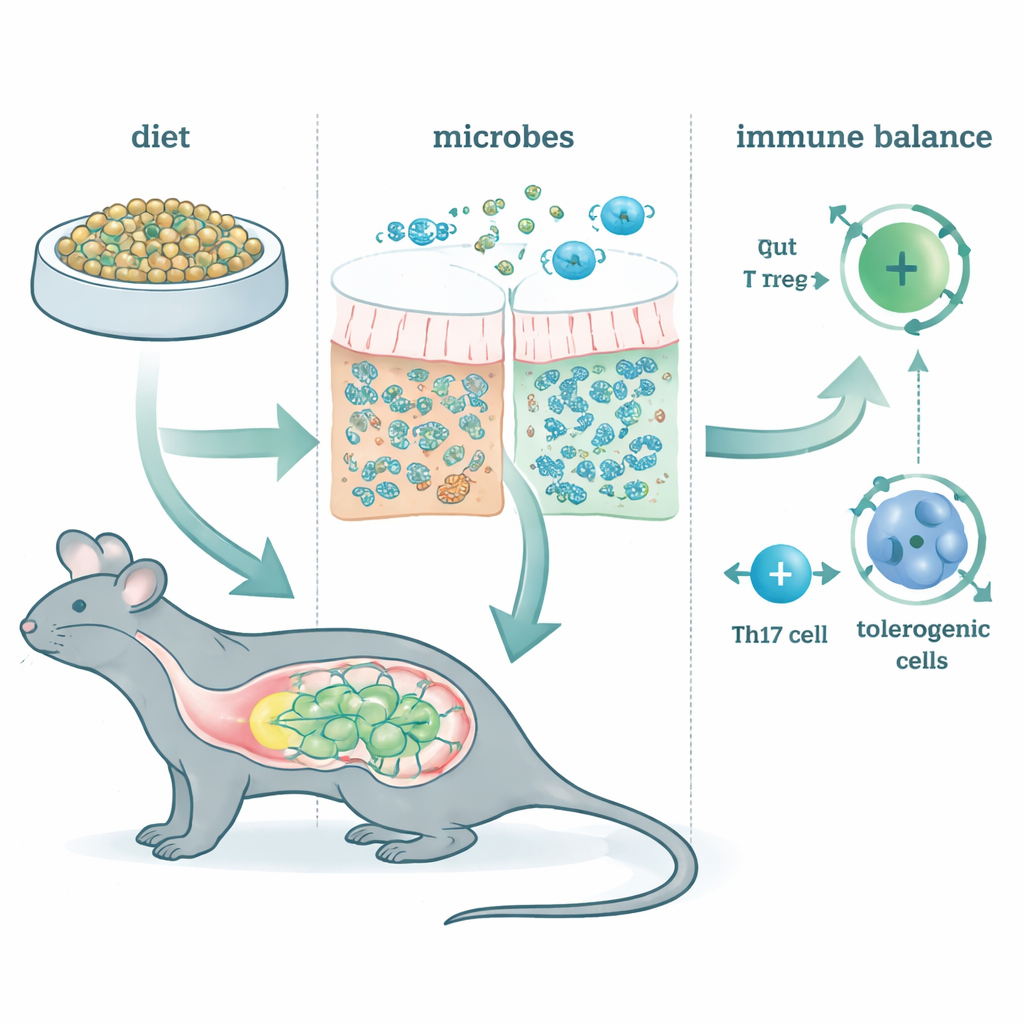
Restructurer le voisinage microbien
L'alimentation au McB a rapidement et durablement modifié le microbiote intestinal, quel que soit le régime de fond des animaux. Seule une fraction minime de McB elle-même est apparue dans les fèces, ce qui signifie que la matière a été presque entièrement consommée dans l'intestin. À la place, une poignée d'espèces bactériennes de familles telles que Lachnospiraceae et Bacteroidaceae ont prospéré. Des analyses génétiques ont montré que ces communautés étaient enrichies en voies de fermentation produisant des acides gras à chaîne courte — de petites molécules déjà connues pour nourrir les cellules intestinales et influencer l'immunité. Autrement dit, McB a agi moins comme une protéine conventionnelle et davantage comme un carburant ciblé qui redéfinit les fonctions des microbes résidents.
Apprendre au système immunitaire à tolérer
Les auteurs ont ensuite examiné les types clés de cellules T qui contribuent à décider si l'intestin réagit calmement ou agressivement à ce qui le traverse. Un groupe, les cellules T régulatrices induites en périphérie (pTregs), aide à prévenir la réaction excessive envers les aliments et les microbes amicaux. Un autre groupe, les cellules Th17, peut soit provoquer une inflammation dommageable, soit aider à maintenir une barrière saine, selon leur « humeur ». L'alimentation au McB a fortement augmenté les pTregs sur l'ensemble de l'intestin, même lorsque la plupart des microbes intestinaux étaient éliminés par des antibiotiques. En revanche, les effets de McB sur les cellules Th17 dépendaient de la présence et du bon fonctionnement des bactéries intestinales. Chez des souris microbiennes intactes, McB a poussé les Th17 vers un état plus apaisant, producteur d'IL‑10 et moins inflammatoire. Lorsque la fermentation était bloquée, ce basculement tolérogène disparaissait, soulignant que McB agit en partie en réorientant les conversations entre microbes et système immunitaire.
Protéger l'intestin lors de lésions
Pour vérifier si ces changements se traduisaient par une protection réelle, les chercheurs ont soumis des souris à deux agressions intestinales sévères. La première était un médicament de chimiothérapie, le 5‑fluorouracile, qui provoque des dommages étendus et le raccourcissement des villosités en doigt qui absorbent les nutriments. L'autre était une substance chimique (DSS) qui déclenche une colite, un modèle d'inflammation du gros intestin. Les souris sous régime McB ont perdu moins de poids, ont conservé des villosités et une longueur du côlon plus importantes, ont présenté moins de lésions hémorragiques et ont eu des scores de dégâts microscopiques plus faibles dans les deux modèles. Ces bénéfices persistaient même lorsque les cellules T CD4 étaient supprimées expérimentalement, ce qui suggère que les actions protectrices de McB sur l'intestin ne sont pas uniquement dues aux cellules immunitaires adaptatives mais impliquent aussi des effets directs sur la muqueuse intestinale.
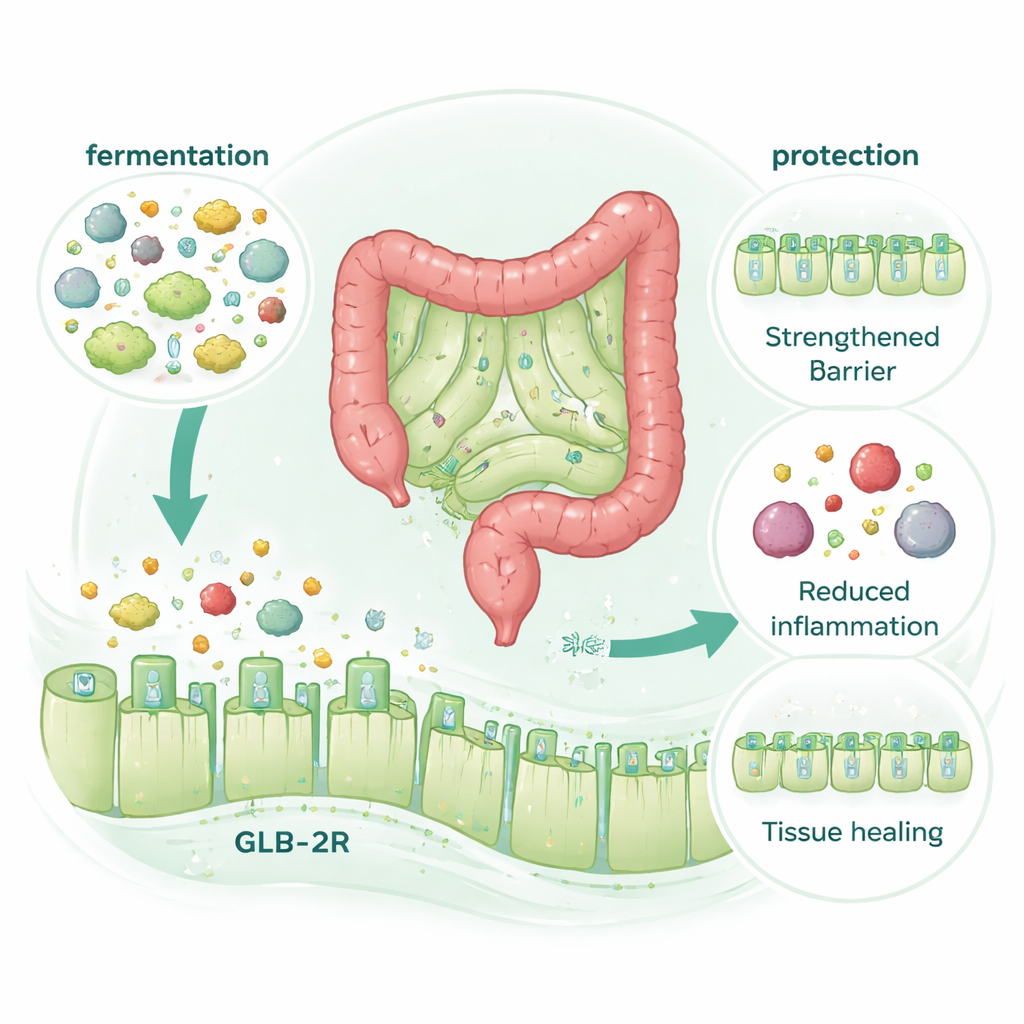
Un récepteur hormonal, mais pas d'hormone en plus
Une découverte surprenante a été que l'effet protecteur de McB nécessitait absolument le récepteur intestinal d'une hormone favorisant la réparation appelée GLP‑2 (le récepteur GLP‑2, ou GLP‑2R), mais pas le récepteur apparenté GLP‑1. Lorsque les souris étaient dépourvues de GLP‑2R, McB ne les protégeait plus des dommages de la chimiothérapie ou de la colite. Pourtant McB lui‑même n'augmentait pas les niveaux de GLP‑2 dans le sang, même lorsque la digestion et la dégradation hormonale étaient soigneusement contrôlées. À la place, les bénéfices disparaissaient lorsque la fermentation microbienne dans le côlon était bloquée chimiquement, alors même que la composition globale du microbiote changeait très peu. Cela indique un mécanisme dans lequel la dégradation microbienne de McB génère de petites molécules qui se comportent comme des « mimétiques » du GLP‑2, activant son récepteur pour renforcer la barrière et favoriser la réparation sans libération hormonale supplémentaire.
Ce que cela pourrait signifier pour les aliments de demain
Pour un lecteur non spécialiste, le message principal est que certaines sources futures de protéines pourraient être conçues non seulement pour réduire l'impact climatique, mais aussi pour soutenir activement la santé intestinale. Chez la souris, un lysat commercialisable de McB a à la fois réorienté l'immunité vers la tolérance et aidé l'intestin à résister à des dommages sévères, par deux voies partiellement indépendantes : une augmentation directe des cellules T régulatrices et une activation du récepteur GLP‑2, dépendante de la fermentation, qui favorise la réparation tissulaire. Bien que des études chez l'humain soient encore nécessaires, ce travail suggère que des protéines d'origine microbienne pourraient constituer une nouvelle classe d'aliments "intelligents" — capables de nous nourrir, de collaborer avec nos propres microbes et de renforcer discrètement les défenses naturelles de l'intestin contre l'inflammation.
Citation: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Mots-clés: inflammation intestinale, protéine microbienne, microbiome, récepteur GLP-2, cellules T régulatrices