Clear Sky Science · fr
Le FUNDC1 endothélial régule le reprogrammation métabolique et la transition obésité‑diabète via l’axe SIRT3/GATA2/endothéline‑1
Pourquoi les cellules des vaisseaux sanguins comptent pour l’obésité et le diabète
L’obésité et le diabète de type 2 sont souvent imputés au tissu adipeux, au foie ou au pancréas. Mais cette étude révèle un acteur surprenant : la fine couche de cellules qui tapisse nos vaisseaux sanguins, appelées cellules endothéliales. Les chercheurs montrent qu’une petite protéine mitochondriale dans ces cellules, nommée FUNDC1, peut contribuer à faire basculer l’organisme d’une simple prise de poids vers un diabète avéré en modifiant la façon dont les vaisseaux communiquent avec les organes métaboliques.
Stress sur la « peau » intérieure du corps
Les cellules endothéliales forment un vaste réseau délicat qui contrôle le flux sanguin, l’apport de nutriments et les signaux envoyés aux tissus voisins. En condition saine, elles équilibrent des facteurs de relaxation comme l’oxyde nitrique avec des facteurs de contraction tels que l’endothéline‑1 (ET‑1). Dans l’obésité et le diabète précoce, cet équilibre bascule en faveur de l’ET‑1, qui non seulement rétrécit les vaisseaux mais perturbe aussi la manière dont les cellules adipeuses, musculaires et hépatiques gèrent le sucre et les lipides. Les auteurs montrent d’abord chez la souris que la dysfonction vasculaire apparaît après seulement deux mois d’alimentation riche en graisses, avant le développement net d’une insulinorésistance, ce qui suggère que l’endothélium lésé peut contribuer à déclencher la maladie métabolique plutôt que d’en être uniquement une conséquence.
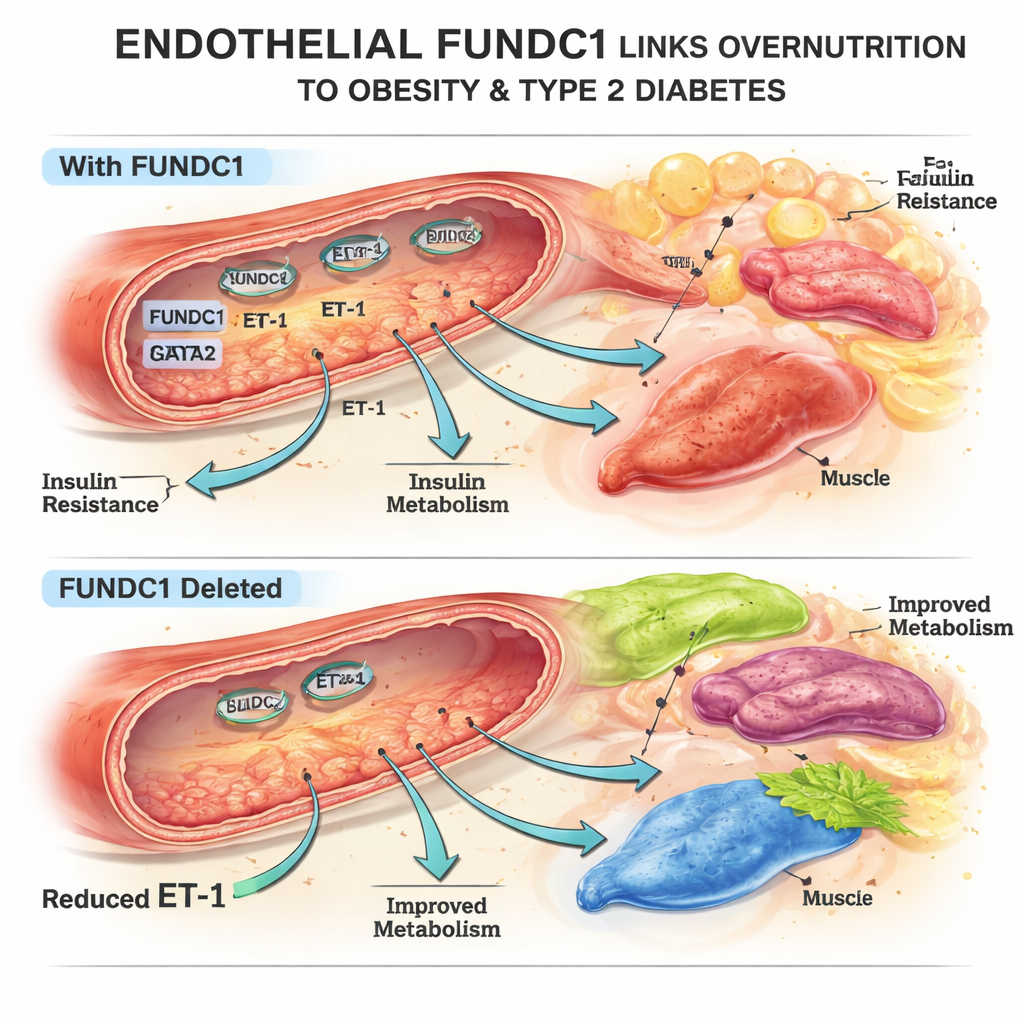
Un interrupteur mitochondrial qui façonne la masse grasse
L’équipe s’est intéressée à FUNDC1, une protéine située à la surface des mitochondries, les centrales énergétiques de la cellule. Dans des cellules endothéliales de souris et d’humains exposées à un excès de lipides, les niveaux de FUNDC1 évoluent avec le temps : ils diminuent d’abord, puis augmentent fortement en cas de surnutrition prolongée. En utilisant des souris génétiquement modifiées dépourvues de FUNDC1 uniquement dans les cellules endothéliales, les chercheurs ont découvert que ces animaux étaient partiellement protégés contre la prise de poids induite par un régime riche en graisses : ils avaient moins de masse grasse, des adipocytes plus petits et une meilleure régulation glycémique. Leurs tissus adipeux, hépatiques et de graisse brune répondaient mieux à l’insuline, alors même que les niveaux d’insuline n’étaient pas augmentés. Ces changements ne s’expliquaient pas par une différence de prise alimentaire ou d’activité, mais plutôt par l’influence du système vasculaire sur le métabolisme.
Un messager chimique qui favorise l’insulinorésistance
Pour comprendre comment FUNDC1 endothélial affecte des organes distants, les auteurs ont dépisté plusieurs substances sécrétées par les cellules endothéliales. Une d’elles ressort : l’ET‑1. Lorsque FUNDC1 était supprimé dans les cellules endothéliales, la production d’ET‑1 dans les vaisseaux et sa concentration sanguine diminuaient nettement, aussi bien en conditions normales qu’en régime riche en graisses. Des expériences sur des adipocytes, des hépatocytes et des cellules musculaires en culture ont montré que l’ET‑1 favorisait la prolifération des préadipocytes, modifiait le stockage et la mobilisation des lipides, et aggravait l’accumulation lipidique dans le foie et le muscle exposés à un excès de graisses — un tableau connu pour promouvoir l’insulinorésistance. Chez la souris, l’administration d’ET‑1 au début d’un régime riche en graisses annulait les bénéfices protecteurs de la suppression de FUNDC1 endothélial : poids corporel, masse grasse, contrôle glycémique et fonction vasculaire se détérioraient, ce qui souligne le rôle clé de l’ET‑1 comme lien entre l’endothélium et la maladie métabolique.
Un axe de signalisation interne : FUNDC1, SIRT3 et GATA2
L’étude cartographie ensuite une chaîne moléculaire détaillée au sein des cellules endothéliales. Sous stress lié à un régime riche en graisses, une forme longue de l’enzyme SIRT3 (SIRT3‑L), qui peut résider à la fois dans le noyau et les mitochondries, migre du noyau vers les mitochondries avec l’aide de FUNDC1 et d’une protéine chaperonne appelée HSC70. Une fois séquestrée dans les mitochondries, moins de SIRT3‑L est disponible dans le noyau pour déacétyler GATA2, un facteur de transcription qui stimule l’activité du gène codant l’ET‑1. GATA2 plus acétylé est plus stable et augmente la production d’ET‑1. Lorsque FUNDC1 manque, SIRT3‑L reste dans le noyau où il déacétyle GATA2, entraînant la dégradation de GATA2 et une moindre production d’ET‑1. Fait intrigant, SIRT3 favorise à son tour la dégradation de FUNDC1, créant une boucle de rétrocontrôle qui limite normalement la voie mais qui se dérègle en cas de surnutrition chronique.
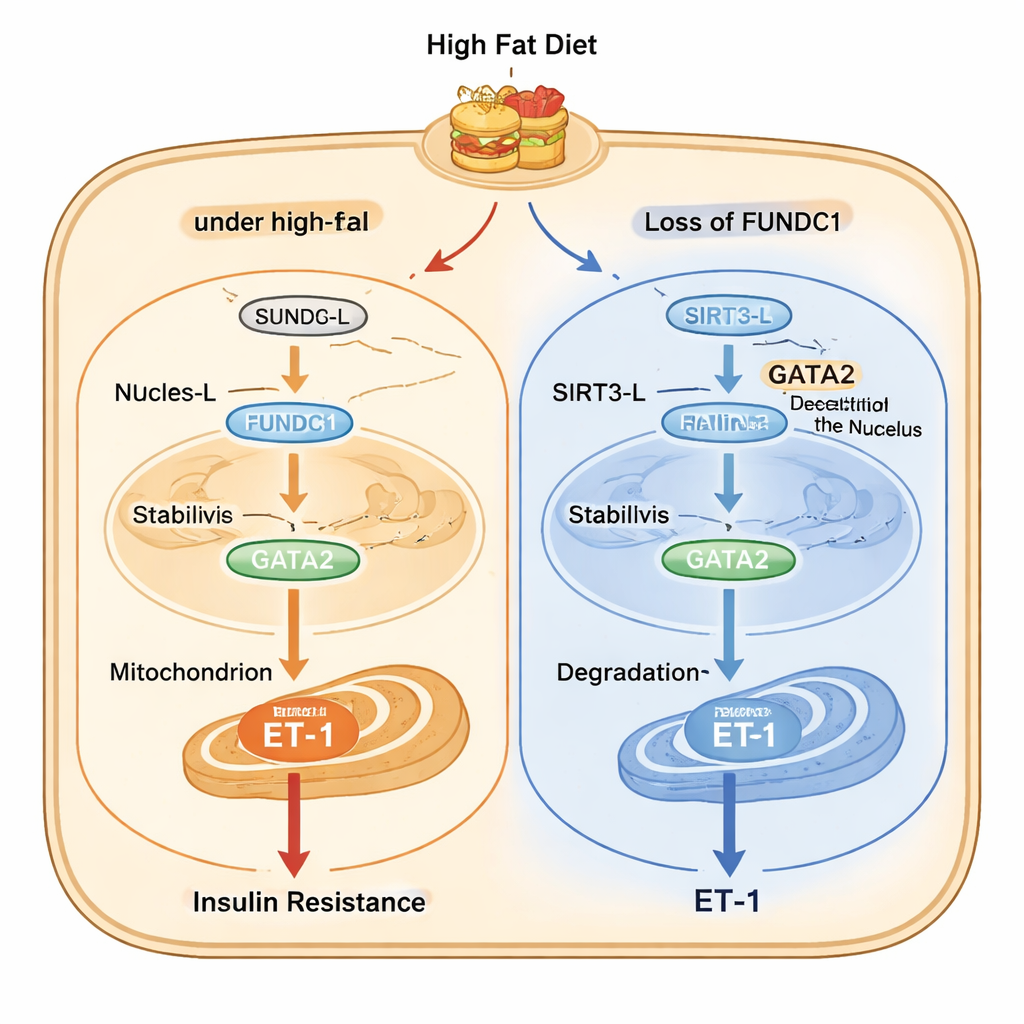
Des modèles murins à la maladie humaine
Pour vérifier si ce mécanisme a une importance chez l’homme, les chercheurs ont examiné le sang et de petites artères provenant de personnes obèses et diabétiques de type 2 ainsi que de volontaires sains. Les patients présentant les deux pathologies avaient des taux sanguins d’ET‑1 plus élevés et une expression accrue de FUNDC1, GATA2 et du gène ET‑1 dans leur endothélium vasculaire. La quantité d’ET‑1 circulant corrélait étroitement avec l’indice de masse corporelle et l’hémoglobine glyquée (HbA1c), et l’expression du gène ET‑1 dans les vaisseaux était fortement corrélée à FUNDC1 et GATA2. Ces schémas reflètent les observations chez la souris et soutiennent l’idée qu’un axe FUNDC1–SIRT3–GATA2–ET‑1 hyperactif sévit dans le tissu vasculaire humain soumis au stress métabolique.
Une nouvelle cible dans la lutte contre le diabète
Pour le grand public, le message central est que les dommages causés par la suralimentation peuvent d’abord apparaître dans les cellules qui tapissent nos vaisseaux sanguins. Là, une protéine mitochondriale, FUNDC1, contribue à détourner une enzyme régulatrice, SIRT3, hors du noyau, ce qui permet à un autre facteur, GATA2, d’augmenter la production d’ET‑1, un signal de type hormonal puissant qui favorise à la fois le durcissement des vaisseaux et l’insulinorésistance. Bloquer cette voie — en réduisant l’activité de FUNDC1 endothélial ou en atténuant l’ET‑1 — pourrait aider à prévenir la transition de l’obésité vers le diabète tout en protégeant le système vasculaire.
Citation: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
Mots-clés: cellules endothéliales, mitochondries, endothéline‑1, obésité, diabète de type 2