Clear Sky Science · fr
Les lipides éther influencent le destin des cellules cancéreuses en modulant l’absorption du fer
Comment une graisse méconnue pourrait révéler le point faible du cancer
Le cancer est souvent décrit comme une « maladie des gènes », mais cette étude montre que les graisses constituant la peau externe d’une cellule peuvent être tout aussi déterminantes. Les chercheurs dévoilent comment une classe particulière de lipides, appelés lipides éther, aide des cellules cancéreuses agressives à importer du fer depuis leur environnement — alimentant à la fois leur capacité à se propager et leur vulnérabilité à une forme récemment reconnue de mort cellulaire. Comprendre ce lien caché entre membranes cellulaires, fer et comportement tumoral pourrait ouvrir la voie à des thérapies ciblant sélectivement les cellules cancéreuses les plus agressives.
Une manière différente de penser les cellules cancéreuses
La plupart des recherches sur le cancer se concentrent sur les mutations de l’ADN et les protéines qu’elles codent. Ce travail déplace l’attention vers la membrane cellulaire — la fine enveloppe huileuse qui entoure chaque cellule. Dans cette enveloppe se trouvent de nombreux types de lipides, chacun avec des formes et des propriétés physiques distinctes. Les auteurs se concentrent sur les lipides éther, qui représentent environ un cinquième des phospholipides dans de nombreuses cellules de mammifères mais ont été relativement peu étudiés. Ils constatent que les cellules cancéreuses très métastatiques et de type souche chargent leurs membranes en lipides éther, conférant à ces membranes une faible tension et une forte fluidité. Ces traits physiques modifient à leur tour la manière dont les cellules importent le fer, un métal qui peut à la fois favoriser la croissance tumorale et déclencher un processus destructeur appelé ferroptose, une forme de mort cellulaire dépendante du fer.
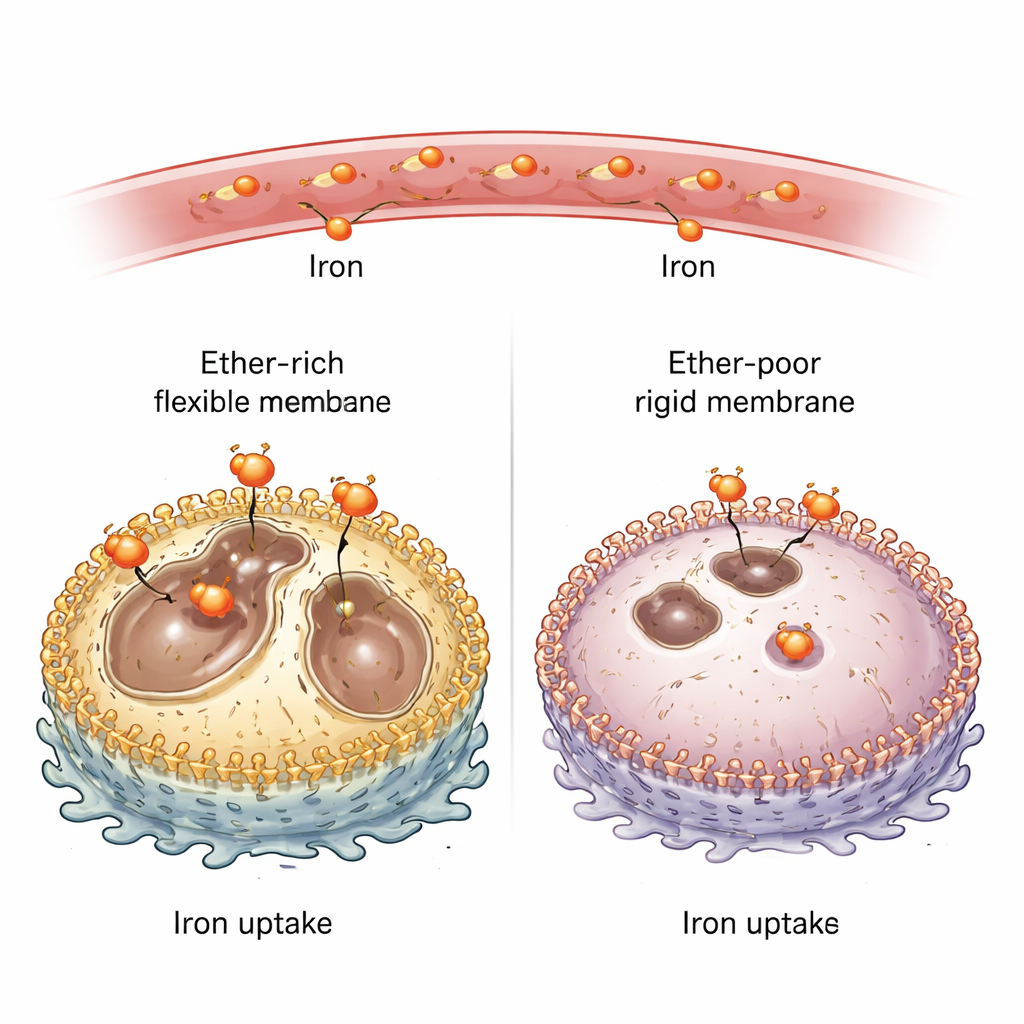
Relier les lipides membranaires à l’entrée du fer
Pour étudier les lipides éther, l’équipe a supprimé des enzymes clés nécessaires à leur synthèse dans plusieurs lignées cellulaires cancéreuses de souris et humaines. Sans ces enzymes, la proportion de lipides éther dans la membrane plasmique est tombée d’environ un quart de tous les lipides à seulement quelques pourcents. Fait surprenant, ces cellules pauvres en éther contenaient beaucoup moins de fer « redox‑actif » — la forme chimiquement réactive qui participe aux réactions d’oxydation — à la fois en culture et dans des tumeurs implantées chez la souris. Lorsque les scientifiques ont apporté du fer supplémentaire de l’extérieur, le niveau de fer des cellules a remonté et elles ont retrouvé leur sensibilité aux médicaments induisant la ferroptose. Cela montre que les lipides éther font plus que servir de combustible oxydable : ils contrôlent activement la quantité de fer qui pénètre dans la cellule.
Une porte spécialisée pour le fer : la voie CD44
Les chercheurs se sont ensuite demandé comment la composition membranaire modifie l’absorption du fer. Les cellules importent typiquement le fer via une protéine bien connue, le récepteur de la transferrine, mais les cellules cancéreuses agressives et de type souche utilisent aussi une autre voie : une protéine de surface nommée CD44 qui internalise le fer lié à une molécule de sucre appelée hyaluronane. En suivant des sondes fluorescentes, l’équipe a montré que l’élimination des lipides éther affectait à peine l’absorption médiée par le récepteur de la transferrine mais ralentissait fortement l’endocytose médiée par CD44 — une voie alternative, indépendante de la clathrine, d’entrée de matériel dans la cellule. La restauration des lipides éther, ou leur ajout sous forme de liposomes, a ravivé cette voie CD44. La perturbation de CD44 elle‑même ou la digestion de l’hyaluronane a diminué le fer cellulaire, confirmant que cette voie dépendante des éthers constitue une porte majeure d’entrée du fer dans ces cellules cancéreuses.
Comment des membranes plus souples modifient le comportement cellulaire
Pourquoi les lipides éther importent‑ils tant pour CD44 mais pas pour le récepteur classique du fer ? La réponse tient à la physique. À l’aide d’outils de précision qui tirent de petits filaments depuis la surface cellulaire, les auteurs ont montré que les membranes riches en éther ont une tension plus basse et sont plus faciles à déformer. Lorsqu’on a retiré les lipides éther, la tension membranaire a augmenté et les lipides se sont compactés, rendant la membrane plus rigide. Ces changements entravent fortement les formes d’endocytose qui dépendent de zones membranaires flexibles et de type radeau — précisément le type utilisé par CD44 — tout en laissant l’absorption basée sur la clathrine globalement intacte. Les lipides éther contribuent également à stabiliser les « radeaux lipidiques », de petits îlots ordonnés dans la membrane où CD44 se regroupe avant d’être entraînée vers l’intérieur. En bref, les lipides éther ajustent le paysage physique de la membrane pour favoriser l’entrée du fer via CD44.
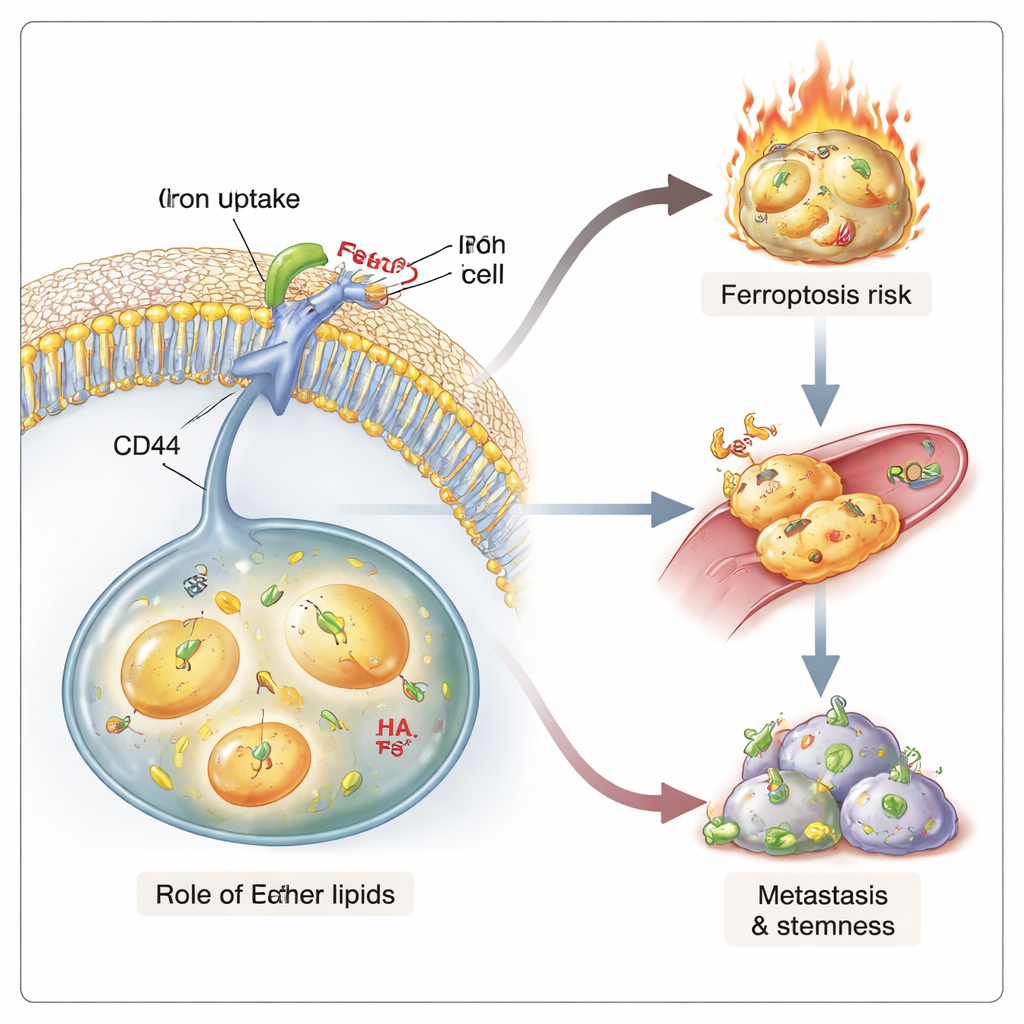
Alimenter à la fois la dissémination et l’autodestruction
Des niveaux élevés de fer et une faible tension membranaire sont liés à des traits qui rendent les cancers mortels : la capacité à engendrer de nouvelles tumeurs et à résister aux traitements. Dans des modèles tridimensionnels de micro‑vaisseaux, les cellules cancéreuses riches en éther se sont plus facilement extraites de structures ressemblant à des vaisseaux sanguins — une étape précoce de la métastase. Chez la souris, les cellules cancéreuses déficientes en éther ont formé moins de métastases, bien que leurs tumeurs primaires aient crû à des rythmes similaires. Ces cellules présentaient aussi une « capacité souche » réduite, mesurée par leur capacité diminuée à former des mammosphères en culture et à initier des tumeurs lors d’implants en dilution limite. Parallèlement, les cellules riches en éther, avec leur charge en fer plus élevée et leurs lipides plus oxydables, étaient plus sensibles à la ferroptose lorsqu’on les confrontait à des médicaments spécifiques ou à des signaux immunitaires. Ainsi, les lipides éther créent un état à double tranchant : ils soutiennent un comportement agressif et de type souche tout en rendant ces mêmes cellules particulièrement éliminables via des dommages lipidiques induits par le fer.
Pourquoi cela compte pour les traitements futurs du cancer
Pour les non‑spécialistes, le message clé est que toutes les cellules cancéreuses ne sont pas également dangereuses, et que leurs membranes externes contribuent à déterminer à la fois leur caractère menaçant et leur vulnérabilité. Les lipides éther remodèlent la surface cellulaire de sorte que le fer puisse entrer par une porte spécialisée, énergisant les cellules métastatiques et de type souche mais aussi leur fournissant les ingrédients de leur propre destruction. Des thérapies qui modifient la production de lipides éther, perturbent l’absorption du fer via CD44 ou déclenchent avec précision la ferroptose pourraient cibler sélectivement ces populations de cellules cancéreuses difficiles à traiter tout en préservant les tissus normaux. En révélant comment une classe de graisses méconnue relie la physique membranaire, le métabolisme du métal et le destin cellulaire, cette étude ouvre une nouvelle voie vers des interventions contre le cancer plus intelligentes et plus précises.
Citation: Mansell, R.P., Müller, S., Yang, JS. et al. Ether lipids influence cancer cell fate by modulating iron uptake. Nat Commun 17, 1835 (2026). https://doi.org/10.1038/s41467-026-68547-5
Mots-clés: lipides éther, cellules souches cancéreuses, absorption du fer, ferroptose, métastase