Clear Sky Science · fr
La palmitoylation de B7H3 déclenchée par l’acide palmitique favorise l’échappement immunitaire
Pourquoi cette recherche compte pour les patients atteints de cancer
La plupart des gens ont entendu que de nouveaux médicaments d’immunothérapie peuvent aider le système immunitaire à attaquer le cancer, mais de nombreux patients atteints d’un cancer colorectal courant tirent peu de bénéfice. Cette étude met au jour une astuce biochimique cachée que les tumeurs colorectales utilisent pour se protéger de l’attaque immune, et elle pointe vers un nouveau type de médicament — un petit peptide — qui pourrait améliorer l’efficacité de l’immunothérapie pour ces patients.
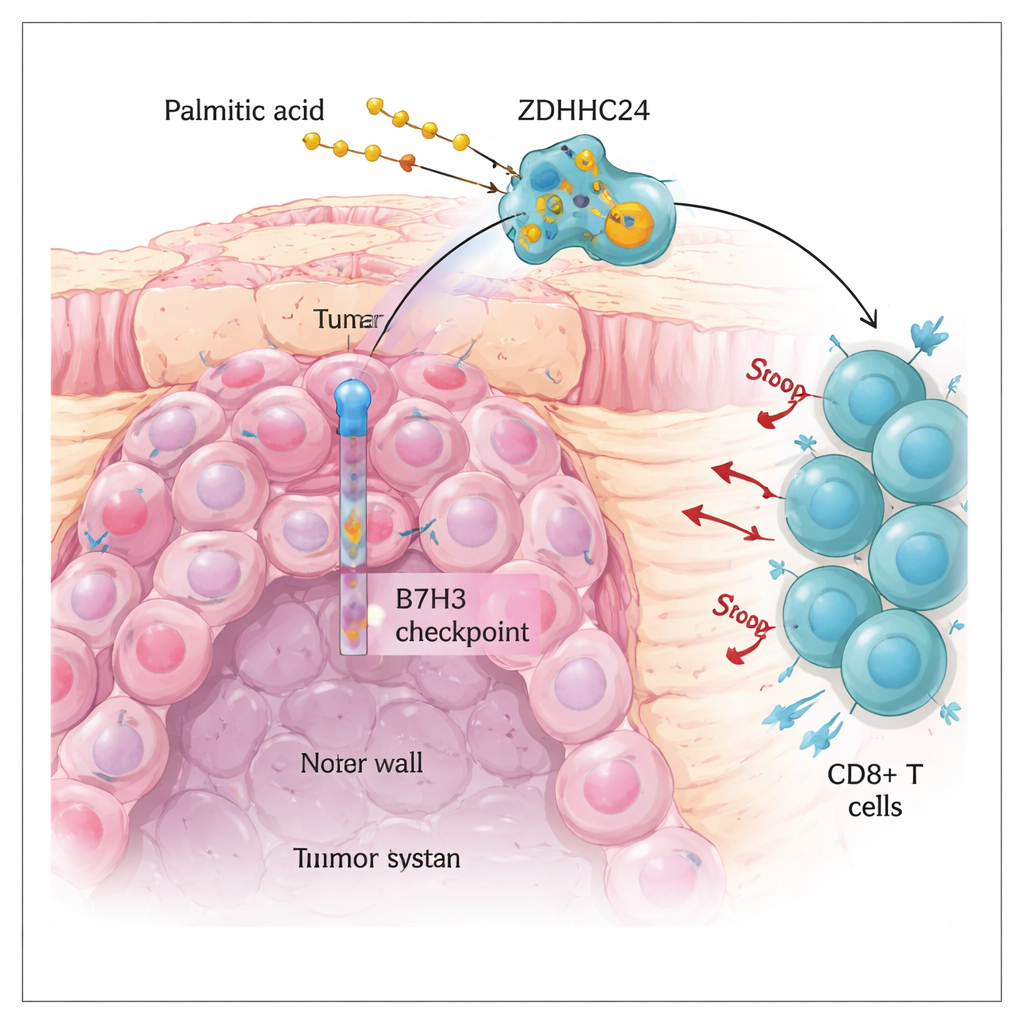
Un obstacle dans l’immunothérapie actuelle du cancer colorectal
Le cancer colorectal est l’un des cancers les plus fréquents dans le monde. Les médicaments d’immunothérapie qui lèvent les « freins » immunitaires, tels que les inhibiteurs de PD‑1 et PD‑L1, ont transformé la prise en charge d’une minorité de patients dont les tumeurs présentent de nombreuses erreurs d’ADN (les tumeurs dit MSI‑H). Malheureusement, la plupart des cancers colorectaux sont microsatellite‑stables (MSS) et répondent mal à ces traitements. Les auteurs se sont intéressés à une autre molécule frein appelée B7H3, qui se trouve à la surface des cellules tumorales et atténue l’activité des cellules tueuses, en particulier des lymphocytes CD8+. Ils ont constaté que la protéine B7H3 est fortement élevée dans les tumeurs MSS et associée à un pronostic plus défavorable, alors que le gène B7H3 n’est pas plus actif. Ce décalage soulève une question cruciale : qu’est‑ce qui maintient une telle abondance de la protéine B7H3 à la surface des cellules tumorales ?
Comment une graisse courante aide les tumeurs à se cacher
L’équipe a émis l’hypothèse que le métabolisme tumoral pouvait stabiliser B7H3. En comparant l’activité génique et les profils de petites molécules des tumeurs MSS et MSI‑H, ils ont découvert que de nombreuses voies liées aux lipides diffèrent, et qu’un acide gras en particulier — l’acide palmitique — se détache. Lorsqu’ils ont exposé des cellules de cancer du côlon à plusieurs produits de dégradation des lipides en laboratoire, seul l’acide palmitique a provoqué une augmentation nette du niveau de la protéine B7H3. Des expériences supplémentaires ont expliqué pourquoi : l’acide palmitique alimente un processus de modification chimique appelé palmitoylation, au cours duquel une chaîne lipidique est attachée à des sites spécifiques des protéines. Cette modification, réalisée par une enzyme nommée ZDHHC24 sur une cystéine unique de B7H3, rend B7H3 plus stable et plus abondante à la surface des cellules tumorales.
Bloquer la voie d’élimination d’un frein immunitaire
Les cellules éliminent normalement les protéines indésirables ou endommagées via des systèmes comparables au recyclage et à l’évacuation des déchets. Les chercheurs ont montré que B7H3 est principalement dégradée par une voie d’« auto‑manger » appelée autophagie, qui utilise un récepteur nommé SQSTM1/p62 pour marquer le cargo destiné à la destruction. Lorsque B7H3 est palmitoylée, elle se lie mal à ce récepteur et échappe à la dégradation autophagique, ce qui entraîne des niveaux persistants et élevés du frein immunitaire. Lorsque le site de palmitoylation a été muté pour ne plus pouvoir porter la chaîne lipidique, ou lorsque l’enzyme ZDHHC24 a été supprimée, B7H3 était mieux dirigée vers les « sacs‑poubelle » cellulaires et dégradée. Chez la souris, les tumeurs dépourvues de B7H3 palmitoylée croissaient plus lentement, ne modifiaient pas leur vitesse de croissance intrinsèque dans des animaux immunodéficients, et présentaient beaucoup plus de lymphocytes CD8+ ainsi qu’une activité de destruction tumorale renforcée. Cela montre que la modification agit principalement en désarmant l’immunité, et non en changeant la vitesse de division des cellules cancéreuses.
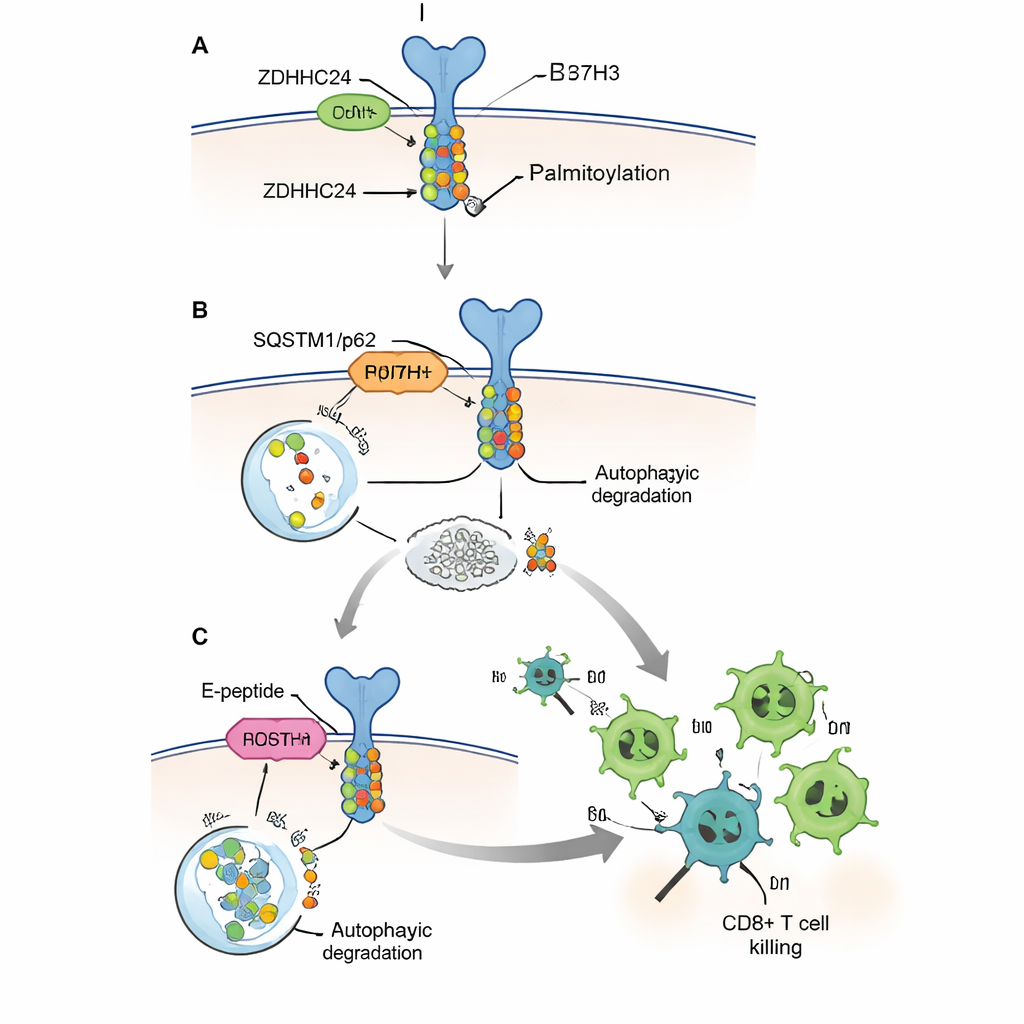
Atténuer le bouclier et renforcer les lymphocytes T
Parce qu’éliminer complètement ZDHHC24 ou B7H3 par génétique n’est pas une option thérapeutique praticable chez les patients, les auteurs ont conçu un peptide court pénétrant qu’ils appellent E‑peptide. Il imite un petit segment de la protéine B7H3 qui se lie normalement à ZDHHC24, agissant comme un leurre empêchant l’enzyme de modifier les véritables molécules B7H3. In vitro, l’E‑peptide a réduit la palmitoylation et le niveau de la protéine B7H3, a rétabli sa reconnaissance par la machinerie d’autophagie, et a permis aux lymphocytes CD8+ humains de tuer les cellules tumorales plus efficacement. Dans plusieurs modèles murins, y compris une souris humanisée portant des cellules immunitaires humaines et des tumeurs colorectales humaines, des injections d’E‑peptide ont réduit la taille des tumeurs, augmenté le nombre de lymphocytes CD8+ infiltrant les tumeurs, et stimulé la production de molécules effectrices clés telles que la granzyme B et l’interféron‑gamma.
Un nouvel allié pour l’immunothérapie existante
Enfin, les chercheurs ont testé si cette stratégie pouvait fonctionner en association avec le blocage standard de PD‑1. Dans des modèles murins de cancer colorectal, l’E‑peptide seul et l’anticorps anti‑PD‑1 seul ont chacun contrôlé partiellement la tumeur. Mais combinés, les deux traitements ont produit une suppression tumorale bien plus forte et durable, entraînant parfois la disparition des tumeurs et plus que doublant la survie moyenne par rapport aux témoins. Cela suggère que neutraliser le bouclier B7H3 en supprimant son « ancrage » lipidique peut compléter les médicaments ciblant la voie PD‑1.
Ce que cela signifie pour le futur du traitement du cancer
Concrètement, cette étude montre qu’une graisse alimentaire courante, l’acide palmitique, peut être détournée par les tumeurs colorectales pour armer chimiquement une protéine bloquant l’immunité (B7H3) et aider le cancer à se cacher. En bloquant cette attache chimique unique, les auteurs ont pu enlever l’armure, permettre aux systèmes d’élimination cellulaires d’évacuer B7H3, et rouvrir l’accès aux lymphocytes CD8+ pour attaquer. Si l’E‑peptide est pour l’instant un outil expérimental précoce, ce travail identifie la palmitoylation de B7H3 — et son enzyme ZDHHC24 — comme des cibles médicamenteuses prometteuses. Si des agents similaires se révèlent sûrs et efficaces chez l’humain, ils pourraient un jour transformer davantage de cancers colorectaux « froids », réfractaires à l’immunothérapie, en tumeurs « chaudes » reconnues et détruites par le système immunitaire.
Citation: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Mots-clés: immunothérapie du cancer colorectal, point de contrôle B7H3, métabolisme de l’acide palmitique, palmitoylation des protéines, immunité tumorale CD8 T