Clear Sky Science · fr
Les macrophages du poisson zèbre transforment les signaux physiques d’une blessure en perméabilisation vasculaire rapide
Ce qu’un petit poisson nous apprend sur le gonflement des blessures
Quand vous écorchez le genou, la zone devient rapidement rouge, gonflée et suintante. Ce changement rapide des vaisseaux sanguins voisins est crucial pour combattre l’infection et lancer la réparation, mais la façon dont le corps détecte une lésion et réagit en quelques secondes a été difficile à observer en temps réel. En utilisant des larves de poisson zèbre transparentes et des techniques avancées d’imagerie live, cette étude révèle comment des cellules immunitaires spécialisées, enroulées autour des vaisseaux, convertissent le choc physique d’une blessure en une fuite quasi instantanée des vaisseaux, apportant un éclairage nouveau sur l’inflammation, la cicatrisation et même les lésions pulmonaires humaines.
Observer la propagation de la lésion dans l’organisme
Les chercheurs ont travaillé avec de jeunes poissons zèbres, dont le corps transparent permet de suivre cellules et vaisseaux au microscope. Ils ont coupé la pointe de la nageoire caudale et rempli la circulation d’un colorant fluorescent qui reste à l’intérieur des vaisseaux sains. Quand les poissons blessés ont été replacés en eau douce normale, l’entrée soudaine d’eau dans les tissus a créé un « choc osmotique » autour de la blessure. En quelques minutes, les vaisseaux proches se sont dilatés et ont commencé à laisser fuiter le colorant fluorescent dans les tissus environnants, reproduisant le gonflement et l’exsudat observés autour des blessures humaines. En déplaçant les poissons entre de l’eau ordinaire et des solutions salines ou sucrées spécialement équilibrées, l’équipe a montré que cette perméabilisation vasculaire rapide dépend fortement des variations osmotiques plutôt que de la simple déchirure tissulaire.
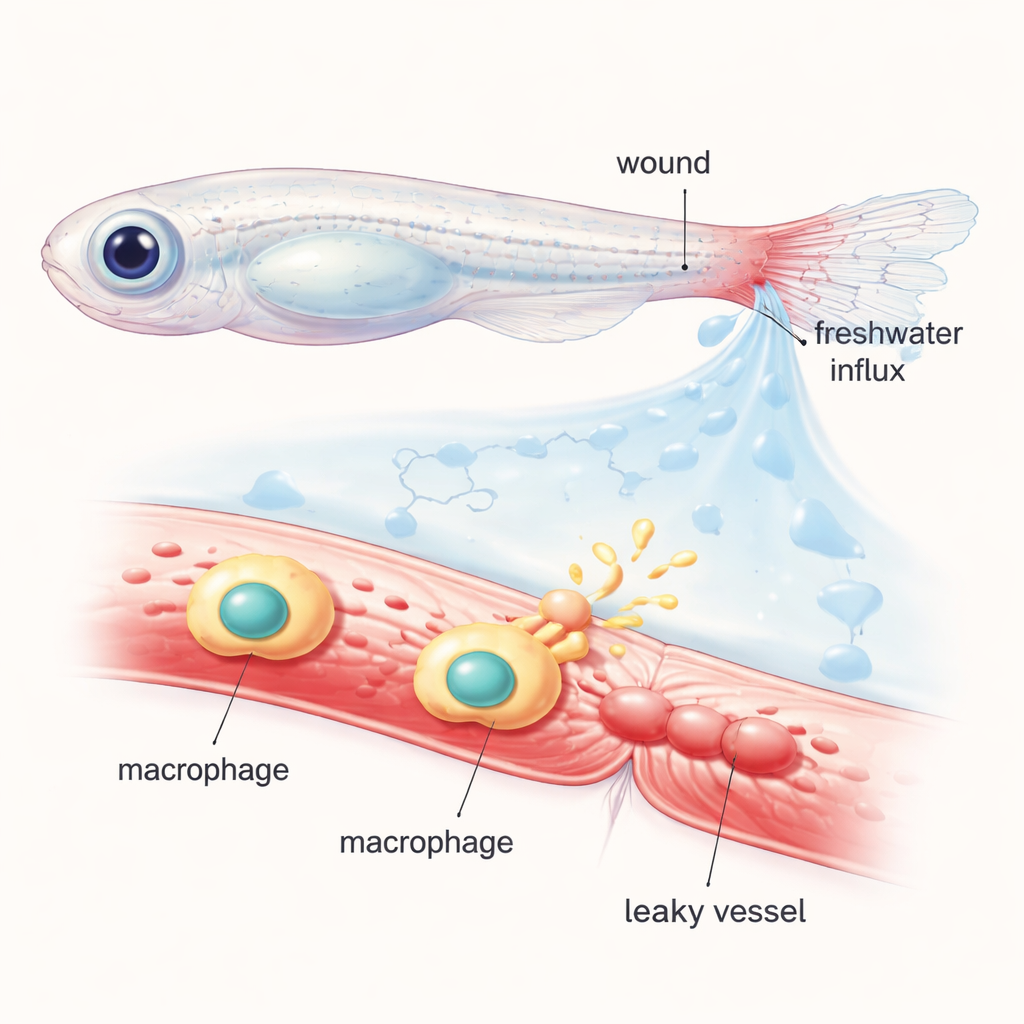
Suivre les messagers chimiques responsables de la fuite
Pour identifier quelles molécules convertissent le choc physique en signal de fuite, les scientifiques ont examiné une famille de composés lipidiques appelés eicosanoïdes, dérivés de l’acide arachidonique. Ces lipides sont bien connus pour leurs rôles dans l’inflammation et le contrôle du flux sanguin. En utilisant des mutants génétiques et des médicaments, ils ont désactivé sélectivement des enzymes individuelles de la voie des eicosanoïdes. Le blocage d’une enzyme clé, Alox5a (5‑lipoxygénase), ou de sa partenaire Lta4h a fortement réduit la quantité de colorant échappant des vaisseaux après le choc osmotique, sans empêcher la fermeture de la blessure elle‑même. En revanche, l’interférence avec d’autres enzymes apparentées avait peu d’effet. Cela pointe vers une branche spécifique de la voie lipidique comme principal moteur de la réponse de fuite rapide, agissant presque comme une vanne chimique que l’on peut ouvrir ou fermer à la demande.
Le rôle surprenant des cellules immunitaires qui étreignent les vaisseaux
Le sang contient différents types de cellules immunitaires ; chez les larves de poisson zèbre, les neutrophiles et les macrophages sont les principaux intervenants. L’équipe a utilisé un stratagème génétique astucieux pour détruire sélectivement soit les neutrophiles soit les macrophages avant la blessure. L’élimination des neutrophiles a eu peu d’effet sur la fuite vasculaire. Mais lorsque les macrophages ont été éliminés, la réponse de fuite a chuté d’environ moitié, reflétant l’effet du blocage de la voie lipidique Alox5a–Lta4h. Il est important de noter que ces manipulations n’ont pas empêché la plaie de se refermer rapidement, montrant que le recrutement des leucocytes et la fuite vasculaire peuvent être contrôlés en partie de manière indépendante. Cela a révélé que les macrophages périvasculaires — installés le long de la surface externe des vaisseaux — sont des traducteurs clés entre la blessure physique et le comportement vasculaire.
De l’étirement nucléaire au signal chimique
Comment ces macrophages périvasculaires détectent‑ils une blessure qui peut être située à distance ? La réponse tient à la façon dont leurs noyaux réagissent au stress mécanique. Quand le choc osmotique de la blessure se propage dans les tissus voisins, l’entrée d’eau provoque un léger gonflement cellulaire et une déformation nucléaire. Les chercheurs ont marqué une enzyme mécanosensible appelée cPla2 par un traceur fluorescent et l’ont exprimée spécifiquement dans les macrophages. Après la blessure en eau douce normale, cPla2 s’est rapidement déplacée vers la face interne de la membrane nucléaire des macrophages, suivant une onde qui a balayé le tissu à environ 50 micromètres par seconde, en phase avec la propagation des sels dissous. Cette translocation dépendait de conditions hypotonique et était beaucoup plus faible en solutions isotoniques. Les macrophages proches des vaisseaux ont présenté des impulsions nettes et réversibles de fixation nucléaire de cPla2, ce qui libère ensuite de l’acide arachidonique pour être converti en lipides induisant la fuite.
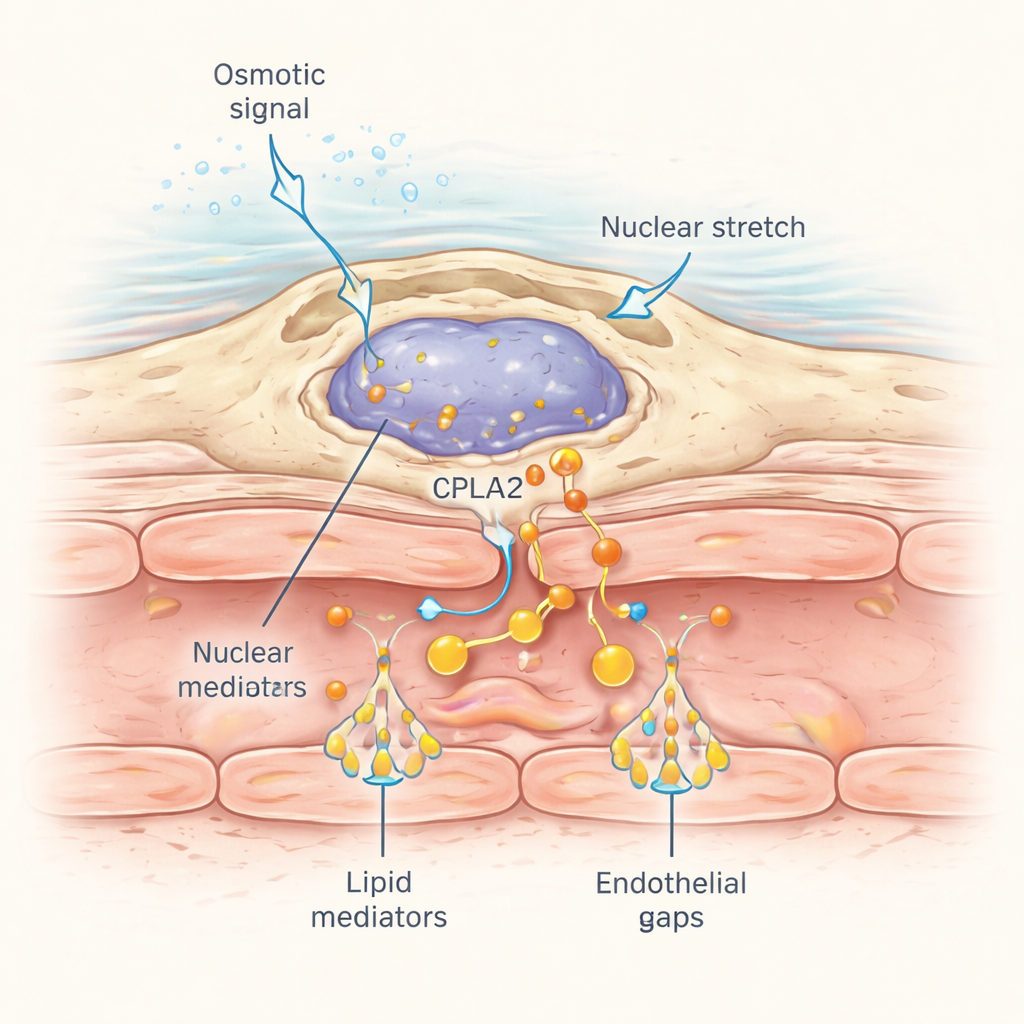
Pourquoi cela importe au‑delà du poisson
En bref, cette étude montre que certains macrophages agissent comme des sentinelles physiques : ils ressentent l’étirement des membranes tissulaires et nucléaires causé par les variations osmotiques au niveau d’une blessure, activent cPla2 à la surface nucléaire et produisent rapidement des messagers lipidiques qui indiquent aux vaisseaux voisins d’« ouvrir les portes » pour laisser entrer fluides et facteurs immunitaires. Bien que le poisson zèbre vive en eau douce et fasse face à des défis osmotiques particuliers, des voies mécanosensibles similaires fonctionnent probablement dans les tissus humains exposés à des pressions et débits changeants, comme les poumons lors de la ventilation mécanique. Comprendre comment l’étirement nucléaire et les signaux lipidiques contrôlent en temps réel la perméabilité vasculaire pourrait à terme orienter des traitements qui moduleraient l’inflammation — soit en atténuant les fuites nuisibles dans des affections comme les lésions pulmonaires aiguës, soit en stimulant des réponses utiles pour accélérer la réparation tissulaire.
Citation: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Mots-clés: guérison des plaies, vaisseaux sanguins, macrophages, inflammation, poisson zèbre