Clear Sky Science · fr
Des forces mécaniques issues de l'auto-assemblage peptidique intercellulaire pilotent la formation de sphéroïdes
Construire de minuscules tissus en laboratoire
Les scientifiques s'activent pour créer des versions miniatures de tissus humains qui se comportent comme les vrais. Ces modèles vivants peuvent rendre les essais de médicaments anticancéreux plus sûrs et rapprocher de nouvelles thérapies pour le diabète et d'autres maladies. Cette étude présente une méthode ingénieuse pour inciter les cellules à former des agrégats tridimensionnels réalistes, dotés de leurs propres réseaux primitifs « semblables à des vaisseaux » qui améliorent l'apport en nutriments et la fonction.
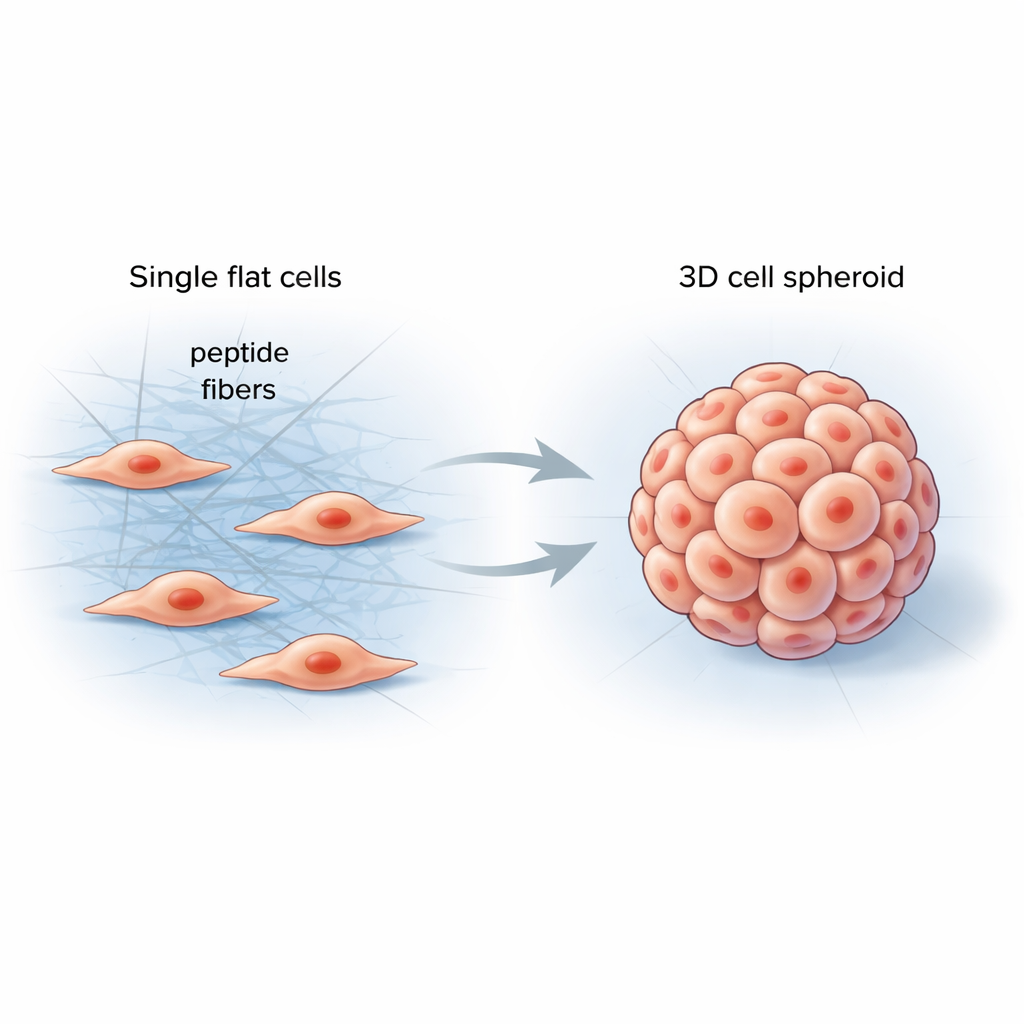
Aider les cellules à percevoir leur environnement
Dans notre corps, les cellules vivent dans un milieu souple mais structuré appelé matrice extracellulaire — un réseau de protéines qui soutient les tissus et envoie en continu des signaux mécaniques aux cellules. Les matériaux de laboratoire classiques peinent à reproduire cette complexité, produisant souvent des couches cellulaires plates qui se comportent très différemment des vrais organes ou tumeurs. Les chercheurs ont cherché à concevoir un matériau simple et programmable qui se formerait directement entre les cellules, rigidifierait leur environnement de façon contrôlée et les pousserait vers des formes tridimensionnelles plus naturelles.
Peptides intelligents qui s'assemblent entre les cellules
L'équipe a conçu de courts fragments protéiques, appelés peptides, capables de se lier entre eux pour former de longues fibres fines lorsqu'ils rencontrent des enzymes spécifiques à la surface des cellules. Lorsqu'on a ajouté ces peptides à des cellules cancéreuses, ils restaient inactifs au départ, comme une solution claire. Une fois qu'une enzyme des cellules a raccourci une partie de la molécule, les peptides se sont auto-assemblés rapidement en un réseau fibreux entourant et s'insinuant entre les cellules voisines. Cette nouvelle matrice fibreuse a modifié les forces mécaniques locales, incitant les cellules à se tirer les unes sur les autres, à remodeler leur échafaudage interne et à se rassembler en sphéroïdes 3D plutôt que de s'étaler en feuillet.
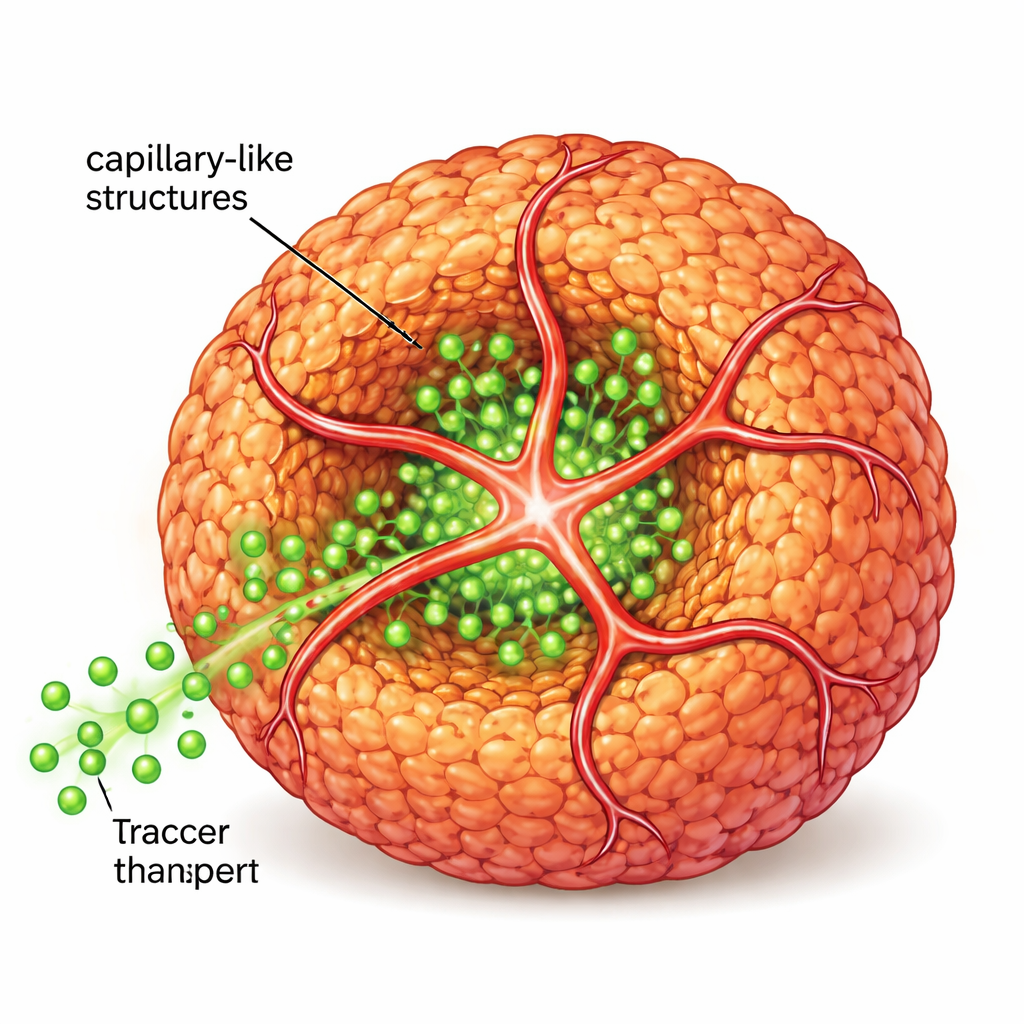
Des amas cellulaires vers des réseaux pseudo-vasculaires
Pour se rapprocher davantage du tissu réel, les scientifiques ont ensuite introduit des cellules endothéliales humaines, celles qui tapissent normalement les vaisseaux sanguins, ainsi qu'un second peptide portant une petite « étiquette d'adresse » qui attire ces cellules. Ensemble, les peptides originaux et modifiés ont formé un échafaudage de nanofibres partagé. Les cellules endothéliales ont utilisé cet échafaudage pour germer en extensions tubulaires qui enserraient et pénétraient les sphéroïdes, créant des structures semblables à des capillaires. Lorsque l'équipe a perfusé des molécules fluorescentes proches du sucre autour de ces structures, elles ont observé une pénétration beaucoup plus profonde dans le cœur du sphéroïde comparé à des sphéroïdes dépourvus de ces tubes internes, montrant que le transport des nutriments et des signaux était nettement amélioré.
Plus proches des vraies tumeurs et des îlots fonctionnels
Le profilage de l'activité génique a révélé que les sphéroïdes tumoraux contenant des structures pseudo-capillaires ressemblaient davantage aux échantillons de glioblastome de patients que ne le faisaient les cultures plates traditionnelles ou les sphéroïdes non vascularisés. Chez la souris, les sphéroïdes intégrant ces réseaux vasculaires primitifs ont donné lieu à des tumeurs plus grandes et mieux vascularisées, indiquant que le modèle in vitro capture des caractéristiques clés du comportement tumoral réel. La même stratégie a été appliquée aux cellules bêta pancréatiques, qui vivent normalement dans des îlots fortement vascularisés et sécrètent de l'insuline en réponse au glucose. Lorsque des sphéroïdes de cellules bêta ont été équipés de structures pseudo-capillaires à l'aide du système peptidique et de cellules endothéliales, ils ont montré une libération d'insuline beaucoup plus forte et plus finement régulée, suggérant un outil puissant pour la recherche sur le diabète et la médecine régénérative.
Pourquoi cela compte pour les thérapies futures
En laissant de simples peptides s'auto-assembler entre des cellules vivantes, ce travail propose une recette générale pour construire des tissus miniatures vascularisés qui ressemblent et fonctionnent davantage comme ceux du corps. Les sphéroïdes obtenus reflètent mieux les tumeurs de patients et les îlots fonctionnels, ce qui les rend précieux pour tester des médicaments, étudier les mécanismes de la maladie et concevoir de nouvelles thérapies cellulaires. Pour un public non spécialisé, l'idée essentielle est que fournir aux cellules cultivées en laboratoire la « bonne sensation » et de minuscules réseaux semblables à des vaisseaux peut améliorer de façon spectaculaire la fidélité avec laquelle elles imitent les tissus humains, accélérant potentiellement le passage de la recherche fondamentale aux traitements efficaces.
Citation: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Mots-clés: génie tissulaire, modèles du cancer, angiogenèse, organoïdes, auto-assemblage peptidique