Clear Sky Science · fr
Le jeûne intermittent inhibe le gliome dirigé par Tp53 via une régulation méthionine‑m6A médiée par le microbiote intestinal
Pourquoi donner une pause à l’intestin pourrait ralentir des tumeurs cérébrales mortelles
Le glioblastome est l’un des cancers du cerveau les plus agressifs, et les traitements actuels — chirurgie, radiothérapie et chimiothérapie — n’offrent souvent aux patients qu’un sursis limité. Cette étude pose une question simple mais puissante, aux grandes implications pour la vie quotidienne : la façon dont nous mangeons, en particulier le jeûne intermittent, peut‑elle modifier nos bactéries intestinales et notre chimie sanguine de manière suffisante pour ralentir sensiblement certains types de tumeurs cérébrales ?
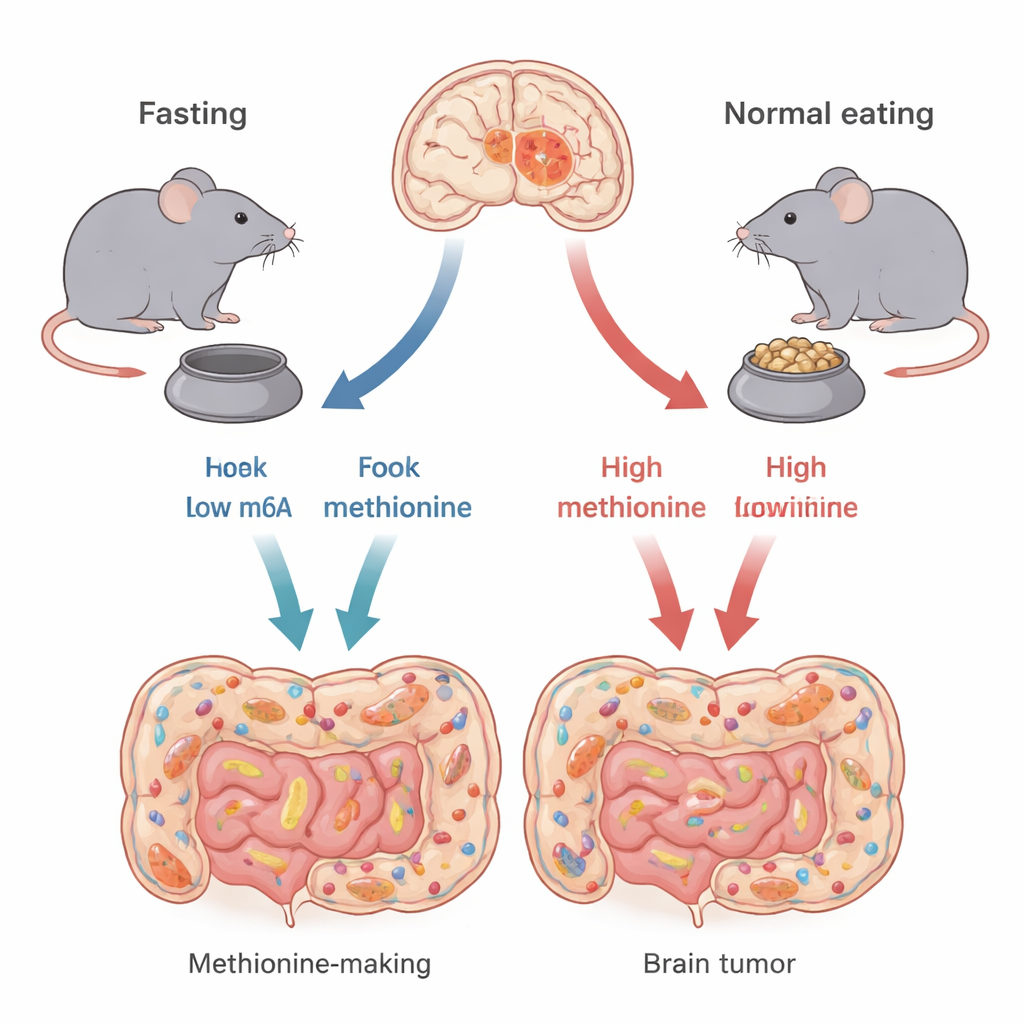
Différents types d’un même cancer cérébral
Tous les glioblastomes ne se valent pas. Les auteurs se concentrent sur deux principaux types génétiques, définis par des altérations des gènes TP53 et CDKN2A. Ces gènes participent au contrôle de la croissance et de la mort cellulaires. À l’aide de modèles murins reproduisant fidèlement chaque sous‑type humain, les chercheurs montrent que le jeûne intermittent — 24 heures sans nourriture suivies de 24 heures d’alimentation — n’aide pas toutes les tumeurs de la même façon. Les souris porteuses de tumeurs de type TP53 ont vécu plus longtemps et avaient des tumeurs plus petites en jeûnant, tandis que les souris avec des tumeurs de type CDKN2A ont présenté peu de bénéfice. Cela suggère que l’efficacité du jeûne dépend fortement du câblage génétique de la tumeur.
Du rythme alimentaire aux microbes intestinaux jusqu’à la chimie cérébrale
L’équipe a ensuite cherché à comprendre comment le jeûne produit cet effet sélectif. Comme la quantité totale de nourriture était la même entre les groupes, la différence clé était le timing de l’alimentation. Ce rythme a profondément remodelé le microbiote intestinal — la vaste communauté bactérienne de l’intestin. Chez les souris TP53 à jeûne, certains groupes bactériens qui produisent efficacement l’acide aminé méthionine, comme des souches particulières d’Alistipes et de Prevotella, ont décliné en abondance. Étant donné que la méthionine est un constituant essentiel que les animaux doivent obtenir par l’alimentation ou via les microbes intestinaux, ce basculement microbien s’est traduit par moins de méthionine passant de l’intestin dans le sang, puis jusqu’au cerveau.
Comment un seul nutriment module des signaux favorisant le cancer
La méthionine n’est pas seulement un nutriment ; c’est aussi le précurseur de la S‑adénosylméthionine (SAM), le « donneur de méthyle » universel de la cellule. La SAM alimente un processus de marquage chimique de l’ARN appelé m6A. Ces marques contribuent à réguler l’intensité d’expression de certains gènes. Dans le modèle tumoral TP53, le jeûne a réduit les niveaux de méthionine et de SAM dans le sang et dans les régions tumorales cérébrales. En combinant plusieurs approches « omiques » — séquençage ARN standard, profilage ARN monocellulaire et cartographies spatiales de l’activité génique et des métabolites — les chercheurs ont observé moins de marques m6A sur des ARN liés au cancer sous jeûne. Une cible importante était TGFB2, un gène de la voie de signalisation TGF‑β, connu pour favoriser la croissance et l’invasion tumorales. Avec le jeûne, l’enzyme METTL3 (qui écrit les marques m6A) et TGFB2 étaient toutes deux atténuées, et la signalisation TGF‑β s’est affaiblie.
Prouver la causalité par des interventions ciblées
Pour dépasser la simple corrélation, les scientifiques ont réalisé des expériences de « sauvetage ». Ils ont bloqué METTL3 avec un médicament, ou transféré le microbiote d’animaux jeûnant à des souris normalement alimentées, et ont observé un ralentissement de la croissance tumorale même sans jeûne — ce qui soutient l’idée que le microbiote et la machinerie m6A sont des acteurs clés. Inversement, lorsque des souris en jeûne ont reçu de la méthionine supplémentaire ou un médicament favorisant les marques m6A, leurs tumeurs ont évolué comme chez des souris normalement alimentées, et l’avantage de survie a disparu. Fait important, perturber la flore intestinale avec des antibiotiques à large spectre a effacé de nombreuses modifications liées au jeûne, soulignant que la communauté microbienne constitue un pivot central de cette chaîne d’événements.
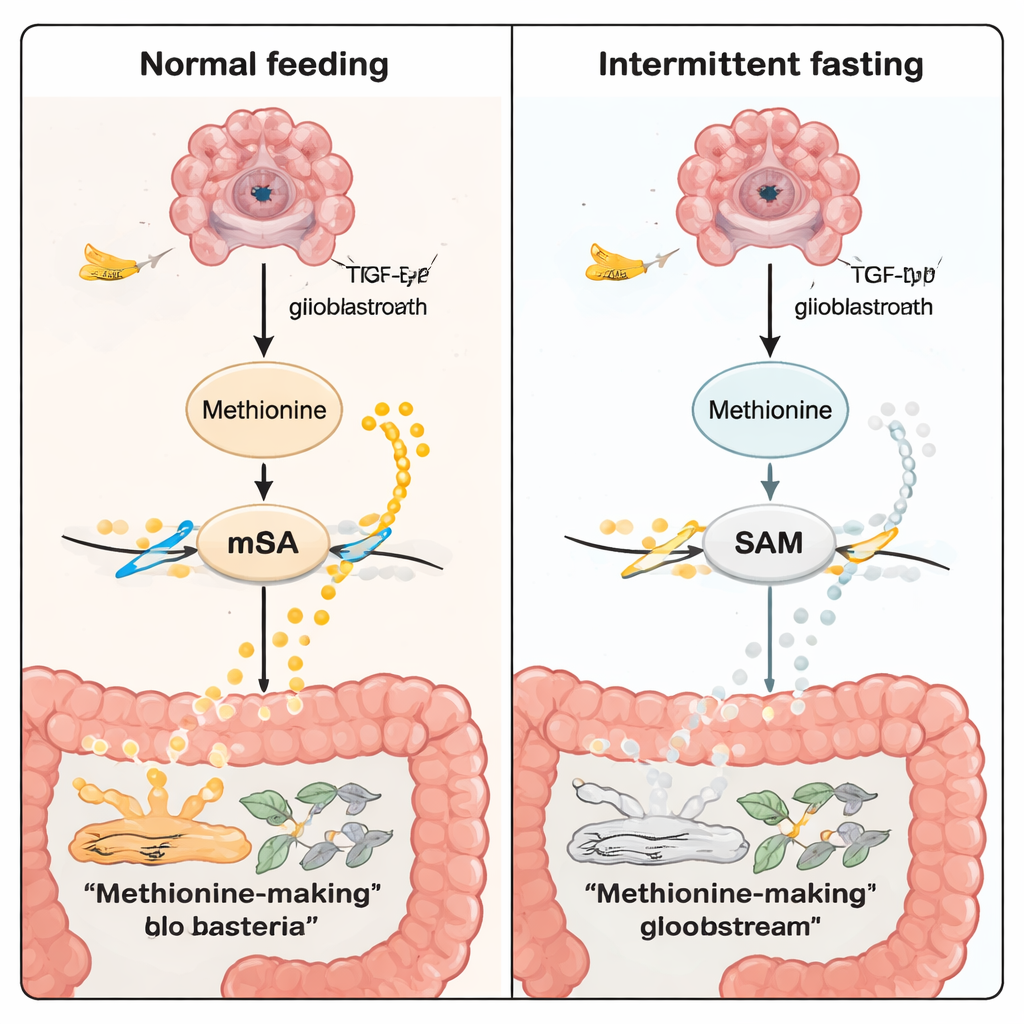
Ce que cela signifie pour les personnes et les thérapies futures
Pour le grand public, le message principal est que tous les cancers, et même tous les glioblastomes, ne répondront pas de la même manière à une stratégie alimentaire comme le jeûne intermittent. Dans les gliomes de type TP53, le jeûne semble « communiquer » avec le cerveau via l’intestin : il modifie les bactéries intestinales, ce qui diminue la production de méthionine, réduit le marquage chimique de l’ARN et atténue des signaux de croissance puissants à l’intérieur des cellules tumorales. Bien que ces travaux aient été réalisés chez la souris et nécessitent une traduction clinique prudente, ils ouvrent la voie à un futur où des habitudes de vie simples, des traitements basés sur le microbiote intestinal et des médicaments ciblant la méthionine ou les voies m6A pourraient être adaptés au sous‑type génétique de la tumeur d’un patient.
Citation: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Mots-clés: jeûne intermittent, glioblastome, microbiome intestinal, métabolisme de la méthionine, modification ARN m6A