Clear Sky Science · fr
Oxydation simultanée du sulfure et réduction des sulfates pour l’homéostasie redox intracellulaire en conditions fortement acides
Pourquoi le nettoyage des gaz toxiques exige des microbes astucieux
De nombreuses industries émettent du sulfure d’hydrogène, un gaz toxique à l’odeur d’œuf pourri qui peut corroder les équipements, polluer l’air et nuire aux travailleurs. Pour l’éliminer, les ingénieurs s’appuient de plus en plus sur des microbes qui transforment le sulfure en formes de soufre moins dangereuses. Cet article révèle une stratégie microbienne inattendue : un Mycobacterium nouvellement identifié qui exécute simultanément deux voies chimiques normalement opposées pour à la fois détoxifier rapidement le sulfure et se protéger des dégâts internes, même dans des conditions extrêmement acides.
Une lutte d’opposition dans le cycle du soufre
Dans la nature, le cycle du soufre est animé par deux réactions contraires. Certains microbes oxydent le sulfure (la forme la plus réduite et la plus toxique) en produits moins nocifs comme le soufre élémentaire ou le sulfate, en tirant de l’énergie du processus. D’autres font le chemin inverse, réduisant le sulfate en sulfure afin de construire des composants cellulaires essentiels, comme des acides aminés contenant du soufre. Parce que ces réactions s’annulent mutuellement, les biologistes supposaient de longue date qu’une cellule unique éviterait de faire tourner les deux voies à la fois ; cela semblerait futile, comme chauffer et climatiser une maison les fenêtres ouvertes. 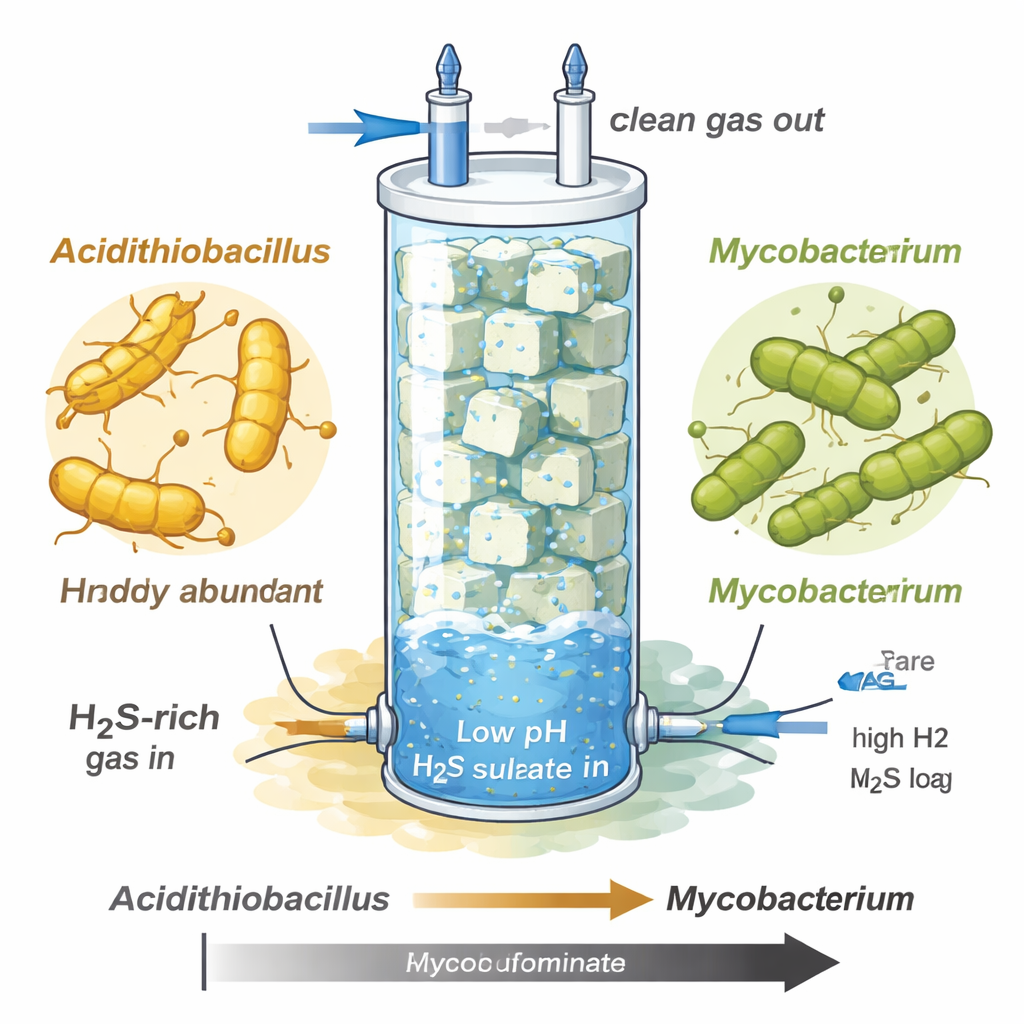
À la recherche d’un survivant dans un réacteur extrême
Les chercheurs ont étudié un filtre biologique à ruissellement : une colonne de verre haute remplie de cubes de mousse, conçue pour épurer le sulfure d’hydrogène des flux gazeux similaires au biogaz brut ou au gaz naturel. En augmentant la charge en sulfure et en maintenant le système très acide (pH autour de 1–1,5), la communauté microbienne a changé de façon spectaculaire. Au départ, un oxydant du sulfure bien connu, Acidithiobacillus, prospérait et convertissait une grande partie du sulfure en sulfate, mais il s’est effondré sous le stress sulfureux extrême. À sa place, une espèce de Mycobacterium jusque-là non caractérisée, désignée MAG-M116, a pris le relais et a dominé presque entièrement la communauté, malgré une croissance plus lente durant la phase initiale moins sévère.
Un microbe qui défie les règles habituelles
Les analyses génétiques et protéiques ont montré que MAG-M116 possède un dispositif métabolique inhabituel. Il porte une enzyme clé, la sulfide:quinone oxydoréductase, qui oxyde le sulfure seulement jusqu’au soufre élémentaire solide, lequel s’accumule sous forme de minuscules particules. En parallèle, le microbe dispose d’un ensemble complet de gènes pour la réduction assimilatrice des sulfates, la voie qui incorpore le sulfate dans la cellule et le réduit pour synthétiser des acides aminés comme la cystéine et la méthionine. En conditions de forte concentration en sulfure, les deux voies étaient activées simultanément. L’oxydation du sulfure injectait des électrons dans la machinerie énergétique de la cellule, tandis que la réduction du sulfate absorbait une partie de ce flux d’électrons, reliant ainsi les deux directions du cycle du soufre au sein d’une même cellule.
Transformer un cycle « gaspilleur » en soupape de sécurité
Faire fonctionner les deux voies à la fois pourrait, en théorie, paraître vain — dépenser de l’énergie sans gain net. Mais l’équipe montre que pour MAG-M116 cela agit comme une soupape de sécurité contre l’excès d’électrons. L’oxydation d’importantes quantités de sulfure libère une vague d’électrons dans la chaîne respiratoire de la cellule, qui peut fuir et générer des espèces réactives de l’oxygène (ROS) — des molécules dommageables qui attaquent l’ADN, les protéines et les membranes. En réduisant activement le sulfate en acides aminés, la cellule détourne 10–14 % de ces électrons vers un travail constructif, réduisant l’accumulation d’un état trop réduit et susceptible de fuite. Des expériences comparant des conditions avec et sans sulfate ont montré que la réduction active du sulfate diminuait la production de ROS d’environ 60 % et empêchait l’accumulation de cofacteurs réduits qui alimenteraient autrement les dommages oxydatifs. 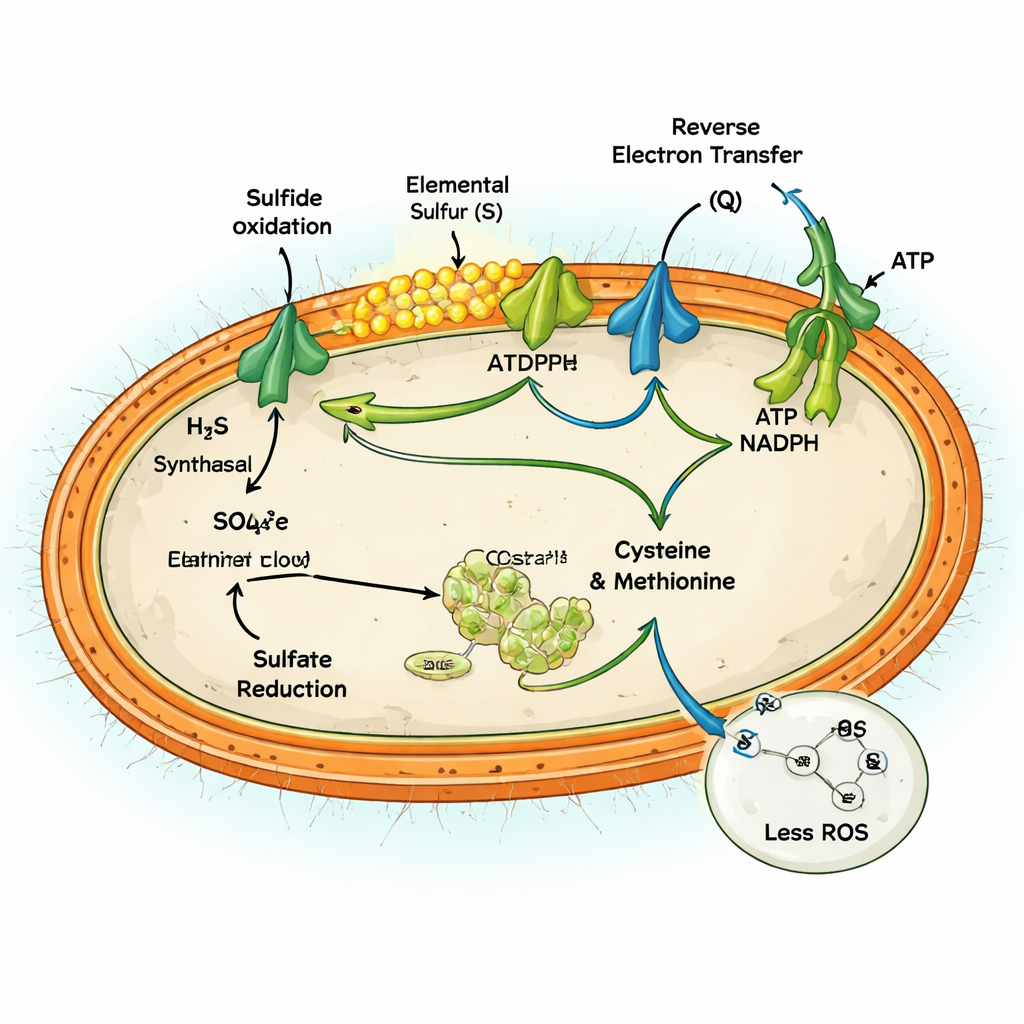
Du gaz toxique à des produits utiles
Dans les étapes ultérieures de fonctionnement du réacteur, lorsque MAG-M116 dominait, presque tout le sulfure d’hydrogène entrant était converti en soufre élémentaire solide, plutôt qu’en sulfate. Parallèlement, les chercheurs ont détecté des niveaux croissants de cystéine et de méthionine en phase liquide, ce qui suggère que le microbe libérait des acides aminés sulfurés en excès dans son environnement. Cette combinaison — soufre élémentaire stable plus composés organiques sulfurés de valeur — transforme ce qui était autrefois un polluant dangereux en un mélange de produits récupérables utiles en agriculture, matériaux et systèmes énergétiques.
Ce que cela implique pour la santé et la technologie
Pour un non-spécialiste, le message clé est que ce Mycobacterium a résolu un double problème : il peut épurer de fortes concentrations d’un gaz toxique tout en maintenant l’équilibre de sa chimie interne. Il le fait en faisant fonctionner des réactions du soufre en « pousser–tirer » qui seraient normalement séparées, utilisant ce cycle apparemment gaspilleur comme amortisseur intégré contre l’excès d’électrons et les radicaux oxygénés nocifs. Cette découverte suggère non seulement de nouvelles façons de concevoir des bioréacteurs robustes et à faible pH pour l’élimination du sulfure et des sulfates, mais laisse aussi entendre que des microbes apparentés, y compris certaines espèces pathogènes de Mycobacterium, pourraient employer des astuces similaires pour survivre aux attaques oxydatives à l’intérieur du corps humain.
Citation: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Mots-clés: cycle du soufre, sulfure d’hydrogène, Mycobacterium, homéostasie redox, biodésulfuration