Clear Sky Science · fr
Une cellule artificielle capable de la transduction du signal médiée par ADRB2 pour la régulation de la glycogénolyse
Apprendre à de minuscules bulles à communiquer
Imaginez une bulle de savon microscopique capable de détecter un signal ressemblant à une hormone à l’extérieur, puis de « décider » de brûler du carburant stocké à l’intérieur, un peu comme une cellule humaine réelle. Cette étude construit exactement ce type de cellule artificielle, montrant comment des imitateurs cellulaires fabriqués par l’homme peuvent recevoir un message chimique et le convertir en une chimie énergétique contrôlée. Ce travail nous rapproche de vecteurs médicamenteux intelligents, de tissus synthétiques et de formes de vie synthétiques simples capables de réagir à leur environnement.
Construire une cellule de l’extérieur vers l’intérieur
Les cellules réelles écoutent constamment leur environnement via des récepteurs dans leur membrane externe. Les auteurs ont cherché à reproduire l’une de ces voies naturelles en n’utilisant que des composants purifiés et de simples bulles de lipides, appelées vésicules géantes. Ils se sont concentrés sur un récepteur humain courant, le récepteur β2‑adrénergique (ADRB2), qui aide dans notre organisme à réguler la fréquence cardiaque, la fonction pulmonaire et l’utilisation des combustibles. Lorsque ce récepteur rencontre un médicament comme l’isoprotérénol (ISO), il déclenche normalement une chaîne d’événements internes qui produit une molécule messagère appelée AMPc, laquelle contrôle à son tour la façon dont les cellules dégradent le glycogène, forme de stockage du glucose. Reproduire toute cette séquence dans une cellule artificielle n’avait pas été réalisé auparavant.
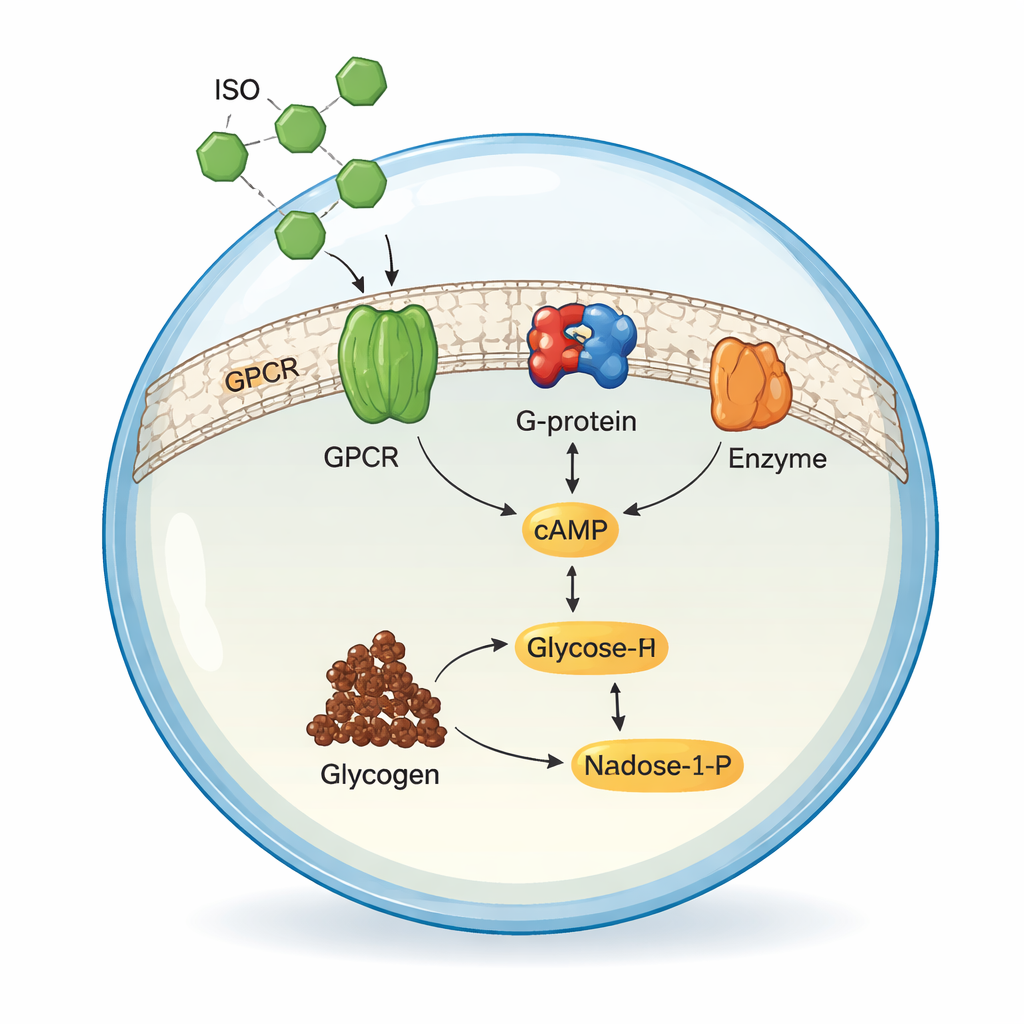
Reconstituer la première relais du signal
L’équipe a d’abord reconstruit les premières étapes de la voie de signalisation en solution, hors de toute membrane. Ils ont produit trois protéines humaines dans des cellules d’insecte : ADRB2, sa sous‑unité partenaire de protéine G (Gsα) et une enzyme appelée adénylate cyclase V (ADCY5), qui fabrique de l’AMPc à partir de l’ATP. Lorsqu’ils ont mélangé ces éléments avec l’ISO dans des conditions soigneusement ajustées, l’activation du récepteur adrénergique a conduit ADCY5 à transformer l’ATP en AMPc. En mesurant l’AMPc par chromatographie liquide haute performance, les chercheurs ont optimisé le pH, la température et le taux de magnésium et ont constaté que leur système reconstitué fonctionnait aussi efficacement, voire mieux, que de nombreuses préparations antérieures, confirmant que la chimie centrale de signalisation était en place.
Installer de vrais récepteurs dans des membranes artificielles
Puis, les auteurs ont intégré les trois protéines dans les membranes de vésicules unilamellaires géantes — des bulles lipidiques de la taille d’une cellule qui servent de châssis pour les cellules artificielles. Ils ont marqué fluorescentement ADRB2 et ADCY5 pour vérifier que les protéines étaient insérées dans la membrane, se déplaçaient librement et étaient présentes en grand nombre, avec environ 1,8 million de récepteurs par vésicule. Un traitement enzymatique a montré que plus de 94 % de ces récepteurs étaient orientés correctement, leurs sites de liaison exposés vers l’extérieur. Une sonde GTP fluorescente a confirmé que la liaison d’ISO à la membrane activait réellement les protéines G à l’intérieur des vésicules. Cela signifiait que, en principe, les cellules artificielles pouvaient transmettre un signal ISO externe à travers leur membrane comme le font les cellules naturelles.
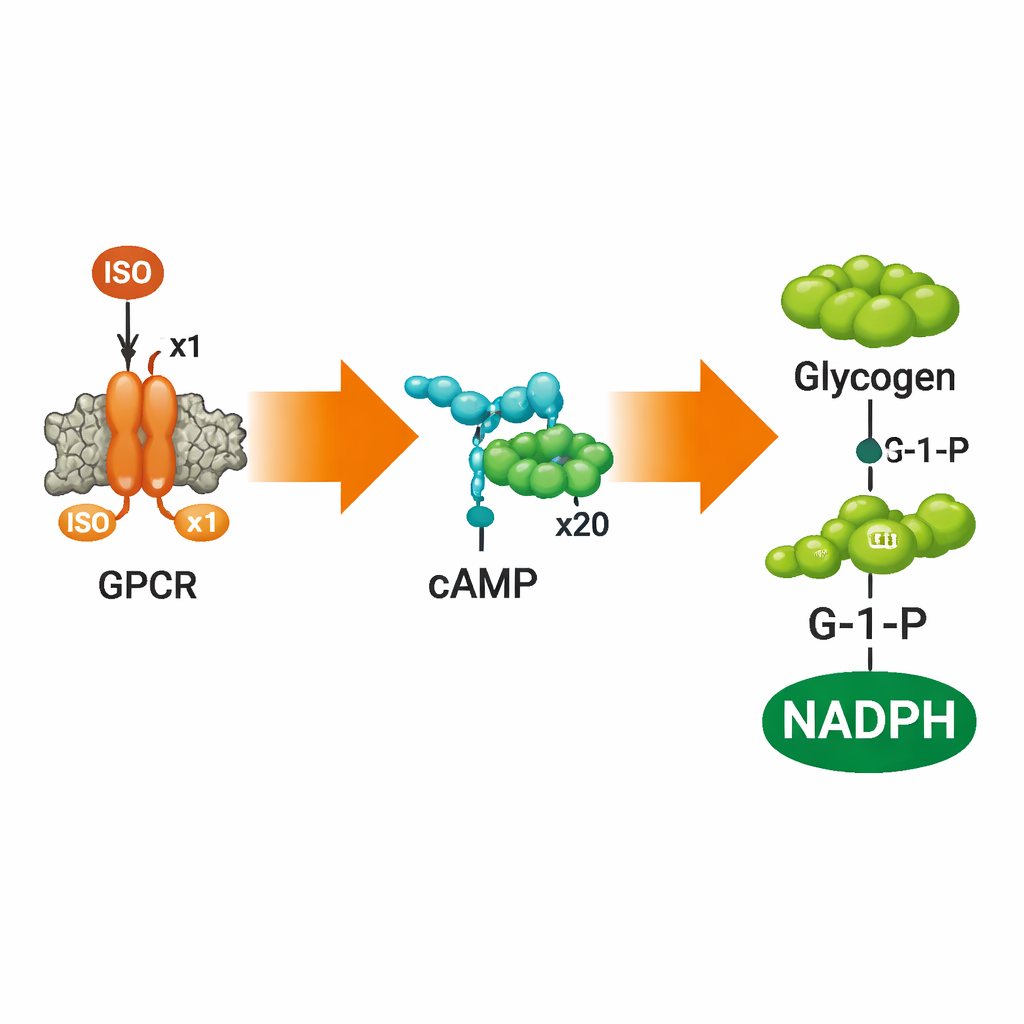
Convertir les signaux en dégradation du carburant
Pour vérifier si ces cellules synthétiques pouvaient faire quelque chose d’utile avec le signal, l’équipe a ajouté un capteur d’AMPc puis une voie complète de dégradation du glycogène à l’intérieur des vésicules. À l’aide d’une sonde AMPc basée sur le FRET, ils ont montré que l’ajout d’ISO à l’extérieur des vésicules entraînait une augmentation des niveaux d’AMPc à l’intérieur de manière dépendante de la dose, puis un plateau lorsque les récepteurs étaient saturés, reflétant le comportement classique des récepteurs couplés aux protéines G naturels. Des médicaments qui bloquent ou désactivent ADRB2 — alprénolol et carazolol — ont interrompu cette réponse exactement comme prévu. Lorsque les auteurs ont également encapsulé cinq enzymes qui convertissent normalement le glycogène en glucose‑1‑phosphate (G‑1‑P) puis en NADPH, la stimulation par ISO a conduit à une production mesurable à la fois de G‑1‑P et de NADPH à l’intérieur des cellules artificielles, suivie par spectrométrie de masse, chromatographie et fluorescence.
Amplifier un chuchotement en un cri
Une découverte clé est l’intensité de l’amplification de la réponse interne. Une quantité modeste d’ISO à l’extérieur des vésicules a produit environ 22 fois plus de molécules d’AMPc que de molécules d’ISO, et cette amplification s’est accrue aux étapes suivantes de la voie. Au moment où le signal avait entraîné la dégradation du glycogène et la conversion en 6‑phosphogluconolactone avec production concomitante de NADPH, l’amplification globale dépassait cent fois. Cette amplification progressive est une caractéristique des signalisations hormonales naturelles et montre que le système artificiel ne se contente pas de détecter l’ISO : il traite et amplifie le message en une sortie métabolique robuste.
Pourquoi cela compte pour la vie synthétique future
Pour un non‑spécialiste, les détails techniques se résument à une idée simple : les chercheurs ont appris à une cellule minimaliste et fabriquée par l’homme à écouter et réagir comme une cellule vivante. Une molécule de médicament externe s’arrime sur un récepteur humain réaliste, un signal est transmis à travers une membrane synthétique et un réseau enzymatique interne répond en mobilisant de l’énergie chimique stockée. Démontrer cette chaîne complète — de l’activation du récepteur à un métabolisme contrôlé — dans un système artificiel épuré est une avancée majeure vers des cellules synthétiques autonomes capables de détecter, décider et agir de manière utile, par exemple en ajustant leur propre réserve d’énergie ou en délivrant des thérapies uniquement lorsqu’elles détectent les bons signaux chimiques.
Citation: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
Mots-clés: cellules artificielles, transduction du signal, GPCR, glycogénolyse, biologie synthétique