Clear Sky Science · fr
Libération spatiotemporelle contrôlée de médicaments via un système click-release utilisant la chimie mono-alcyl-hydroxylamine et cyclooctyne
Activer des médicaments puissants uniquement là où ils sont nécessaires
Beaucoup de médicaments modernes sont extrêmement puissants, ce qui est utile pour combattre le cancer ou soulager la douleur — mais comporte des risques pour le reste de l’organisme. Cette étude décrit un « interrupteur » chimique qui permet de conserver les médicaments sous une forme inactive et inoffensive, puis de les activer uniquement à un lieu et un moment choisis, par exemple à l’intérieur d’une tumeur ou dans une petite zone nécessitant une anesthésie locale.
Un nouveau type d’interrupteur chimique
Les chercheurs s’appuient sur le concept de « chimie click », une famille de réactions appréciée pour leur rapidité, leur précision et leur compatibilité avec des milieux biologiques. Les réactions click classiques joignent deux molécules de façon permanente. Ici, l’équipe inverse cette logique : leur réaction click est directement liée à la rupture d’une liaison et à la libération d’un médicament ou d’une molécule signal. Les acteurs clés sont une molécule cyclique appelée cyclooctyne et une petite partenaire, la mono‑alcyl‑hydroxylamine. Lorsque ces deux éléments se rencontrent, ils se lient très rapidement puis se réarrangent de façon à ce qu’un « chargement » lié soit libéré. En fixant différents médicaments ou colorants fluorescents comme chargement, la même réaction de base peut servir à de nombreuses applications. 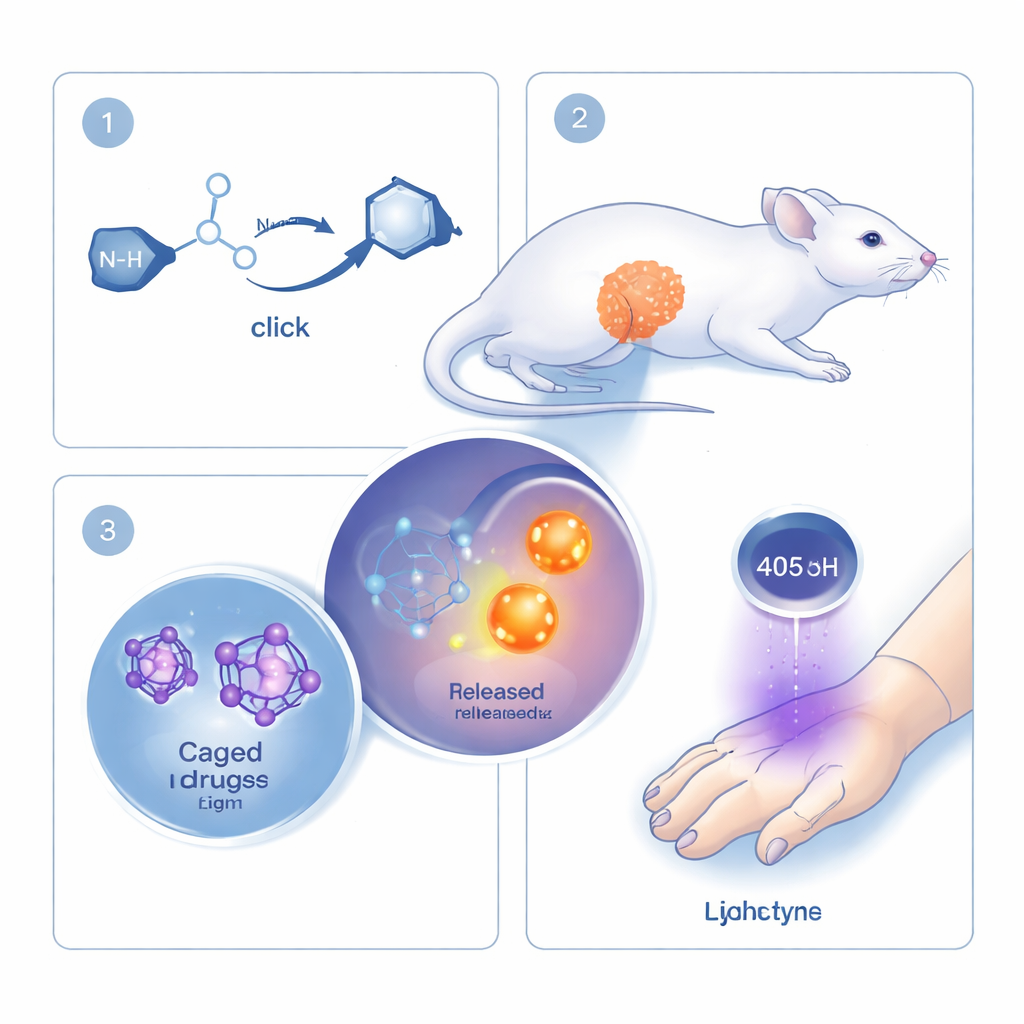
Libération rapide et propre à l’intérieur et à l’extérieur des cellules
Pour vérifier que cet interrupteur serait pratique, l’équipe a mesuré la vitesse de la réaction et l’efficacité de libération du chargement. Ils ont constaté que des mono‑alcyl‑hydroxylamines soigneusement choisies réagissent bien plus vite que l’hydroxylamine simple, atteignant une conversion presque complète en l’espace de minutes à heures selon la structure. Fait important, les étapes chimiques qui libèrent réellement le chargement sont si rapides et sélectives que presque toute la molécule liée est relâchée, avec très peu de sous‑produits indésirables. Les auteurs ont testé une gamme de cargaisons, incluant des colorants fluorescents et même un ion fluorure, et ont montré que le système peut rompre plusieurs types de liaisons couramment utilisés en conception de médicaments, comme les carbamates et les éthers.
Illuminer des cellules et activer des médicaments anticancéreux à la demande
Ensuite, les chercheurs sont passés à des cellules vivantes. Ils ont d’abord dissimulé des colorants fluorescents intenses derrière l’interrupteur chimique et ajouté ces sondes « cagées » à des cellules cancéreuses. Elles sont restées sombres tant que rien ne les activait, montrant que les sondes ne s’activent pas par accident. Lorsque le partenaire mono‑alcyl‑hydroxylamine a été ajouté, les colorants ont été libérés et les cellules se sont illuminées en bleu, vert ou proche infrarouge, confirmant que la réaction fonctionne de manière fiable en environnement biologique. Ils ont ensuite appliqué la même idée au doxorubicine, un médicament de chimiothérapie largement utilisé. Sous forme de pro‑médicament cagé, la doxorubicine était bien moins toxique pour les cellules. Mais en présence du partenaire click, le médicament actif a été libéré efficacement, retrouvant une capacité à tuer les cellules cancéreuses presque comparable à celle de la doxorubicine libre.
Construire des déclencheurs intelligents pour le lieu et le moment
Une limitation de nombreux systèmes click existants est que les éléments réactifs sont toujours « activés », ce qui complique le contrôle précis du lieu et du moment de l’action. Pour résoudre cela, l’équipe a temporairement bloqué la réactivité de la mono‑alcyl‑hydroxylamine avec de petites capsules protectrices retirées uniquement par des déclencheurs spécifiques. Ils ont créé des versions réactives à des niveaux élevés de glutathion (une petite molécule abondante dans de nombreuses tumeurs), à des enzymes, et à des flashes de lumière violette. Dans des cellules et chez des souris porteuses de tumeurs, la version sensible au glutathion est restée silencieuse en conditions normales mais s’est activée dans l’environnement chimiquement réducteur de la tumeur, libérant des colorants fluorescents ou activant le pro‑médicament de doxorubicine exactement là où la tumeur se développait. Les souris traitées par la combinaison pro‑médicament plus déclencheur ont montré une régression tumorale plus importante que celles recevant de la doxorubicine standard, tout en subissant une moindre exposition du médicament dans des organes sensibles comme le cœur.
Anesthésie locale télécommandée par la lumière
Pour démontrer le contrôle temporel, les auteurs ont conçu une seconde application : une anesthésie locale guidée par la lumière. Ils ont lié le médicament anesthésiant tetracaïne à leur échafaudage cyclooctyne, le rendant inactif, et ont mélangé ce pro‑médicament avec une version photosensible de l’hydroxylamine dans un gel thermo‑réactif. Injectée dans la patte d’un rat, la formulation n’a rien fait tant que la peau n’était pas illuminée à 405 nanomètres. L’illumination a déclenché la réaction click‑release, libérant la tetracaïne et produisant un engourdissement comparable à une injection directe de tetracaïne. En modulant la durée et l’intensité de l’éclairement, les chercheurs ont pu régler la durée du bloc nerveux, et ils ont même réussi à déclencher des vagues répétées d’anesthésie à partir d’une seule injection. 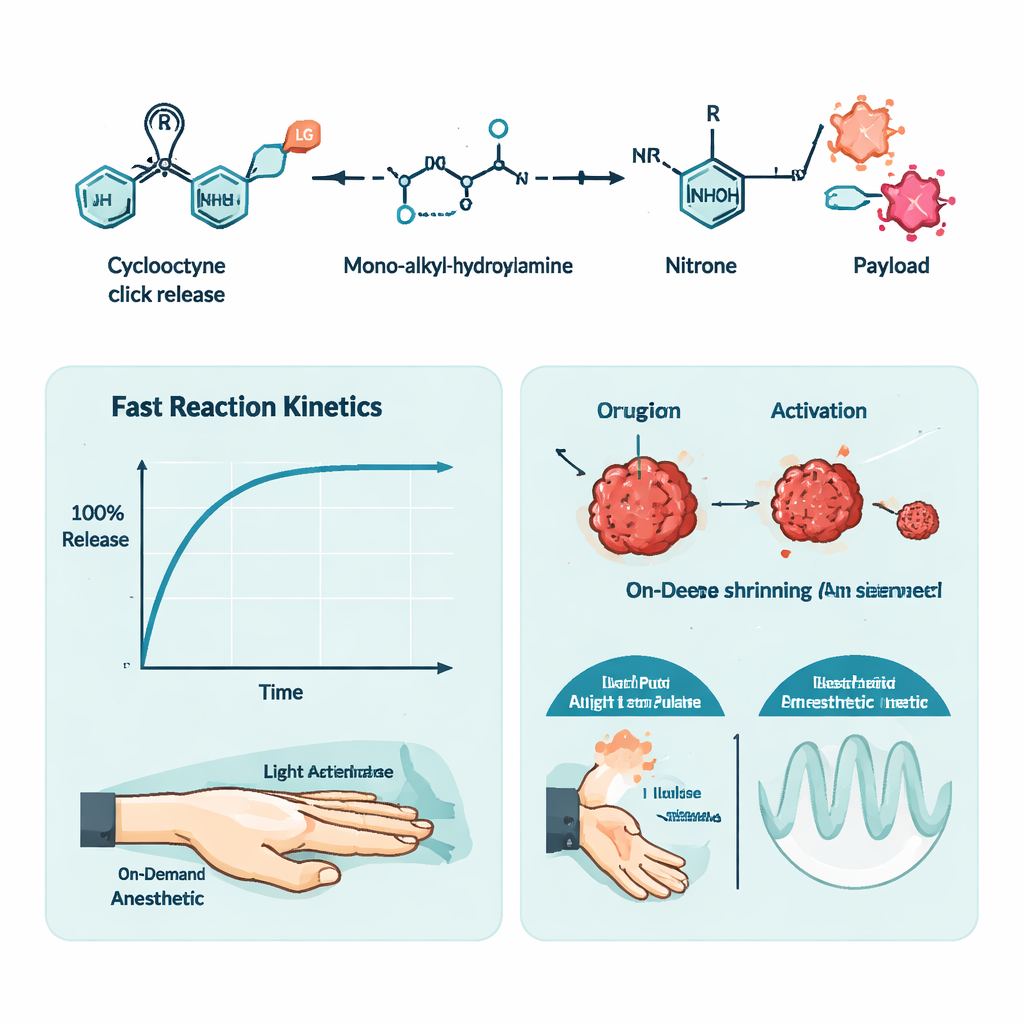
Ce que cela pourrait signifier pour les traitements futurs
Pour les non‑spécialistes, le message clé est que ce travail propose une télécommande chimique flexible pour les médicaments : des traitements peuvent être délivrés sous une forme sûre et silencieuse puis activés uniquement au bon endroit et au bon moment, en utilisant des signaux provenant du corps lui‑même ou d’une source lumineuse externe. Bien que des tests supplémentaires soient nécessaires avant une utilisation clinique, l’approche pourrait à terme rendre les traitements anticancéreux plus ciblés et moins toxiques, permettre un contrôle de la douleur personnalisable après chirurgie, et soutenir une gamme d’autres thérapies qui bénéficient d’un contrôle spatiotemporel précis.
Citation: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
Mots-clés: chimie click, administration ciblée de médicaments, pro-médicaments, microenvironnement tumoral, anesthésie photo‑contrôlée