Clear Sky Science · fr
Synthèse électrochimique sélective d’urée à partir de nitrate et de dioxyde de carbone avec un faible surtension
Transformer les déchets en engrais
L’agriculture moderne dépend largement de l’engrais urée, mais sa fabrication traditionnelle consomme beaucoup de combustibles fossiles et émet d’importantes quantités de dioxyde de carbone. Cette étude explore une voie plus propre : utiliser l’électricité et des matériaux spécialement conçus pour convertir directement le dioxyde de carbone et le nitrate — deux polluants courants — en urée dans des conditions douces. À l’échelle industrielle, un tel procédé pourrait aider à nourrir les populations tout en réduisant les émissions de gaz à effet de serre et en valorisant mieux les flux de déchets.
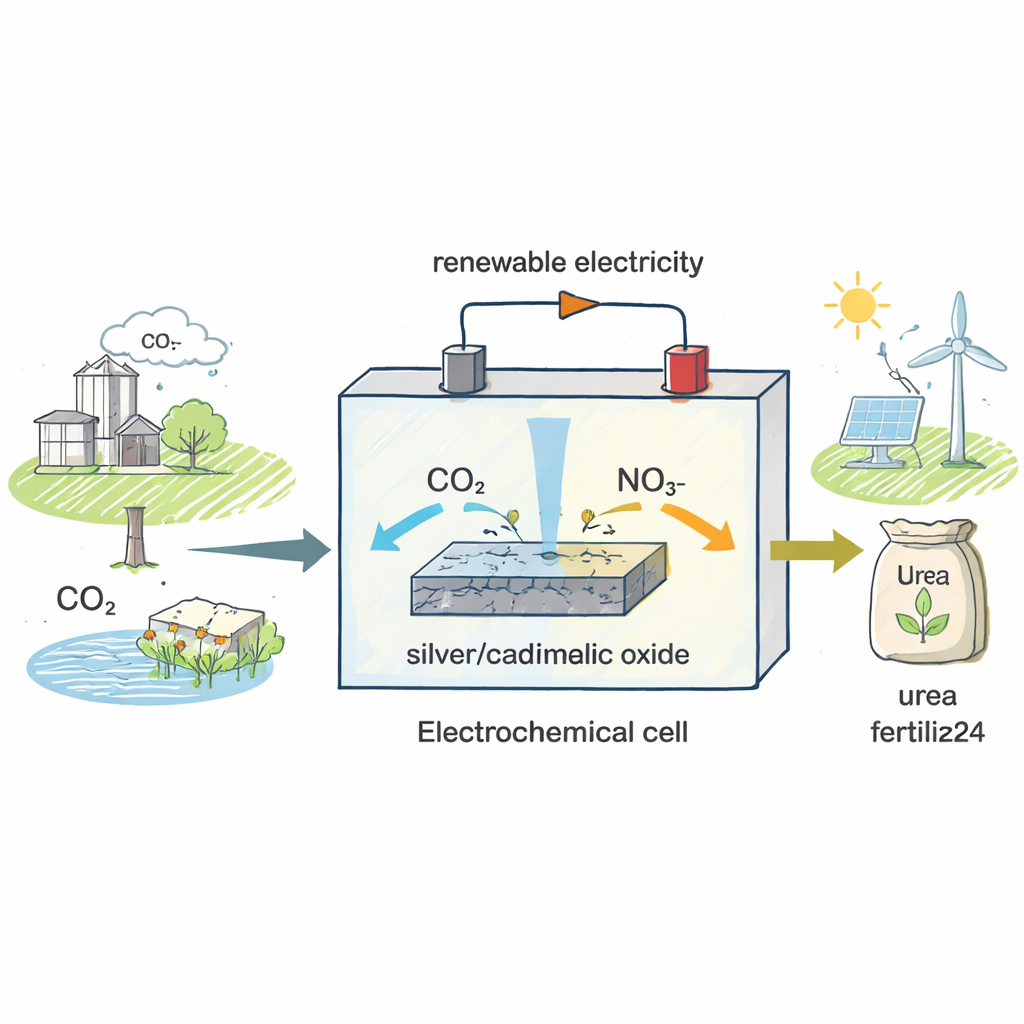
Une nouvelle manière de produire un engrais ancien
Les usines d’urée actuelles fonctionnent à haute température et pression et reposent sur la production préalable d’ammoniac à partir de l’azote atmosphérique, une étape qui à elle seule consomme plus de 2 % de l’énergie mondiale. Les auteurs cherchent à contourner cette filière énergivore. Plutôt que de partir de l’azote gazeux, ils utilisent le nitrate, un composé azoté présent dans les rejets agricoles et les eaux industrielles, et le combinent avec le dioxyde de carbone, principal gaz à effet de serre. Ces deux substances sont alimentées dans une cellule électrochimique — un dispositif où l’électricité pilote des réactions chimiques — de sorte que, avec le bon catalyseur, elles puissent être assemblées en urée à température ambiante et sous des tensions relativement faibles.
Concevoir une surface utile
Le cœur de l’appareil est un catalyseur solide constitué de nanoparticules combinant argent (Ag) et oxyde de cadmium (CdO). La microscopie et les techniques aux rayons X montrent que ces particules forment des « hétérostructures » intimes, où l’argent métallique et le CdO sont en contact à l’échelle nanométrique et échangent des électrons. Cette interaction électronique modifie subtilement la manière dont chaque composant adsorbe les molécules entrantes. En conditions opératoires, la partie CdO se transforme en carbonate de cadmium (CdCO₃) contenant des lacunes d’oxygène. Ces sites vacants jouent le rôle de petites stations d’amarrage qui aident à capter et activer le dioxyde de carbone, tandis que les régions argentées voisines sont particulièrement efficaces pour attirer les espèces azotées issues du nitrate.
Produire de l’urée efficacement et de façon sélective
Lorsque le dioxyde de carbone et le nitrate traversent ce catalyseur Ag/CdO dans une cellule de laboratoire, le matériau les convertit en urée à une « surtension » exceptionnellement faible, c’est‑à‑dire que le supplément de tension par rapport à l’exigence thermodynamique idéale est réduit. Dans une cellule en H simple, la composition optimisée, appelée Ag₀.₀₇/CdO, atteint une sélectivité pour l’urée d’environ 50 % à seulement −0,10 volt par rapport à une référence standard, et produit peu d’ammoniac ou de monoxyde de carbone comme sous‑produits. Dans une cellule à flux plus avancée, où les gaz et liquides sont fournis en continu, ce même catalyseur atteint un taux de production d’urée élevé d’environ 112 millimoles par gramme de catalyseur et par heure à −0,15 volt. En optimisant encore la conception du réacteur et les conditions opératoires, l’équipe pousse le taux de production à environ 427 millimoles par gramme et par heure à des courants plus élevés, tout en maintenant les performances pendant 1 000 heures d’opération continue — un indicateur important de stabilité.
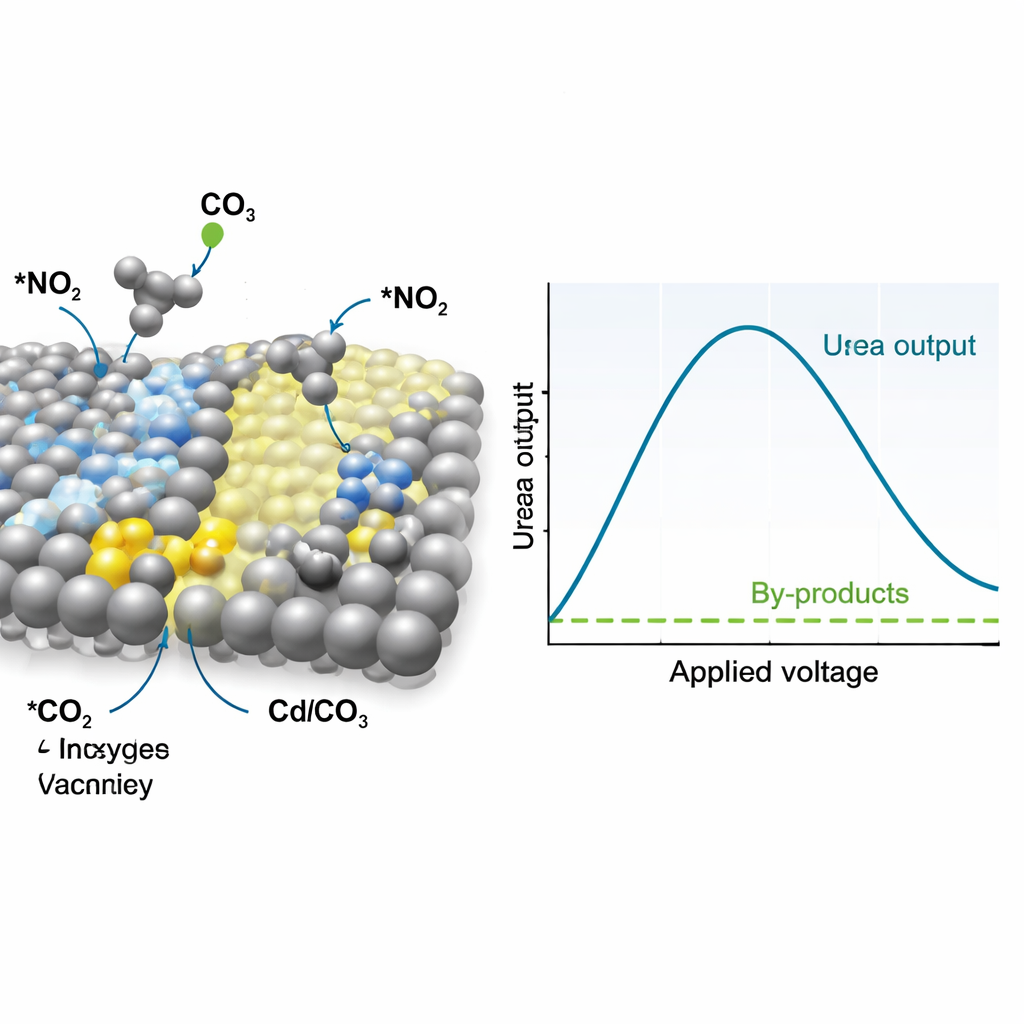
Comment le catalyseur oriente la réaction
Pour comprendre pourquoi ce matériau fonctionne si bien, les chercheurs ont suivi en temps réel le catalyseur et les intermédiaires réactionnels à l’aide de spectroscopies Raman et infrarouge, ainsi que de sondes X avancées. Ces mesures indiquent que les sites argentés convertissent préférentiellement le nitrate en un intermédiaire réactif souvent noté *NO₂, tandis que le CdCO₃ reconstruit, riche en lacunes d’oxygène, fixe le dioxyde de carbone et le transforme en *CO, un autre intermédiaire de courte durée de vie. Des signaux associés à des liaisons carbone–azote apparaissent aux tensions d’exploitation, montrant que *NO₂ et *CO se couplent tôt dans le processus pour former une espèce de type urée plutôt que de se détourner vers la formation séparée d’ammoniac ou de monoxyde de carbone. Des simulations informatiques étayent ce tableau, révélant que l’interface entre l’argent et le CdCO₃ riche en lacunes abaisse la barrière énergétique de cette étape clé de couplage C–N et la rend plus favorable que les réactions concurrentes.
Ce que cela pourrait signifier pour les engrais et le climat
Dans l’ensemble, ce travail montre que des surfaces catalytiques finement conçues peuvent guider des molécules de déchets simples comme le dioxyde de carbone et le nitrate le long d’une voie économe en énergie vers l’urée, dans des conditions douces et avec une longue durée de fonctionnement. Pour un non‑spécialiste, l’essentiel est que l’équipe a construit une sorte de « filtre électronique » qui favorise l’assemblage du carbone et de l’azote en urée plutôt que leur échappée sous forme d’autres produits. Si un déploiement à grande échelle nécessitera de traiter des questions telles que le coût des matériaux, l’ingénierie des réacteurs et la gestion sécurisée du cadmium, l’étude fournit un plan pour une production future d’engrais pouvant être alimentée par de l’électricité renouvelable et mieux intégrée à des cycles durables du carbone et de l’azote.
Citation: Liu, S., Wang, T., Liu, J. et al. Selective electrosynthesis of urea from nitrate and carbon dioxide with low overpotential. Nat Commun 17, 1787 (2026). https://doi.org/10.1038/s41467-026-68497-y
Mots-clés: synthèse électrochimique d’urée, valorisation du dioxyde de carbone, réduction du nitrate, conception d’électrocatalyseur, engrais vert