Clear Sky Science · fr
Identification de peptides antimicrobiens à partir de microbiomes intestinaux anciens
Fouille de pistes anciennes pour combattre les microbes modernes
Alors que la résistance aux antibiotiques augmente dans le monde, les médecins manquent de solutions pour traiter les infections dangereuses. Cette étude adopte une approche inhabituelle : elle ne se tourne pas vers des laboratoires de chimie de pointe, mais vers les restes fossilisés d’excréments humains — des « capsules temporelles » intestinales anciennes — pour découvrir des molécules naturelles anti‑microbes qui pourraient encore fonctionner contre les bactéries d’aujourd’hui.
Les microbes anciens, armoires à pharmacie cachées
Bien avant la médecine moderne, l’intestin humain était déjà un champ de bataille où microbes bienveillants et germes envahisseurs se disputaient l’espace et les nutriments. Nombre de bactéries intestinales bénéfiques produisent des peptides antimicrobiens — de courts fragments protéiques qui perforent les cellules bactériennes ou les neutralisent autrement. Les recherches actuelles ont principalement exploré les microbiomes contemporains pour ces peptides. Mais nos communautés intestinales modernes ont évolué sous l’influence des antibiotiques et des modes de vie actuels, offrant de nombreuses occasions aux bactéries nuisibles de développer des résistances. En revanche, les communautés intestinales anciennes, préservées dans des fèces desséchées appelées coprolithes, se sont formées dans un monde sans antibiotiques sur ordonnance. Cela en fait une source prometteuse de défenses « oubliées » que les pathogènes modernes n’auraient pas encore apprises à contourner.
Un outil IA léger pour lire l’ADN fossile
Pour explorer cette pharmacie ancienne, les chercheurs ont développé un nouvel outil informatique nommé AMPLiT (AMP Lightweight Identification Tool). Plutôt que de nécessiter de puissants supercalculateurs, AMPLiT fonctionne efficacement sur un ordinateur portable ordinaire tout en conservant une grande précision. Il parcourt d’énormes jeux de données d’ADN issus d’échantillons de microbiome et repère de courtes séquences susceptibles de coder des peptides antimicrobiens. L’équipe a affiné la conception d’AMPLiT pour qu’il puisse traiter des millions de fragments provenant d’ADN endommagé vieux de plusieurs siècles en quelques heures, réduisant le temps d’entraînement d’environ 80 % par rapport aux méthodes antérieures, tout en conservant une performance proche de l’état de l’art pour détecter des candidats susceptibles de tuer les germes.
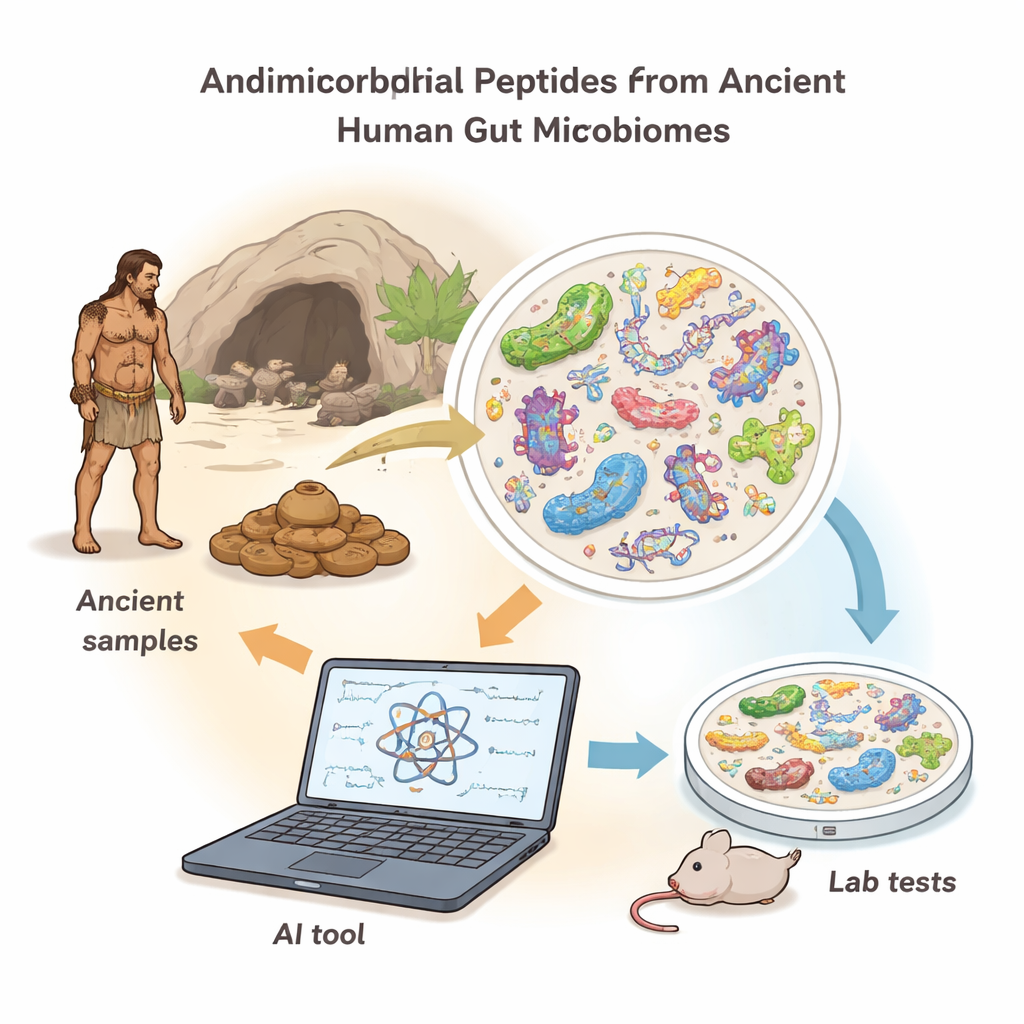
Ressusciter des tueurs de microbes d’un habitant intestinal ancien
Avec AMPLiT, les scientifiques ont examiné l’ADN intestinal de sept humains anciens ayant vécu il y a 1 000 à 2 000 ans en Amérique du Nord. Après avoir éliminé la contamination environnementale et ciblé des longueurs de peptides courtes et pratiques, l’outil a prédit des centaines de milliers de séquences antimicrobiennes potentielles. Une série de filtres plus stricts — présence chez plusieurs individus, propriétés chimiques et faible toxicité prédite — a réduit ce lot à 41 candidats de haute confiance, dont 40 pouvaient être synthétisés chimiquement en laboratoire. Testés contre des bactéries « Gram‑positives » et « Gram‑négatives » (deux grands groupes comprenant de nombreux pathogènes courants), 36 des 40 peptides ont ralenti ou arrêté la croissance bactérienne à des doses relativement faibles, un taux de réussite exceptionnel pour ce type de découverte.
L’étoile surprenante : un allié intestinal en voie de disparition
Environ deux tiers des peptides les plus actifs provenaient d’une seule bactérie intestinale : Segatella copri, proche parente d’un microbe autrefois classé sous Prevotella copri. Cette espèce était abondante dans les intestins anciens et reste courante chez les personnes ayant des régimes plus traditionnels et moins industrialisés, mais elle est désormais rare dans de nombreuses populations urbaines de style occidental. En retraçant l’emplacement des gènes de peptides dans le génome de Segatella, l’équipe a découvert que la plupart sont en fait des fragments de gènes « ménagers » plus grands que le microbe semble avoir réutilisés comme armes — une astuce évolutive efficace. Beaucoup de ces peptides anciens diffèrent nettement de ceux des bases de données modernes, ce qui suggère qu’ils représentent des conceptions chimiques véritablement nouvelles, et non de simples variations d’antibiotiques connus.
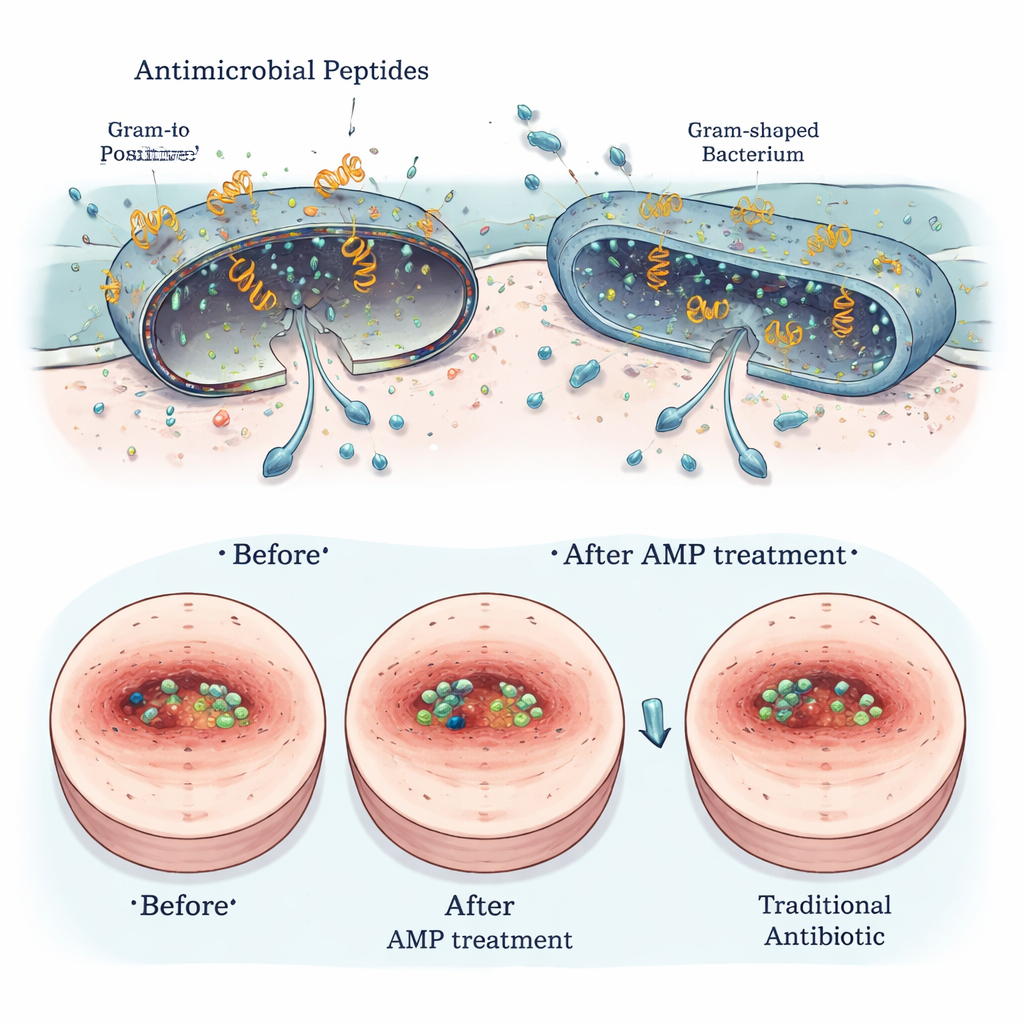
Sûrs pour l’hôte, durs pour les microbes — et prometteurs pour les plaies
Plusieurs des peptides Segatella les plus prometteurs ont été testés pour la sécurité et l’utilité in vivo. En culture, ils ont causé peu ou pas de dégâts aux globules rouges et n’ont eu que des effets légers, si présents, sur des cellules semblables à celles de l’intestin humain. La microscopie à haute résolution a montré que les peptides perturbaient physiquement les membranes externes des bactéries nuisibles, tout en épargnant les cellules animales. Dans des modèles de plaies infectées chez des rongeurs, des peptides sélectionnés appliqués sur la peau ont réduit la charge bactérienne, accéléré la cicatrisation et atténué les signes d’inflammation, avec des performances comparables à des antibiotiques établis tels que la vancomycine et la polymyxine B, en particulier contre des bactéries Gram‑positives comme Staphylococcus aureus.
Ce que cela signifie pour les médicaments futurs
Pour le non‑spécialiste, le message est simple : les microbes intestinaux de nos ancêtres pourraient contenir des plans pour de nouveaux antibiotiques encore efficaces contre les infections difficiles à traiter aujourd’hui. Cette étude montre qu’avec des outils d’IA intelligents et efficaces comme AMPLiT, les scientifiques peuvent exploiter l’ADN ancien pour identifier des peptides antimicrobiens à la fois puissants et relativement respectueux des cellules humaines. Même si de nombreuses étapes restent à franchir avant que l’une de ces molécules devienne un médicament, le travail suggère que ressusciter des partenaires microbiens « perdus » comme Segatella copri — ou du moins s’approprier leurs armes moléculaires — pourrait aider à reconstituer notre arsenal face aux bactéries résistantes en augmentation.
Citation: Chen, S., Yuan, Y., Wang, Y. et al. Identification of antimicrobial peptides from ancient gut microbiomes. Nat Commun 17, 1788 (2026). https://doi.org/10.1038/s41467-026-68495-0
Mots-clés: peptides antimicrobiens, microbiome ancien, Segatella copri, résistance aux antibiotiques, extraction métagénomique