Clear Sky Science · fr
Cibler la cascade UFL1-AKT supprime la progression du cancer du sein triple négatif
Pourquoi cette recherche compte
Le cancer du sein triple négatif (CSTN) est l’une des formes les plus mortelles du cancer du sein car il est dépourvu des récepteurs hormonaux et des récepteurs de facteurs de croissance ciblés par de nombreux médicaments modernes. Les patientes reçoivent souvent seulement une chimiothérapie traditionnelle, qui peut cesser d’être efficace lorsque les tumeurs développent des résistances. Cette étude met au jour un « moteur » moléculaire jusque-là caché qui aide les cellules de CSTN à croître et à résister à la chimiothérapie, et propose un nouveau type de médicament qui bloque directement ce moteur.
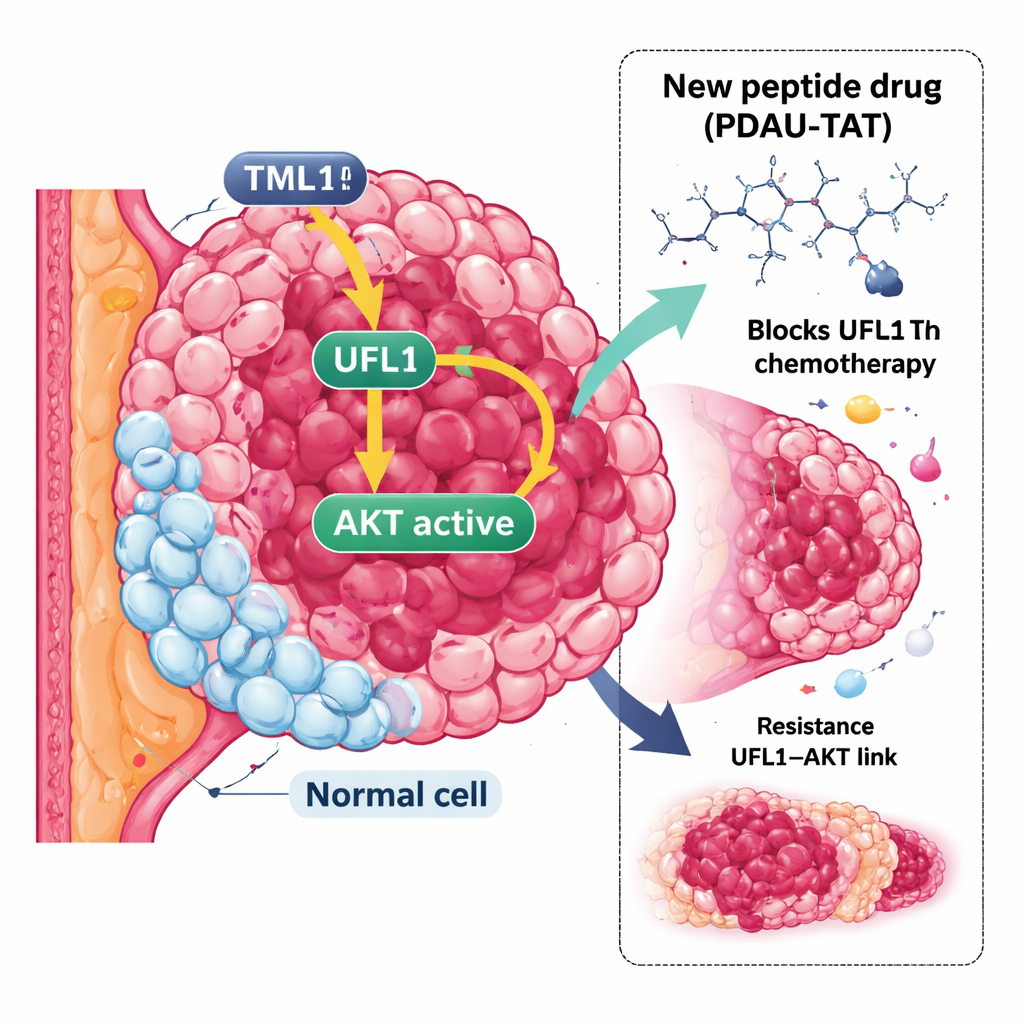
Une forme tenace de cancer du sein
Le CSTN se définit par l’absence de trois marqueurs courants : le récepteur aux œstrogènes, le récepteur à la progestérone et le récepteur de croissance HER2. En l’absence de ces marqueurs, de nombreuses thérapies ciblées efficaces ne s’appliquent tout simplement pas. Des médicaments classiques comme le cisplatine et la doxorubicine sont donc utilisés, mais les tumeurs de CSTN résistent souvent ou s’adaptent rapidement à ces traitements et sont plus susceptibles de métastaser. Cela crée un besoin urgent de stratégies nouvelles qui dépassent les cibles habituelles et recherchent d’autres points faibles dans les systèmes de contrôle tumoraux.
Une protéine peu connue mais très influente
Les chercheurs se sont intéressés à UFL1, une protéine qui ajoute une petite étiquette, appelée UFM1, sur d’autres protéines dans un processus nommé UFMylation. Ce système d’étiquetage n’a été découvert que récemment, et son rôle dans le cancer était encore flou et parfois contradictoire. En analysant des données de patientes et des échantillons tumoraux, l’équipe a montré que UFL1 est nettement surexprimé dans le CSTN par rapport au tissu mammaire normal. Lorsque les chercheurs ont réduit les niveaux de UFL1 dans des lignées cellulaires de CSTN et dans des modèles tumoraux murins, les cellules cancéreuses ont proliféré plus lentement et sont devenues beaucoup plus sensibles à la chimiothérapie, suggérant que UFL1 favorise la tumeur dans ce contexte.
Relier UFL1 à un commutateur maître de la croissance
En creusant davantage, les scientifiques ont découvert que UFL1 se lie directement à AKT, une protéine de signalisation centrale qui pilote la croissance cellulaire, la survie et le métabolisme, et qui est souvent hyperactive dans les cancers. Dans le CSTN, AKT est fréquemment trop actif même en l’absence des mutations en amont habituelles. L’équipe a constaté que UFL1 étiquette chimiquement AKT en trois positions spécifiques, ce qui facilite ensuite l’activation d’AKT par ses partenaires activateurs tout en le protégeant des enzymes qui l’éteindraient normalement. Les cellules dépourvues de UFL1 ou exprimant une forme d’AKT modifiée ne pouvant pas recevoir ces étiquettes présentaient une activité AKT beaucoup plus faible, une croissance ralentie et une plus grande vulnérabilité à la chimiothérapie, tant en cultures cellulaires que dans des modèles animaux.
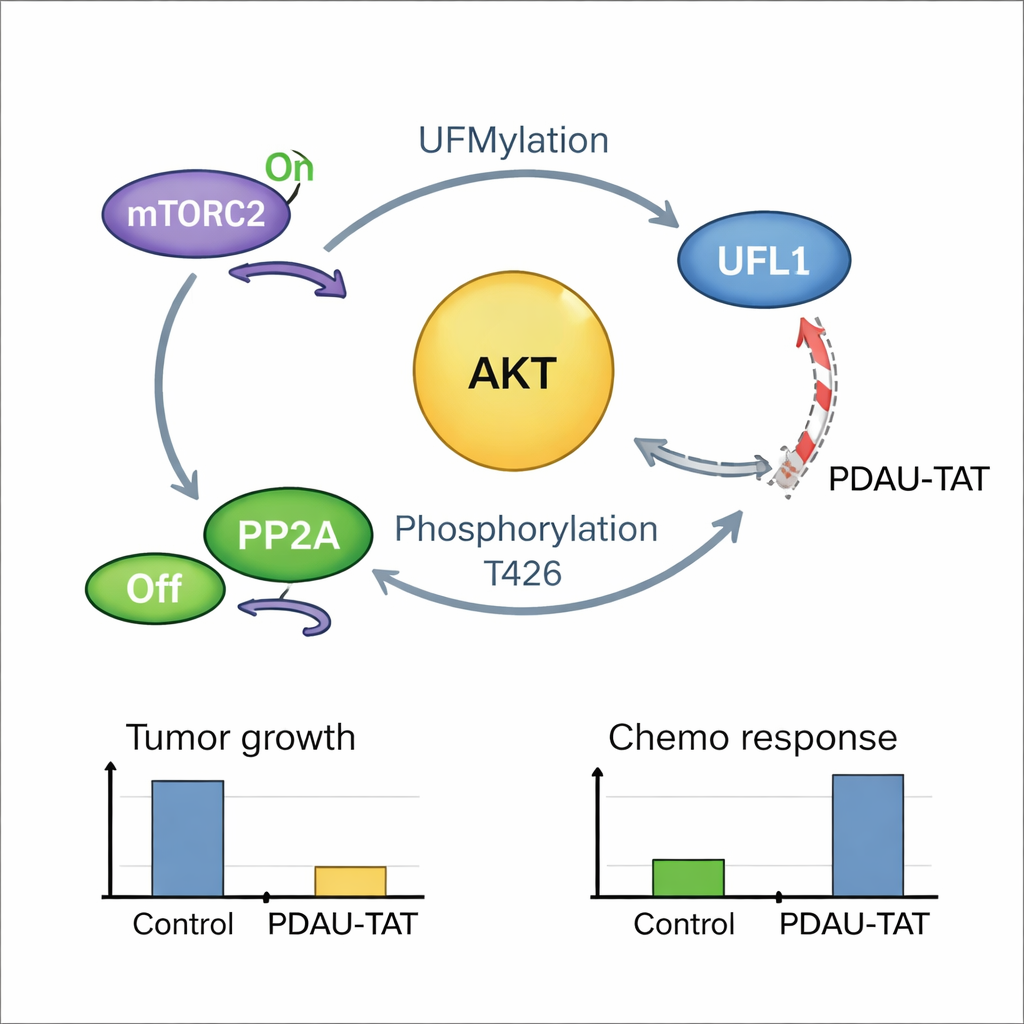
Une boucle tumorale auto‑entretenue et un moyen de la briser
L’histoire s’est révélée encore plus liée : une fois activé, AKT rétroagit et modifie UFL1 en un site crucial, renforçant l’activité d’étiquetage de UFL1 sur AKT et d’autres cibles. Cela crée une boucle de rétroaction positive où UFL1 active AKT, et AKT actif, à son tour, suralimente UFL1. Les échantillons tumoraux de patientes montraient que des niveaux élevés d’UFL1 modifié corrèlent fortement avec des niveaux élevés d’AKT actif, ce qui soutient l’existence de cette boucle dans la maladie humaine. Pour exploiter cette vulnérabilité, l’équipe a conçu un court peptide pénétrant les cellules, nommé PDAU‑TAT, qui imite une petite région de UFL1 et se glisse entre UFL1 et AKT. Ce peptide perturbe leur interaction, réduit l’activation d’AKT, ralentit la croissance tumorale et rend les cellules de CSTN et les tumeurs dérivées de patientes plus sensibles à la chimiothérapie, sans dommages apparents aux organes majeurs chez la souris.
Ce que cela pourrait signifier pour les patientes
En termes simples, les chercheurs ont mis au jour un schéma de câblage caché à l’intérieur des cellules de CSTN : UFL1 et AKT sont verrouillés dans une boucle d’amplification qui maintient les signaux de croissance en position « marche » et aide les tumeurs à résister aux traitements. En développant un petit peptide qui s’insère dans cette boucle et déconnecte UFL1 d’AKT, ils montrent une manière plausible d’affaiblir les tumeurs de CSTN tout en épargnant les cellules normales, qui ont tendance à avoir des niveaux plus faibles d’UFL1. Bien que ce travail soit encore au stade préclinique, il ouvre la voie à une nouvelle classe de thérapies ciblées visant non pas les récepteurs habituels mais les interactions protéine–protéine qui alimentent certains des cancers du sein les plus agressifs.
Citation: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Mots-clés: cancer du sein triple négatif, signalisation AKT, UFMylation, UFL1, thérapie peptidique anticancéreuse