Clear Sky Science · fr
La boucle de rétroaction positive UFL1-AKT favorise la progression du cancer du sein en renforçant la synthèse lipidique
Pourquoi les cellules cancéreuses tiennent tant aux lipides
Les cellules du cancer du sein, comme toutes les cellules à croissance rapide, ont besoin d’un apport constant de blocs de construction pour fabriquer de nouvelles membranes et des molécules de signalisation. Les graisses, ou lipides, constituent une part essentielle de cet approvisionnement. Cette étude révèle comment un système protéique peu connu fait basculer les cellules cancéreuses en « surproduction de lipides », aidant ainsi les tumeurs à se développer et à échapper aux traitements. Comprendre cette voie d’alimentation cachée pourrait ouvrir de nouvelles pistes pour ralentir ou affamer les cancers du sein.
Une étiquette protéique cachée aux grandes conséquences
Nos cellules ajustent en permanence le comportement de leurs protéines au moyen de petites étiquettes chimiques. L’une d’elles, appelée UFM1, est ajoutée par une enzyme nommée UFL1. L’étiquetage par UFM1 (UFMylation) a été associé à la réparation de l’ADN et aux réponses au stress, mais son rôle dans le cancer restait flou. Les auteurs montrent que UFL1 est beaucoup plus actif dans les tumeurs mammaires humaines que dans le tissu mammaire normal, et ce dans tous les principaux sous‑types. Les patientes dont les tumeurs présentent des niveaux élevés de UFL1 tendent à avoir une survie plus mauvaise. Quand les chercheurs ont réduit UFL1 dans des cellules de cancer du sein ou dans des tumeurs de souris, la croissance tumorale a ralenti, la division cellulaire a diminué et la mortalité cellulaire a augmenté, suggérant que UFL1 se comporte comme un facteur favorisant le cancer.
Comment un centre de signalisation est basculé en mode production de lipides
Pour comprendre comment UFL1 aide les tumeurs, l’équipe a recherché ses partenaires moléculaires et a identifié une protéine clé de contrôle du signal, AKT1. AKT1 est un interrupteur central qui ordonne aux cellules de croître et de synthétiser de nouveaux lipides. L’étude montre que UFL1 se lie physiquement à AKT1 et le marque par des UFM1 en plusieurs sites spécifiques. Cet étiquetage modifie la conformation d’AKT1, desserrant un « frein » interne qui le maintient normalement inactif. Il favorise aussi la relocalisation d’AKT1 vers une membrane intracellulaire, le réticulum endoplasmique, où d’autres enzymes peuvent l’activer pleinement par phosphorylation. Sans ces marques UFM1 à ces positions, AKT1 est beaucoup plus difficile à activer.
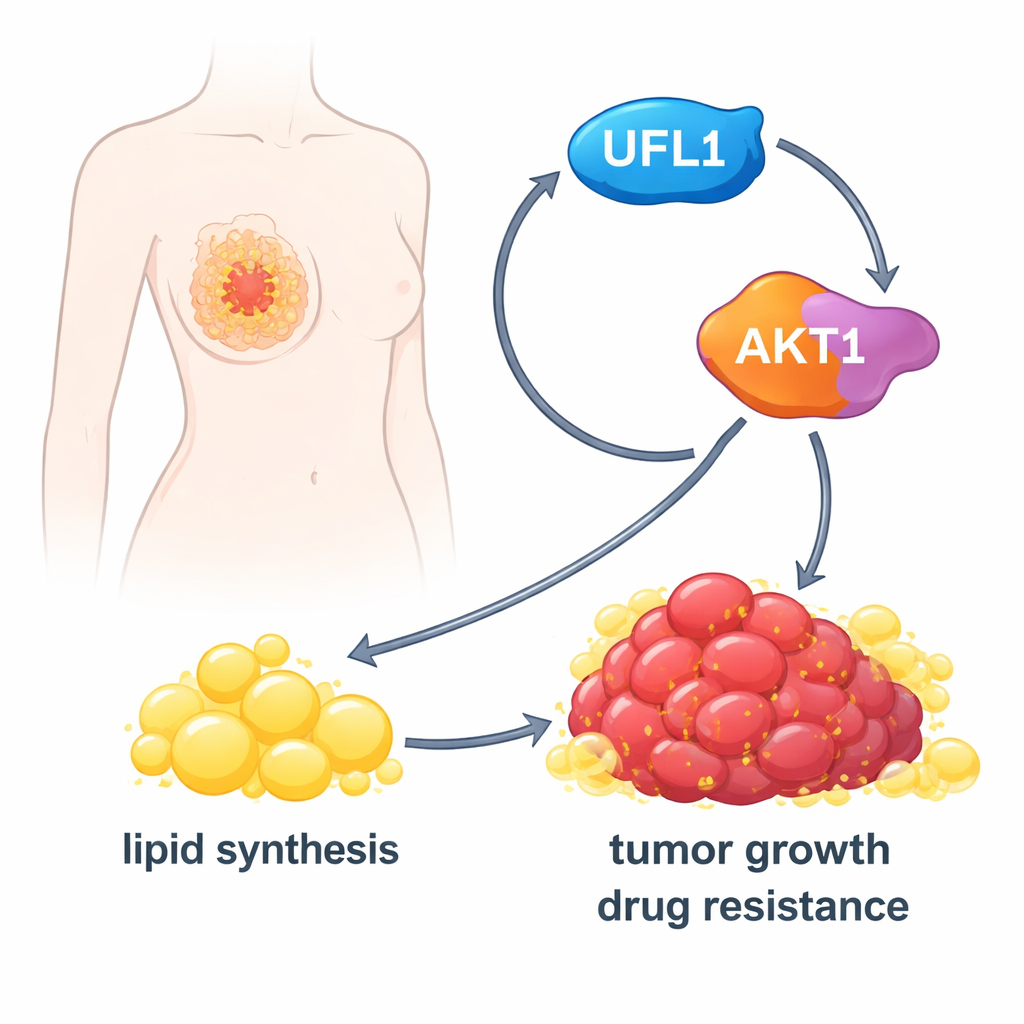
Mise en marche de l’usine à graisses du cancer
Une fois activé, AKT1 pousse les cellules à augmenter leur production de lipides. Il stimule l’activité d’une enzyme métabolique clé, ACLY, et accroît les niveaux de régulateurs maîtres comme SREBP1 qui activent de nombreux gènes de la lipogenèse. Dans des cellules de cancer du sein cultivées en laboratoire, UFL1 faisait accumuler davantage de gouttelettes lipidiques, d’acides gras libres et de cholestérol. La suppression de UFL1 réduisait fortement ces réserves lipidiques, à la fois en culture et dans des tumeurs implantées chez la souris. L’apport d’acides gras exogènes pouvait en grande partie restaurer la croissance des cellules cancéreuses déficientes en UFL1, indiquant que l’effet principal de UFL1 est d’assurer suffisamment de lipides pour soutenir l’expansion tumorale.
Une boucle auto‑amplificatrice qui alimente la croissance tumorale
De façon surprenante, la relation entre UFL1 et AKT1 est bidirectionnelle. Les chercheurs ont découvert qu’une fois AKT1 activé, il ajoute à son tour un groupe phosphate sur UFL1 à un site particulier. Cette modification renforce encore la capacité de UFL1 à marquer AKT1 par UFM1, créant une boucle de rétroaction positive : UFL1 active AKT1, et AKT1 active UFL1. La mutation des sites d’UFM1 sur AKT1 ou du site de phosphorylation sur UFL1 rompt cette boucle. Chez la souris, les tumeurs portant ces versions mutantes croissaient peu, contenaient moins de lipides et présentaient davantage de cellules en mort. Dans des échantillons de patientes atteintes d’un cancer du sein triple négatif, des niveaux élevés d’UFL1 activé et d’AKT1 activé apparaissaient souvent ensemble, soulignant que cette boucle fonctionne dans les tumeurs réelles.
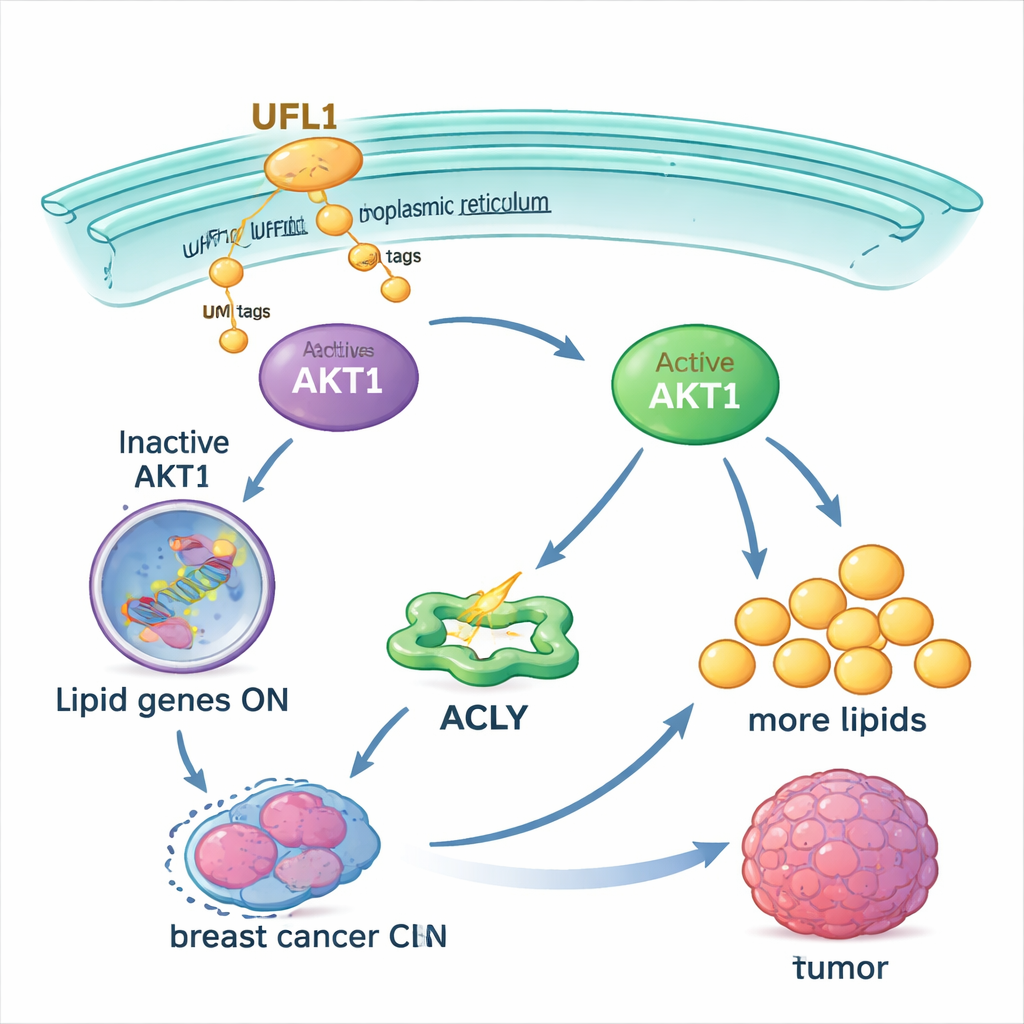
Affaiblir la boucle pour améliorer l’efficacité des traitements
Étant donné que de nombreux essais cliniques ciblent déjà AKT, les auteurs ont testé si bloquer l’UFMylation pouvait rendre ces traitements plus efficaces. Dans des cellules de cancer du sein, un petit inhibiteur moléculaire de l’UFMylation et un inhibiteur d’AKT réduisaient chacun l’activité d’AKT1 et l’accumulation lipidique, mais leur combinaison était bien plus efficace que chaque traitement seul. L’association ralentissait également la croissance tumorale et diminuait le contenu lipidique dans les tumeurs de souris sans perte de poids notable chez les animaux. Le blocage de l’UFMylation rendait en outre les cellules cancéreuses plus sensibles aux chimiothérapies standards comme le cisplatine et l’étoposide, qui échouent souvent lorsque AKT est fortement actif.
Ce que cela signifie pour les patientes
Pour un lecteur non spécialiste, l’étude montre que certains cancers du sein se câblent eux‑mêmes via une boucle auto‑renforçante qui alimente à la fois leur croissance et leur réserve lipidique. UFL1 et AKT1 agissent de concert comme deux pédales enfoncées simultanément : l’un étiquette, l’autre signale, et ensemble ils stimulent la production de lipides et l’expansion tumorale. En trouvant des médicaments qui perturbent cette boucle — en bloquant l’UFMylation, AKT1 ou leur interaction — les thérapies futures pourraient ralentir la croissance tumorale et rendre les traitements existants plus efficaces, en particulier pour les formes agressives de cancer du sein.
Citation: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Mots-clés: cancer du sein, métabolisme des lipides, signalisation AKT, UFMylation, thérapie ciblée