Clear Sky Science · fr
Hydrogel réservoir cellulaire auto-assemblé in situ pour piloter une radioimmunothérapie en plusieurs étapes
Transformer la radiation en une arme anticancéreuse plus intelligente
La radiothérapie est l’un des traitements du cancer les plus utilisés, mais les tumeurs survivent souvent en se dissimulant au système immunitaire et en se développant dans des conditions pauvres en oxygène (hypoxie) qui atténuent l’effet des radiations. Cette étude décrit un hydrogel injectable « intelligent » qui se forme directement à l’intérieur d’une tumeur et fait office de petite usine de médicaments et de générateur d’oxygène. En apportant à la tumeur à la fois la radiation et des signaux immunostimulants soigneusement synchronisés, le système vise à transformer un cancer difficile à traiter en une cible que les défenses de l’organisme peuvent reconnaître et détruire.
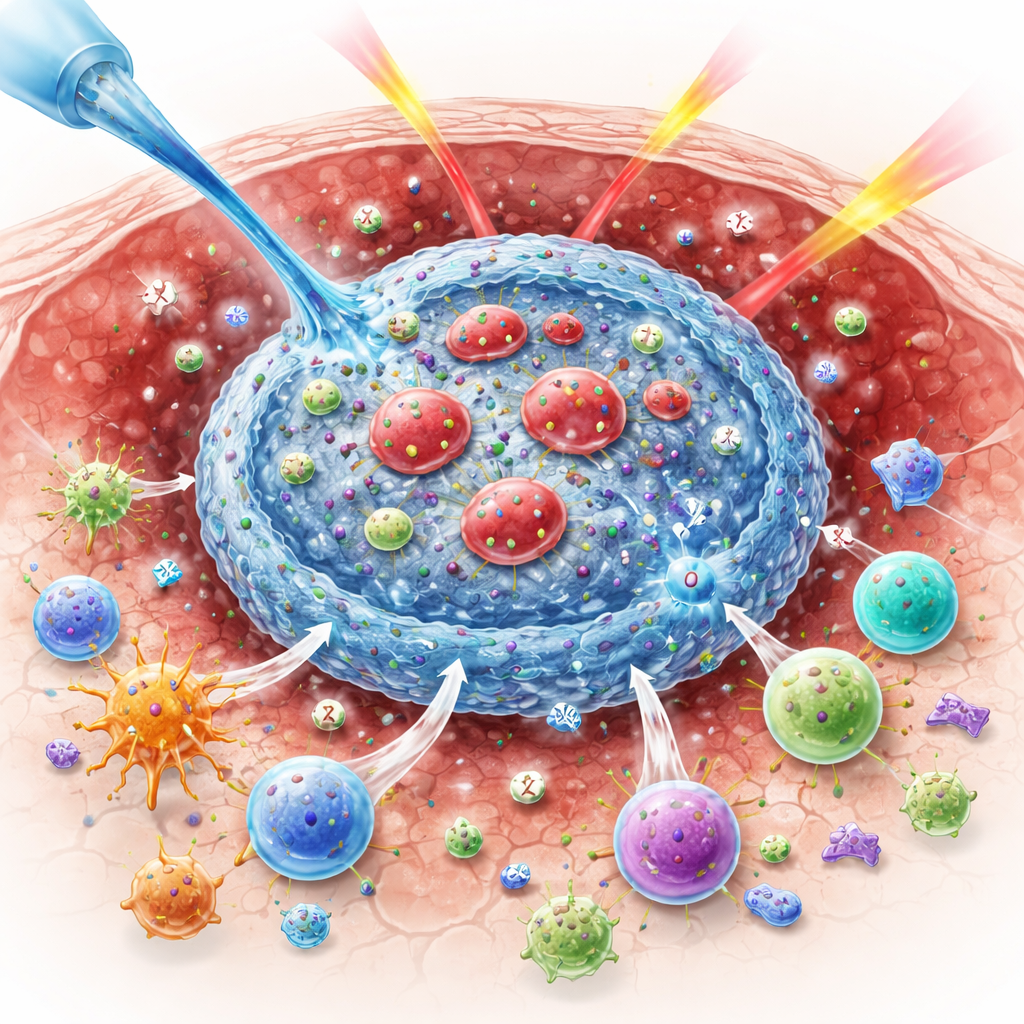
Pourquoi l’oxygène est crucial pour vaincre les tumeurs
La radiation tue les cellules cancéreuses en partie en générant des espèces d’oxygène hautement réactives qui fragmentent l’ADN. Lorsqu’une tumeur manque d’oxygène, cette chimie est moins efficace, et davantage de cellules cancéreuses survivent. Parallèlement, la radiation envoie des signaux contradictoires au système immunitaire. Elle peut exposer des protéines tumorales qui signalent le danger, mais elle peut aussi renforcer des « freins » des cellules immunitaires, tels que la protéine checkpoint CTLA-4, et favoriser les cellules T régulatrices qui suppriment l’attaque. Ces effets opposés expliquent en partie pourquoi la combinaison de radiation et de médicaments immunitaires n’a pas toujours donné des résultats aussi probants chez l’humain que chez la souris.
Un gel vivant construit à l’intérieur de la tumeur
Les chercheurs ont conçu un matériau qui s’auto-assemble uniquement dans l’environnement acide d’une tumeur. Il est composé de trois éléments clés : un polymère naturel à base de sucre appelé alginate, une poudre inorganique nommée peroxyde de baryum, et des globules rouges légèrement modifiés pour transporter deux médicaments immunitaires. Lorsque le mélange est injecté dans une tumeur, l’acidité déclenche la décomposition du peroxyde de baryum, libérant des ions baryum et du peroxyde d’hydrogène. Les ions baryum réticulent instantanément l’alginate en un hydrogel souple, emprisonnant les globules rouges modifiés et empêchant les médicaments d’être emportés. Simultanément, des enzymes naturellement présentes dans les globules rouges convertissent le peroxyde d’hydrogène en oxygène, contribuant à réduire l’hypoxie tumorale et à préparer la tumeur à une radiation plus efficace.
Libération chronométrée de deux signaux immunitaires
La véritable puissance du système tient à la manière dont il échelonne la libération de deux agents immunitaires : un anticorps qui bloque CTLA-4 et une cytokine appelée interleukine-12 (IL-12). L’anticorps est chargé à l’intérieur des globules rouges, tandis que l’IL-12 est ancrée à leur surface. À mesure que l’oxygène est produit, des pores s’ouvrent dans la membrane des globules rouges, permettant à l’anticorps anti–CTLA-4 de s’échapper rapidement. Cette libération précoce lève la suppression immunitaire, encourage les cellules dendritiques à transporter des antigènes tumoraux vers les ganglions lymphatiques voisins et aide à activer des cellules T spécifiques de la tumeur. L’IL-12, en revanche, diffuse lentement au fur et à mesure que la structure de l’hydrogel se relâche. Ce signal tardif pousse les cellules T et les cellules tueuses naturelles à produire de l’interféron-gamma, favorise le recrutement supplémentaire de cellules immunitaires cytotoxiques dans la tumeur et renforce une boucle de rétroaction positive entre sentinelles et effectrices immunitaires.
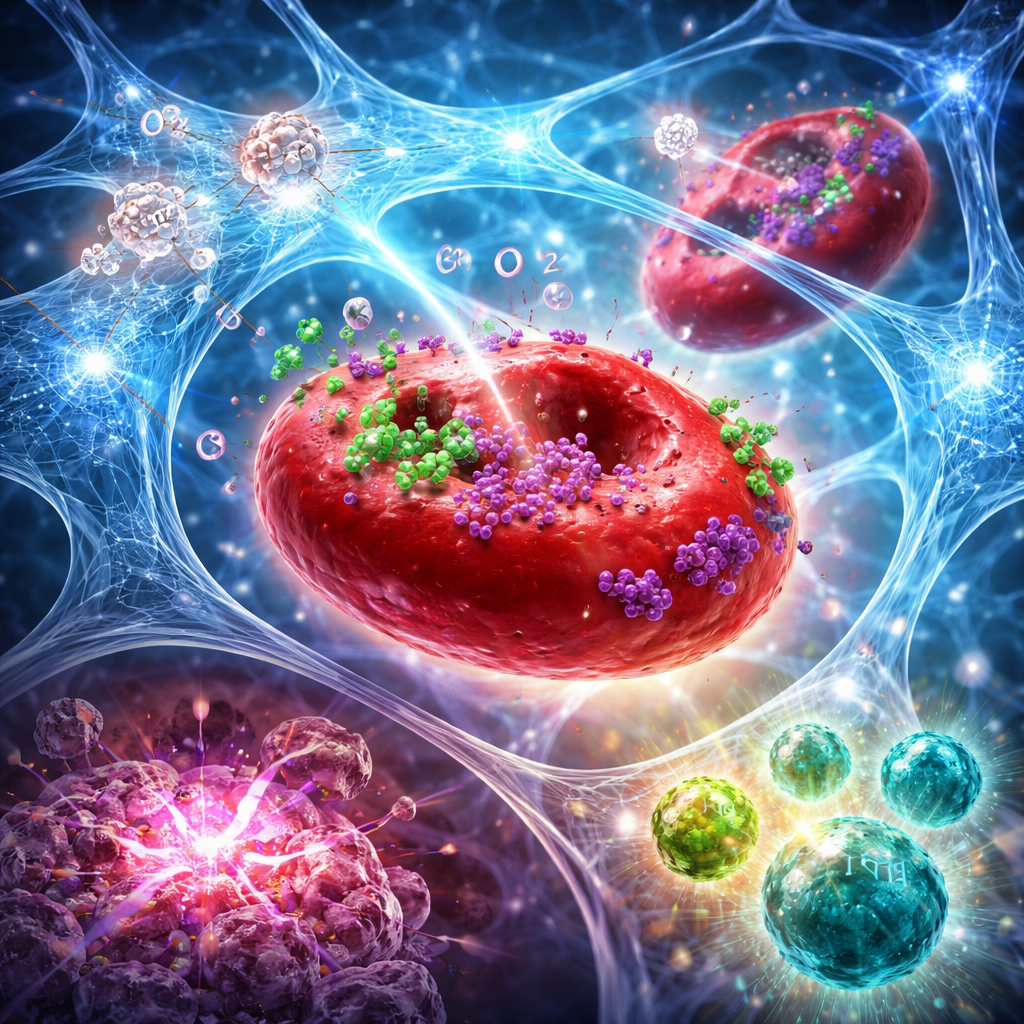
De l’injection locale à une attaque immunitaire systémique
Dans des modèles murins de cancers du sein et du pancréas agressifs, l’association de cet hydrogel à une radiation ciblée a fait plus que réduire la taille de la tumeur traitée. L’approche combinée a augmenté les niveaux d’oxygène dans les tumeurs pendant plusieurs jours, amplifié les dommages à l’ADN induits par la radiation et déclenché une forme de mort cellulaire plus propre qui signale naturellement les tumeurs pour reconnaissance immunitaire. La cytométrie en flux et les colorations tissulaires ont montré un changement marqué du microenvironnement tumoral : plus de cellules T CD8 cytotoxiques et de cellules NK, moins de cellules T régulatrices, et un rapport plus élevé de cellules « effectrices » sur « suppresseures ». Des cellules dendritiques spécialisées dans les ganglions lymphatiques ont également augmenté, indiquant une meilleure présentation d’antigènes. De nombreux souris ont présenté une régression tumorale complète, et certaines ont été protégées contre la repousse tumorale lorsque des cellules cancéreuses ont été réintroduites plusieurs semaines plus tard, suggérant la formation d’une mémoire immunitaire durable.
Sécurité, praticité et perspectives
Parce que le gel se forme localement et retient son chargement, seules de petites quantités d’IL-12 et d’anti–CTLA-4 s’échappent dans la circulation sanguine, réduisant le risque d’effets indésirables graves comme les tempêtes de cytokines ou les lésions d’organes qui ont limité l’usage de ces agents par le passé. Les composants — alginate, globules rouges et peroxyde de baryum — sont relativement peu coûteux et faciles à produire à grande échelle, laissant espérer que cette stratégie puisse être adaptée à différents cancers. Bien que des défis subsistent en matière de fabrication, de contrôle qualité et d’administration du gel aux tumeurs profondes ou disséminées, le travail illustre une voie prometteuse pour synchroniser la radiation avec une activation immunitaire précisément chronométrée, transformant un traitement physique du cancer en un puissant déclencheur d’immunité antitumorale systémique.
Ce que cela pourrait signifier pour les patients
Concrètement, cette recherche suggère que plutôt que d’administrer séparément la radiation et les médicaments immunitaires en espérant qu’ils coopèrent, on peut les emballer dans un matériau intelligent qui s’installe dans la tumeur, fabrique son propre oxygène et libère des signaux immunitaires selon une séquence soigneusement chorégraphiée. Chez les animaux, cette approche a non seulement rendu la radiation plus létale pour les cellules cancéreuses, mais a aussi entraîné le système immunitaire à reconnaître et mémoriser la tumeur, aidant à prévenir sa récidive. Si des résultats similaires peuvent être obtenus chez l’humain, de tels hydrogels pourraient un jour transformer des tumeurs difficiles à traiter en cibles que les défenses naturelles de l’organisme peuvent trouver et détruire de manière fiable.
Citation: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
Mots-clés: radioimmunothérapie, hydrogel, immunothérapie du cancer, microenvironnement tumoral, radiothérapie