Clear Sky Science · fr
Les sous-types de bradyzoïtes régissent le carrefour du développement de Toxoplasma
Stades cachés d’un parasite courant
Toxoplasma gondii est un minuscule parasite qui infecte discrètement environ une personne sur trois dans le monde, généralement sans qu’elle ne s’en aperçoive. Mais chez les personnes dont le système immunitaire est affaibli — comme les patients atteints de cancer sous chimiothérapie ou les personnes vivant avec le sida — le parasite peut sortir de son état dormant et provoquer une maladie cérébrale grave, parfois mortelle. Cette étude explore ce stade dormant pour poser une question simple mais cruciale : tous les parasites « endormis » sont-ils identiques, ou existe-t-il différents types ayant des rôles distincts ?
Pourquoi les parasites dormants comptent
Lors d’une infection de longue durée, Toxoplasma se cache à l’intérieur de bulles microscopiques résistantes dans le cerveau et les muscles, appelées kystes tissulaires. À l’intérieur de chaque kyste vivent des centaines de bradyzoïtes, la forme lente et au repos du parasite. Ces bradyzoïtes constituent le réservoir qui alimente l’infection à vie et peuvent soudainement se reconvertir en une forme à croissance rapide, les tachyzoïtes, qui endommage les tissus et se propage dans l’organisme. Comme les traitements actuels n’éliminent pas ces kystes, comprendre précisément ce qui se passe à l’intérieur est essentiel pour prévenir la réactivation chez les patients vulnérables.
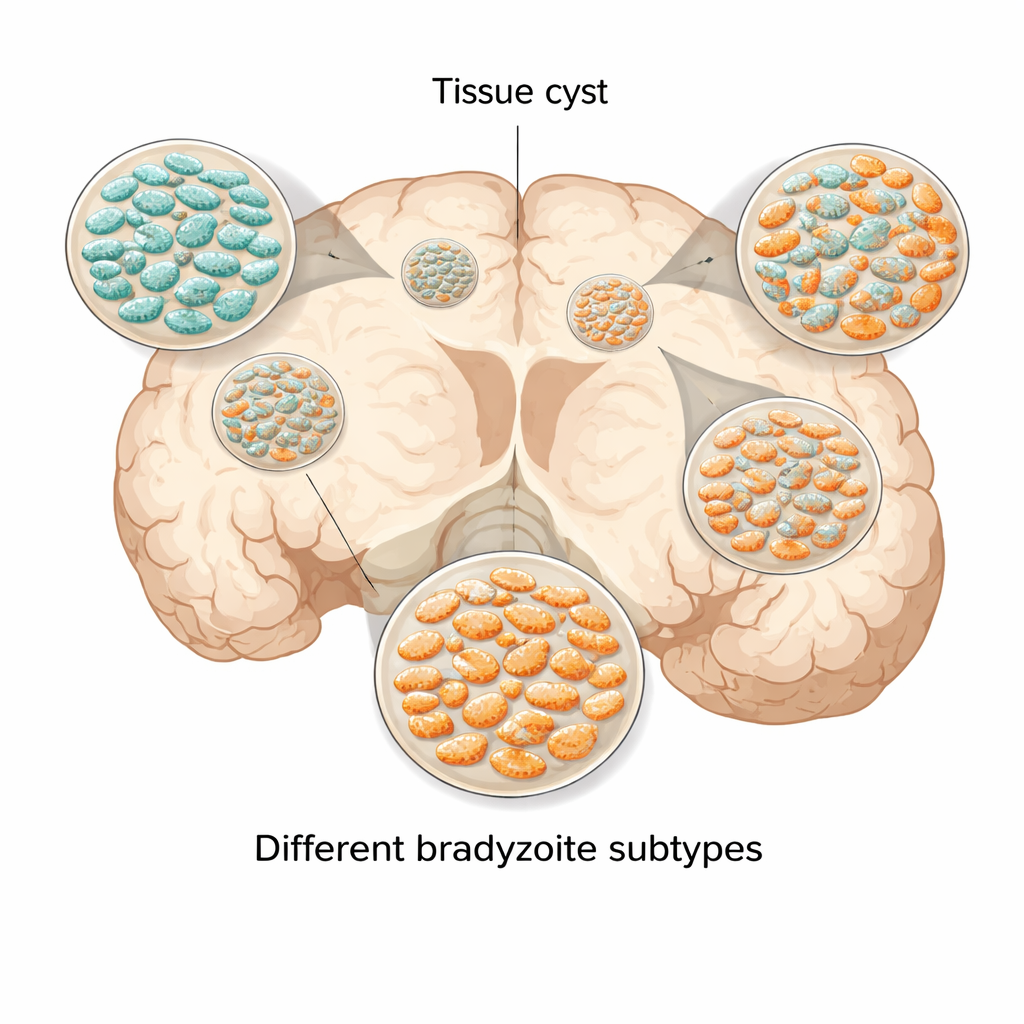
Découvrir différentes « personnalités » à l’intérieur des kystes
Les chercheurs se sont concentrés sur une molécule de surface appelée SRS22A, présente sur certains bradyzoïtes chez la souris mais étrangement absente des kystes cultivés en laboratoire standard. En utilisant des anticorps spécialement conçus comme « surligneurs » moléculaires, ils ont montré que les kystes cérébraux issus de souris infectées ne sont pas uniformes. Certains kystes sont presque entièrement peuplés de parasites positifs pour SRS22A, d’autres ne présentent pas ce marqueur, et beaucoup contiennent un mélange des deux. Ces configurations évoluent au cours de l’infection, révélant que les kystes croissent, se rompent et se reforment tout en préservant une riche diversité interne plutôt que de converger vers un état unique et mature.
Deux destins principaux : disséminer ou rester
Pour tester la portée de ces différences, l’équipe a séparé les bradyzoïtes positifs et négatifs pour SRS22A prélevés dans des cerveaux de souris et a suivi ce qui se passait lorsque chaque groupe infectait des cellules cérébrales en culture et des souris vivantes. Les parasites SRS22A-positifs se sont rapidement convertis en tachyzoïtes à forte réplication qui se sont propagés à travers les couches cellulaires et les organes des souris. Les souris infectées contenaient davantage de parasites durant la phase précoce de l’infection et ont développé beaucoup plus de kystes cérébraux par la suite. En revanche, les parasites SRS22A-négatifs avaient tendance à rester sous forme de bradyzoïtes, se multipliant lentement et construisant de nouvelles parois de kystes. Plutôt que de provoquer une dissémination explosive, ce groupe semblait orienté vers le maintien discret du réservoir à long terme.
Cinq sous-types révélés par le profilage unicellulaire
En allant plus loin, les scientifiques ont utilisé le séquençage ARN unicellulaire, une technique qui lit quels gènes sont activés dans des milliers de parasites individuels. Cela a permis d’identifier au moins cinq sous-types majeurs de bradyzoïtes à l’intérieur des kystes cérébraux chroniques, chacun avec sa propre « signature » d’activité génique. Un groupe, enrichi en SRS22A et d’autres marqueurs généralement observés au stade félin du parasite, pourrait être prêt à relancer la reproduction sexuelle lorsqu’un chat mange une proie infectée. D’autres groupes activaient des gènes liés aux outils d’invasion ou à la construction de la paroi du kyste, suggérant que certains parasites se préparent à sortir et envahir de nouvelles cellules, tandis que d’autres renforcent la coque protectrice autour de la communauté.
Repenser un cycle de vie trop simple
Pris ensemble, ces résultats renversent l’image simple des manuels selon laquelle Toxoplasma passe lentement du tachyzoïte rapide à un unique stade stable de bradyzoïte « au repos ». Au contraire, chaque kyste ressemble davantage à un petit village hétérogène de spécialistes : certains parasites sont prêts à exploser et à se répandre, d’autres à approfondir l’infection chronique en construisant de nouveaux kystes, et d’autres encore peuvent se préparer au passage vers un hôte félin. Cette complexité explique pourquoi les modèles de laboratoire qui ne produisent qu’une partie de ces types peuvent manquer des comportements clés observés dans les infections réelles, et pourquoi les médicaments ciblant un seul stade échouent souvent à guérir la maladie.
Ce que cela signifie pour les patients
Pour les personnes porteuses d’une infection à Toxoplasma, le message de l’étude est que les parasites « endormis » dans leurs tissus ne sont pas tous identiques. Certains sous-types semblent être les véritables moteurs des poussées dangereuses, tandis que d’autres maintiennent une infection silencieuse et chronique ou préparent le parasite à la transmission vers de nouveaux hôtes. En identifiant des marqueurs de surface tels que SRS22A et des profils géniques distinctifs, les chercheurs disposent désormais d’une feuille de route pour concevoir de meilleurs modèles de laboratoire, vaccins et médicaments ciblant spécifiquement les formes les plus susceptibles de causer des maladies graves. À terme, cela pourrait conduire à des thérapies qui non seulement contrôlent les symptômes, mais empêchent aussi le parasite de se réveiller.
Citation: Ulu, A., Srivastava, S., Kachour, N. et al. Bradyzoite subtypes rule the crossroads of Toxoplasma development. Nat Commun 17, 1783 (2026). https://doi.org/10.1038/s41467-026-68489-y
Mots-clés: Toxoplasma gondii, bradyzoïte, kyste tissulaire, réactivation parasitaire, séquençage ARN unicellulaire