Clear Sky Science · fr
Multistabilité continûment réglable dans des réseaux de réplication de l’ADN
Des interrupteurs simples à de nombreux états possibles
Les systèmes biologiques, des cellules en division aux embryons en développement, ne fonctionnent rarement comme de simples interrupteurs allumés ou éteints. Ils conservent souvent de nombreux états durables, à la manière d’un variateur qui peut s’arrêter à une infinité de positions. Cet article présente un réseau chimique à base d’ADN qui se comporte davantage comme ce variateur : il peut maintenir de façon stable non pas seulement quelques états distincts, mais essentiellement n’importe quelle composition le long d’un continuum. Cette capacité pourrait servir de base puissante pour des matériaux intelligents futurs, des mémoires moléculaires et des ordinateurs biochimiques traitant de l’information analogique, et non seulement numérique.
Pourquoi plusieurs états stables comptent
Beaucoup de décisions cellulaires — qu’un cellule souche se différencie, qu’une cellule s’autodétruise, ou qu’un réseau génique se souvienne d’un signal passé — reposent sur la « multistabilité », la capacité à rester dans plus d’un motif d’activité stable sous les mêmes conditions. Les versions synthétiques traditionnelles de tels systèmes ont été construites à partir de circuits géniques, d’enzymes ou de brins d’ADN qui s’activent ou s’inhibent mutuellement. Ces conceptions produisent généralement une poignée de résultats discrets, comme les commutateurs bistables classiques à deux états durables. Étendre cette idée est difficile : un système à N états peut nécessiter de l’ordre de N×(N−1) liaisons inhibitrices finement réglées, et le système ne saute toujours que parmi un petit ensemble de points fixes plutôt que de former un continuum lisse de possibilités.
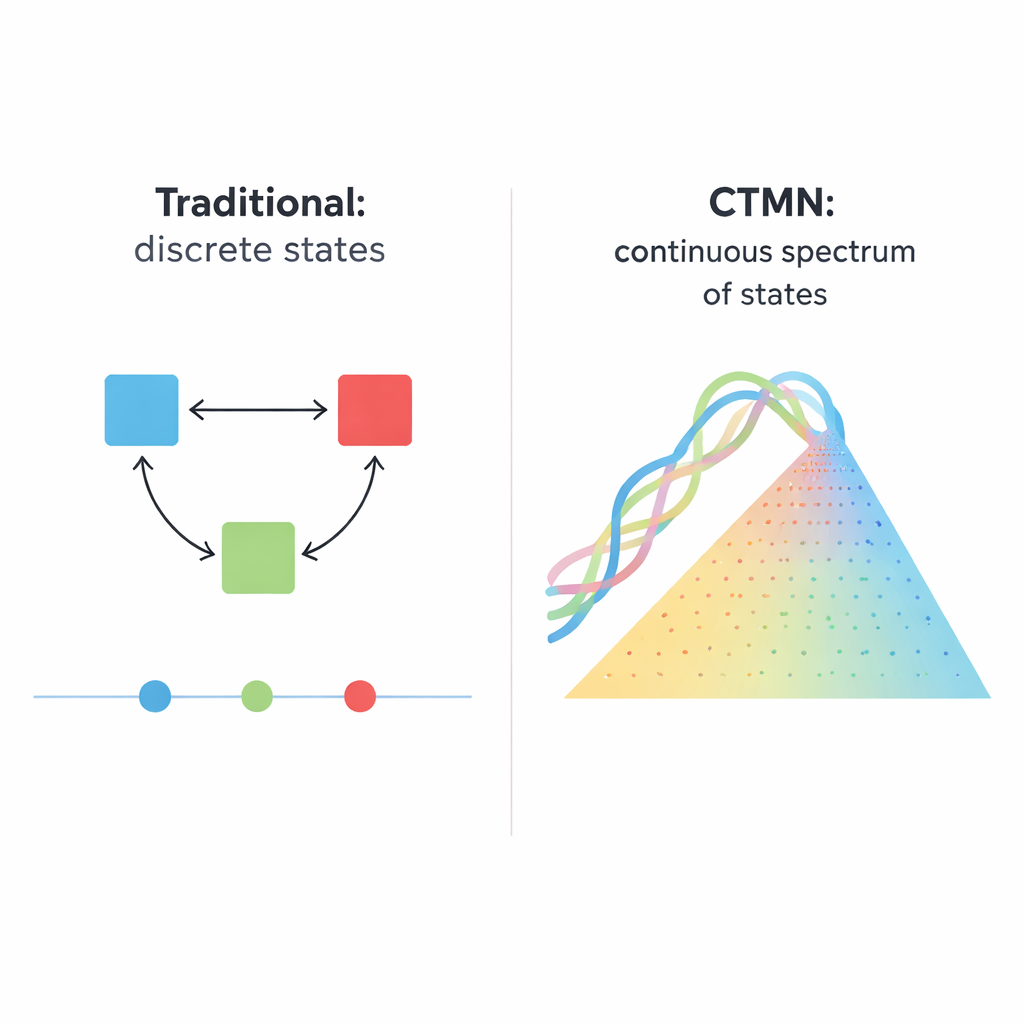
Un nouveau type de réseau d’ADN : continûment réglable
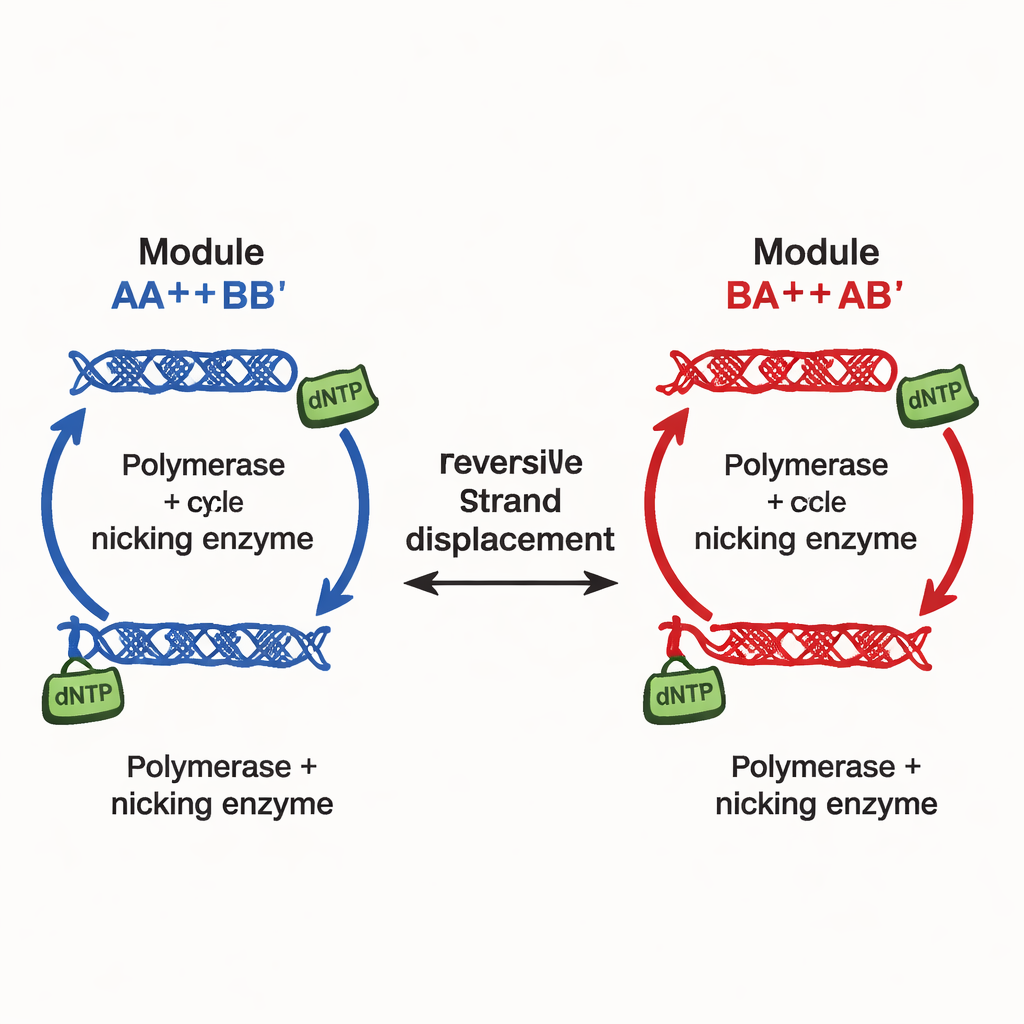
Les auteurs introduisent un principe de conception différent, mis en œuvre dans ce qu’ils appellent des réseaux de multistabilité continûment réglable (CTMN pour continuously tunable multistability networks). Plutôt que de s’appuyer sur de nombreux signaux inhibiteurs séparés, ils utilisent la compétition directe entre modules de réplication d’ADN reliés par des réactions d’échange de brins réversibles. Chaque module est constitué de duplexes d’ADN conçus qui peuvent à la fois participer à des déplacements de brins et servir de modèles pour une ADN polymérase, aidée par une enzyme nickase qui coupe et régénère des segments clés. Le carburant chimique — des nucléotides appelés dNTP — alimente la polymérisation et le nickage continus, maintenant le système loin de l’équilibre. Dans ces conditions, les modules en compétition se « figent » efficacement dans les proportions relatives dans lesquelles ils ont été lancés, produisant non seulement deux ou trois résultats mais une ligne continue entière (ou, pour plus de modules, un plan) d’états durables.
Comment la machinerie moléculaire verrouille la mémoire
Dans leur réseau à deux modules le plus simple, CTMN‑1, l’équipe montre expérimentalement et par des modélisations cinétiques détaillées que le système peut se stabiliser dans une famille de mélanges stables couvrant presque toute l’étendue allant de « principalement module A » à « principalement module B ». La polymérisation convertit des duplex actifs en formes étendues temporairement retirées de la compétition d’échange de brins ; le nicking les restaure ensuite, fermant une boucle autorégulatrice. Lorsque les deux modules partagent cette boucle, ils suppriment l’interconversion mutuelle si fortement que le système reste verrouillé près de sa composition initiale pendant de nombreuses heures, tant que du carburant est disponible. L’analyse de stabilité linéaire des équations sous‑jacentes révèle une variété entière — effectivement un continuum — d’états stationnaires, en contraste avec le point fixe unique observé lorsque les enzymes ou le carburant sont retirés.
Réponses programmables et mémoire moléculaire
Puisque l’état du réseau est stocké dans des compositions d’ADN, il peut être orienté et lu de manière programmable. Les auteurs conçoivent de courts « déclencheurs » en ARN qui se lient temporairement à des brins d’ADN spécifiques, biaisant la compétition et déplaçant le réseau vers une nouvelle composition. Même après que l’ARN est dégradé par une enzyme, le nouvel état persiste, fonctionnant comme une forme de mémoire moléculaire. Des stimuli répétés ou plus forts poussent le système de façon continue le long du continuum d’états plutôt que de le basculer entre positions simples marche/arrêt. De plus, les produits de réplication d’ADN eux‑mêmes peuvent être personnalisés pour agir comme signaux pour des processus en aval : dans les démonstrations, différents états de CTMN‑1 activent sélectivement l’un de deux catalyseurs à base d’ADN ou orientent la transcription d’ARN vers l’un de deux brins messagers, sans perturber la multistabilité sous‑jacente.
Monter en puissance vers des « variateurs » moléculaires complexes
Pour montrer que cette stratégie est évolutive, les chercheurs construisent un réseau à trois modules, CTMN‑2, en ajoutant davantage de duplex d’ADN conçus qui partagent un domaine d’échange commun mais codent des modèles de réplication différents. Les états stationnaires possibles remplissent désormais une région bidimensionnelle, comme des points à travers un diagramme de phase triangulaire, plutôt qu’une simple ligne. Là encore, les expériences confirment que de nombreuses compositions distinctes sont stables tant que carburant et enzymes sont présents, et que tout s’effondre vers un point d’équilibre unique lorsque l’apport d’énergie est coupé. Parce que l’ajout de nouveaux modules ne requiert que de nouvelles constructions d’ADN s’insérant dans le même cadre de déplacement de brins, le câblage global n’explose pas en complexité comme dans les conceptions traditionnelles.
Ce que cela signifie pour les technologies moléculaires futures
Pour un non‑spécialiste, le message central est que les auteurs ont transformé un réseau de réplication d’ADN en un dispositif mémoire analogique hautement flexible. Plutôt que de choisir parmi quelques options prédéfinies, leur système peut tenir de manière fiable l’un des dizaines d’états expérimentalement distinguables, chacun défini par la quantité relative de chaque module d’ADN présent, et convertir des impulsions chimiques transitoires en décalages durables le long de ce continuum. Comme les brins d’ADN produits sont programmables et découplés du mécanisme de stabilisation, le même cadre pourrait, en principe, réguler une large gamme de réactions biochimiques en aval ou des propriétés de matériaux avec un contrôle fin et graduel. Ce travail ouvre ainsi la voie à des dispositifs moléculaires qui calculent, mémorisent et s’adaptent davantage comme des systèmes analogiques neuronaux ou mécaniques que comme de simples interrupteurs numériques.
Citation: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Mots-clés: multistabilité de l’ADN, mémoire moléculaire, réseaux biochimiques synthétiques, déch displacement de brins d’ADN, calcul moléculaire analogique