Clear Sky Science · fr
Prédiction robuste et interprétable des marqueurs géniques et des types cellulaires à partir de données de transcriptomique spatiale
Transformer des lames de tissu de routine en cartes moléculaires
Lorsqu’une biopsie est prélevée, les médecins voient généralement seulement ce que révèle le microscope : les formes et les motifs des cellules sur des colorations rose et violette. Pourtant, sous ces couleurs se cache un monde de gènes qui s’activent ou se désactivent, influençant la croissance d’un cancer et sa réponse au traitement. Cette étude présente STimage, un nouveau système d’intelligence artificielle (IA) qui vise à lire ce scénario moléculaire directement à partir d’images pathologiques standard, offrant potentiellement des informations plus rapides et moins coûteuses sans tests de laboratoire supplémentaires.
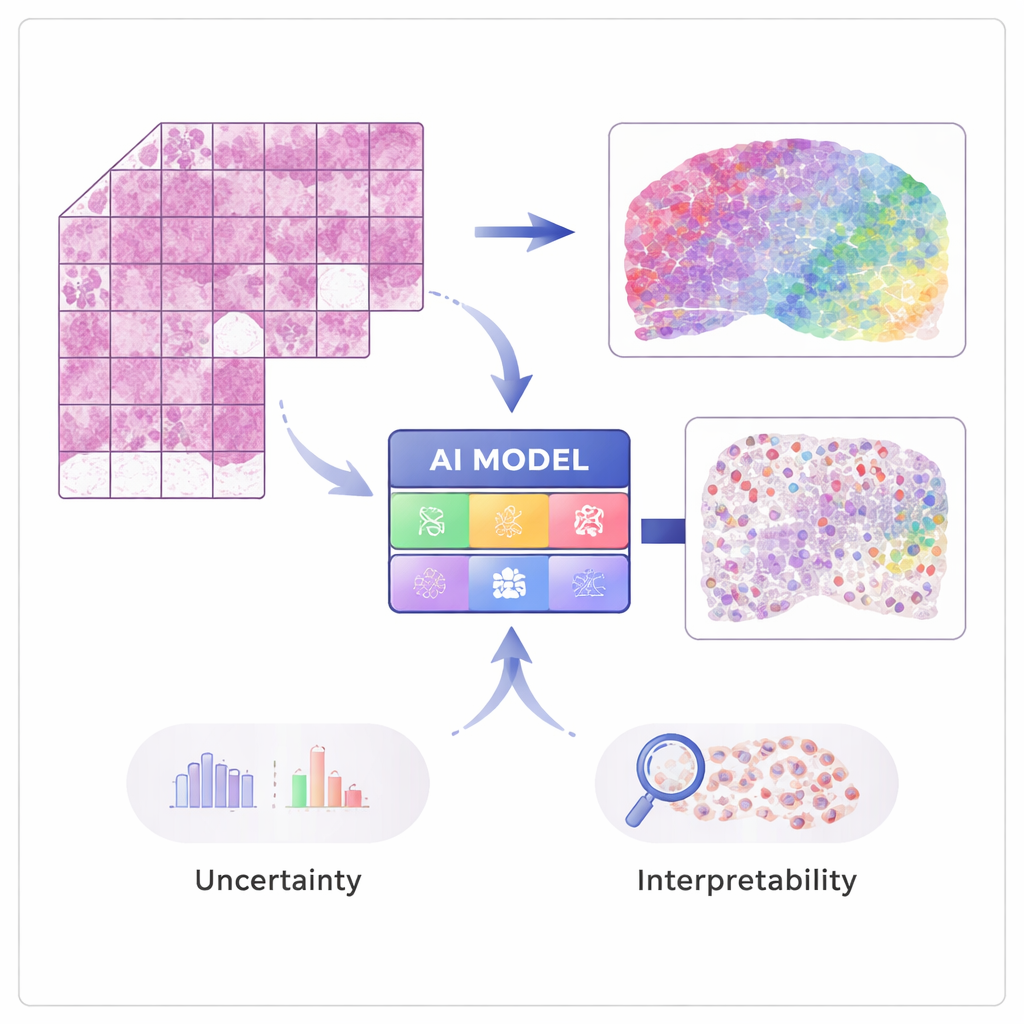
Des images à l’activité génique
Les techniques modernes de « transcriptomique spatiale » peuvent mesurer l’activité de dizaines de milliers de gènes tout en conservant l’information sur l’emplacement de chaque signal dans le tissu. Ces méthodes sont puissantes mais coûteuses et pas encore routinières dans les hôpitaux. STimage est entraîné sur un nombre modéré de jeux de données spatiales, où chaque image de tissu est associée à des mesures géniques détaillées à de nombreux petits points. L’IA apprend à associer des motifs visuels locaux sur la lame colorée à l’hématoxyline et à l’éosine (H&E) — par exemple la densité ou l’irrégularité des noyaux — à l’activité génique sous-jacente, de sorte qu’ensuite elle puisse prédire l’expression des gènes et les types cellulaires à partir d’images ordinaires uniquement.
Construire un pathologiste IA plus digne de confiance
Un objectif clé du travail n’est pas seulement la précision, mais aussi la fiabilité et l’explicabilité. Plutôt que de fournir un seul nombre pour chaque gène, STimage prédit une distribution de probabilité complète, décrivant une plage probable d’activité génique à chaque emplacement. Il sépare également deux types d’incertitude : l’une due à des données bruyantes ou variables, et l’autre reflétant le manque de connaissance du modèle lui‑même. En entraînant de nombreuses versions légèrement différentes du modèle et en les moyennant — une approche dite d’« ensemble » — les chercheurs améliorent à la fois les performances et obtiennent une vision plus claire des zones où le système est confiant et où il ne l’est pas, ce qui est crucial pour la prise de décision clinique.
Testé à travers cancers, technologies et hôpitaux
L’équipe a évalué STimage sur des jeux de données variés issus de cancers du sein, de la peau et du rein, ainsi que d’une maladie hépatique à composante immunitaire. Il a appris à prédire des marqueurs importants du cancer et de l’immunité, reproduisant souvent les véritables motifs spatiaux observés dans des expériences indépendantes. Le modèle a résisté lorsqu’on l’a mis au défi avec des données provenant de laboratoires différents, de méthodes de préparation d’échantillons variées, et même de technologies sous-jacentes différentes, y compris des plates‑formes à résolution unicellulaire et des systèmes plus anciens à plus faible résolution. Dans des comparaisons directes avec plusieurs outils IA existants, STimage et ses variantes en ensemble se sont généralement distingués, en particulier pour évaluer dans quelle mesure les motifs prédits correspondaient à la distribution réelle de l’activité génique dans le tissu.
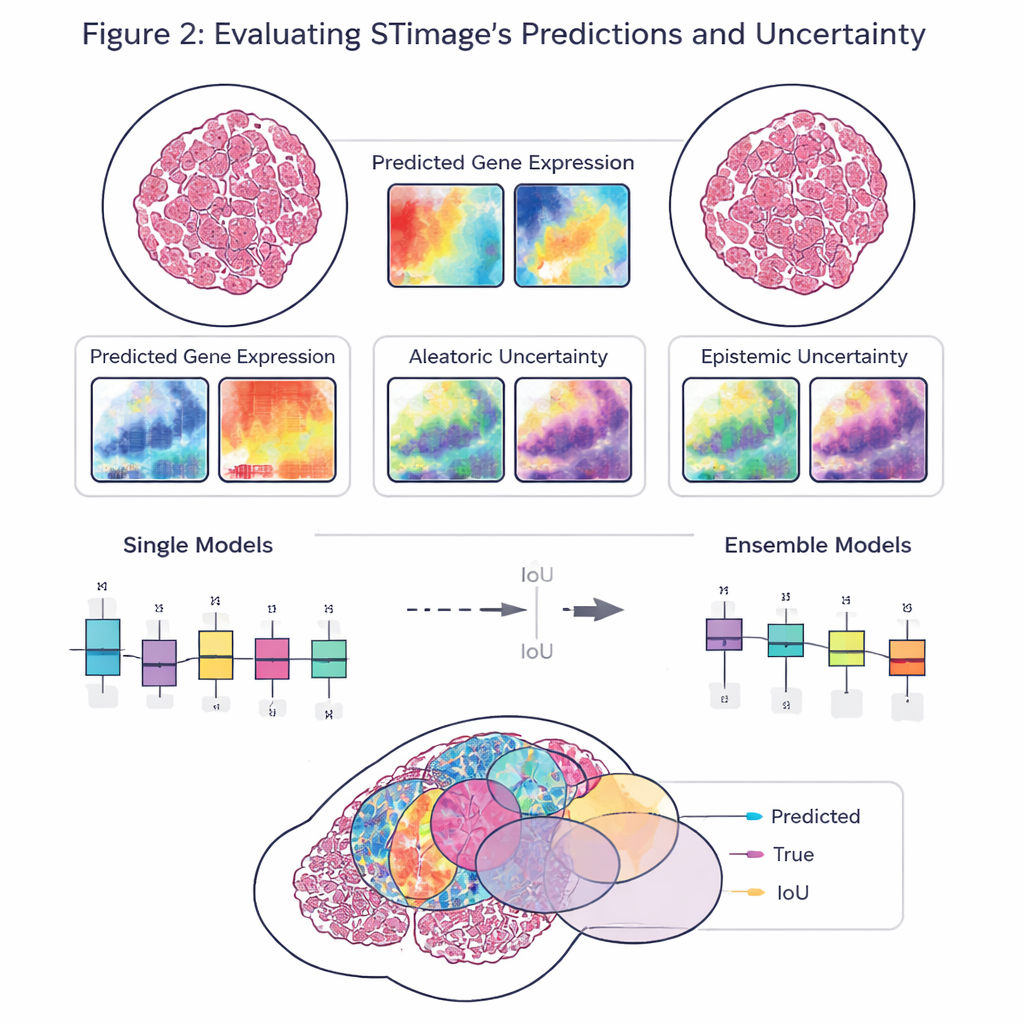
Regarder à l’intérieur des tumeurs : cellules, survie et réponse aux médicaments
STimage va au‑delà de la prédiction génique pour inférer quels types cellulaires occupent chaque région, en utilisant des jeux de données haute résolution où l’identité de chaque cellule est connue. Le modèle a pu distinguer les cellules cancéreuses des cellules immunitaires et des cellules de soutien et cartographier leur disposition sur une lame. Les auteurs ont ensuite appliqué STimage à de grandes collections d’images de cancer de routine issues du Cancer Genome Atlas. Même sans mesures spatiales, les profils géniques prédits par l’IA étaient étroitement alignés avec les données géniques en vrac réelles. Ces prédictions étaient suffisamment robustes pour regrouper les patients en catégories de risque plus élevé ou plus faible et pour aider à distinguer ceux plus susceptibles de répondre complètement à certains traitements du cancer du sein.
Pourquoi cela compte pour les patients à venir
Pour les patients et les cliniciens, la promesse de STimage est une sorte de « superposition moléculaire » sur la lame de pathologie familière. Plutôt que de commander plusieurs tests coûteux, une seule image scannée pourrait un jour révéler où des programmes géniques agressifs sont actifs, comment les cellules immunitaires sont réparties, et quels marqueurs indiquent de meilleurs ou pires pronostics ou des réponses médicamenteuses différentes. Bien que la méthode soit encore en cours d’affinement et que la corrélation avec des mesures réelles ne soit pas parfaite, sa capacité à capturer des motifs spatiaux, à estimer sa propre incertitude et à mettre en évidence quelles cellules motivent ses prédictions en fait une étape pratique vers une pathologie numérique plus informative et plus transparente.
Citation: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Mots-clés: pathologie numérique, transcriptomique spatiale, biomarqueurs du cancer, apprentissage profond, microenvironnement tumoral