Clear Sky Science · fr
PTRAMP, CSS et Ripr forment un complexe conservé nécessaire à l’invasion des érythrocytes par les mérozoïtes des espèces Plasmodium
Pourquoi cela compte pour la lutte contre le paludisme
Les parasites du paludisme doivent pénétrer nos globules rouges pour provoquer la maladie. Cette étude met au jour un petit ensemble de protéines qui forment un « pont d’embarquement » partagé par plusieurs espèces majeures de paludisme, y compris celles qui infectent l’homme. En révélant comment ce pont est assemblé et comment des anticorps peuvent parfois le bloquer, le travail ouvre des pistes pour concevoir des vaccins capables de protéger contre plus d’un type de paludisme simultanément. 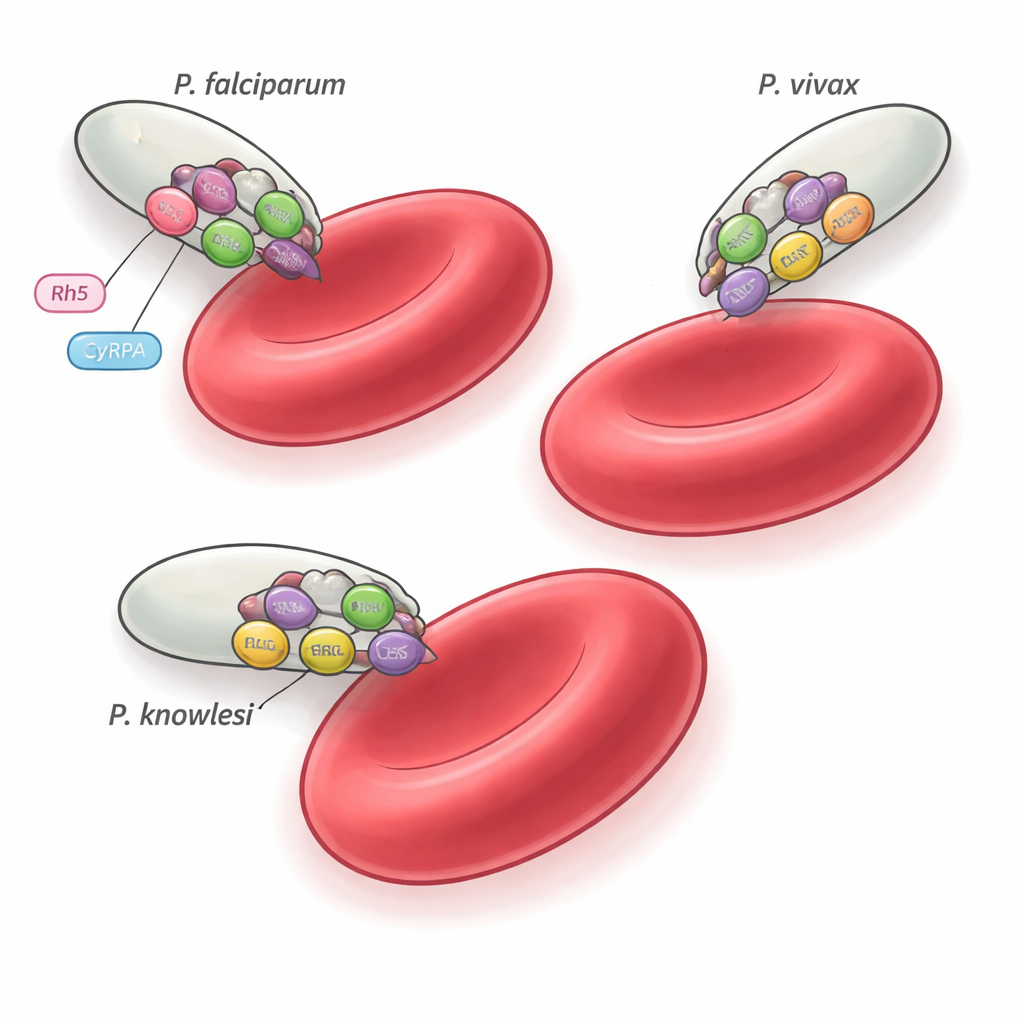
Une boîte à outils commune à de nombreux parasites du paludisme
Il existe plus de 200 espèces de Plasmodium, mais seules quelques-unes, comme P. falciparum, P. vivax et P. knowlesi, infectent l’homme. Ces espèces se situent sur des branches différentes de l’arbre phylogénétique du parasite et privilégient différents types de globules rouges, pourtant toutes doivent envahir les érythrocytes avec une grande précision. Des travaux antérieurs sur P. falciparum ont identifié un assemblage en cinq éléments, le complexe PCRCR, essentiel à l’invasion et qui se fixe sur un récepteur des globules rouges humains nommé basigine. Un des composants de ce complexe, une protéine appelée Rh5, est propre à P. falciparum et ses proches parents, ce qui pose la question : que font les autres espèces de paludisme à la place ? L’étude actuelle se concentre sur trois protéines associées — PTRAMP, CSS et Ripr — qui sont conservées dans tout le genre et teste si elles forment une machinerie d’invasion universelle.
Assembler un pont d’invasion en trois éléments
En effectuant des recherches de séquences à travers de nombreux génomes de parasites, les auteurs montrent que PTRAMP, CSS et Ripr sont présents dans toutes les grandes lignées de Plasmodium, contrairement à Rh5, qui est limité à un sous-groupe. Des prédictions de structure avec AlphaFold, combinées à des mesures biochimiques détaillées, révèlent que PTRAMP et CSS s’associent pour former une paire stable, maintenue par une liaison disulfure spécifique entre deux cystéines conservées. Cette plateforme en deux protéines s’accroche ensuite à l’extrémité C-terminale de Ripr, créant un complexe à trois éléments PTRAMP–CSS–Ripr (PCR). Des expériences avec des protéines provenant de P. falciparum, P. vivax et P. knowlesi montrent que ce complexe se forme dans ces trois espèces avec une forte affinité, et qu’une petite région à l’extrémité C-terminale de Ripr suffit pour une liaison serrée. 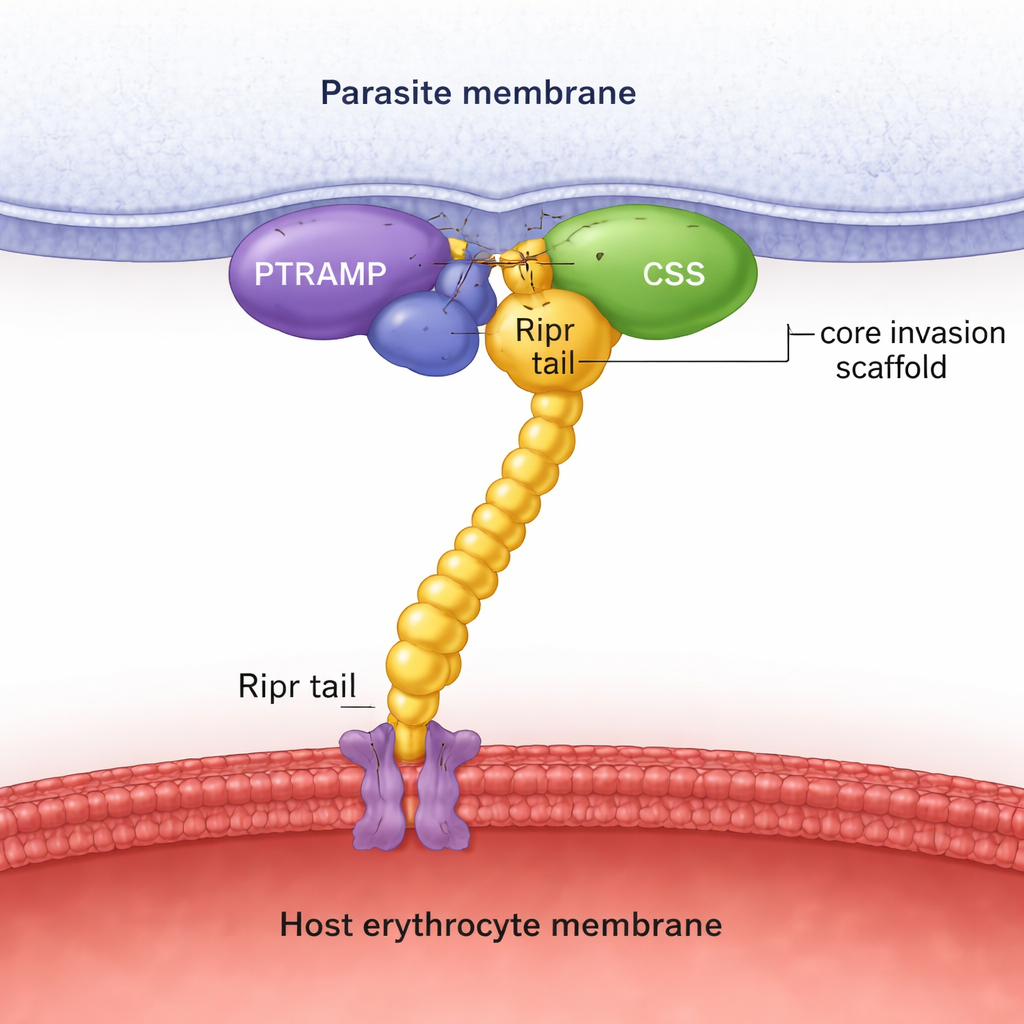
Observer la structure au niveau atomique
Pour aller au-delà des prédictions, l’équipe a résolu des structures cristallines et collecté des images en cryo‑microscopie électronique. La structure cristalline de la paire PTRAMP–CSS de P. vivax montre exactement comment un court segment de PTRAMP s’étire à travers CSS et forme la liaison disulfure clé. Une autre structure capture un anticorps puissant lié à deux domaines de type facteur de croissance de Ripr, cartographiant un épitope inhibiteur sur la queue de Ripr. L’analyse cryo‑EM du complexe PCR de P. knowlesi confirme la forme globale prédite par AlphaFold : PTRAMP et CSS se situent près de la membrane du parasite et maintiennent Ripr, dont le corps allongé s’étend en direction de la cellule hôte. Ensemble, ces instantanés structuraux appuient l’idée que le trio PCR forme un échafaudage rigide qui comble physiquement l’espace entre le parasite et le globule rouge lors de l’invasion.
Des anticorps qui reconnaissent plusieurs espèces
Parce que ces protéines sont conservées, les auteurs se sont demandé si les infections humaines génèrent naturellement des anticorps qui réagissent entre espèces. Le plasma de patients infectés par P. falciparum, P. vivax ou P. knowlesi montrait de fortes réponses anticorps contre CSS et Ripr de plusieurs espèces, suggérant que les personnes développent des anticorps dirigés contre des régions partagées du complexe PCR. L’équipe a ensuite produit des anticorps monoclonaux et des nanocorps ciblant PTRAMP, CSS et Ripr de P. vivax, et testé s’ils pouvaient bloquer la croissance du parasite en culture. Certains anticorps, en particulier un nommé 5B3 qui se lie à la queue de Ripr, ont été capables d’inhiber l’invasion par P. knowlesi et, à des concentrations plus élevées, par P. falciparum. Fait surprenant, ces mêmes anticorps n’ont pas empêché P. vivax ni le parasite de singe étroitement apparenté P. cynomolgi, même s’ils pouvaient se lier aux protéines de ces espèces.
Un échafaudage partagé avec des accessoires spécifiques à chaque espèce
Les tests fonctionnels montrent que le complexe PCR lui-même ne se fixe pas directement aux globules rouges ; il sert plutôt de structure conservée sur laquelle chaque espèce fixe ses propres partenaires de liaison aux récepteurs. Dans P. falciparum, par exemple, le trio PCR s’associe à CyRPA et Rh5 pour engager la basigine des érythrocytes humains. Dans P. vivax et P. knowlesi, les protéines de liaison au récepteur équivalentes et leurs cibles hôtes restent inconnues, mais le noyau PTRAMP–CSS–Ripr semble organiser la machinerie d’invasion. Le fait que certains anticorps puissent réagir entre espèces mais n’en inhibent que certaines met en évidence combien de petites différences dans l’assemblage du complexe et le calendrier d’action peuvent modifier la vulnérabilité à l’attaque immunitaire.
Ce que cela signifie pour les futurs vaccins contre le paludisme
Pour le non‑spécialiste, le message principal est que des parasites de paludisme très différents partagent une « prise » commune qu’ils utilisent pour entrer dans les globules rouges — composée des protéines PTRAMP, CSS et Ripr — même s’ils relient cette prise à des récepteurs différents à la surface cellulaire. Cette prise conservée est maintenant cartographiée structurellement et, dans certains cas, peut être ciblée par des anticorps agissants contre plusieurs espèces. Bien que des travaux supplémentaires soient nécessaires pour identifier l’ensemble des partenaires et améliorer les anticorps inhibiteurs, la découverte d’un échafaudage d’invasion universel ouvre la voie à des conceptions de vaccins susceptibles de protéger contre plusieurs formes de paludisme plutôt que contre une seule.
Citation: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Mots-clés: invasion du paludisme, protéines de Plasmodium, entrée des mérozoïtes, vaccin inter-espèces, infection des érythrocytes