Clear Sky Science · fr
La cryo‑tomographie électronique révèle la réplication, le bourgeonnement et la maturation couplés des flavivirus
Comment des virus infectant le cerveau détournent les membranes cellulaires
Les flavivirus, un vaste groupe viral qui comprend les agents responsables de la dengue et de l'encéphalite transmise par les tiques, peuvent pénétrer dans le cerveau et provoquer des maladies sévères. Pourtant, la manière précise dont ces minuscules agents se répliquent et assemblent de nouvelles particules virales à l'intérieur de nos cellules est restée en grande partie cachée. Cette étude utilise l'imagerie électronique 3D à très basse température pour observer des flavivirus transmis par les tiques à l'œuvre dans des cellules humaines et des tissus cérébraux de souris, révélant un couplage inattendu entre la copie du génome, l'assemblage virale et la maturation virale.
Des usines virales dissimulées dans les membranes cellulaires
Les flavivirus ne se contentent pas de flotter dans la cellule pendant qu'ils se répliquent. Ils remodèlent un système membranaire cellulaire appelé réticulum endoplasmique (RE) pour former des espaces spécialisés appelés organites de réplication. Ceux‑ci ressemblent à de minuscules bourgeons orientés vers l'intérieur à la surface du RE et servent de chambres protégées où les génomes d'ARN viral sont copiés. Grâce à la cryo‑tomographie électronique, une technique qui produit des instantanés 3D de cellules vitrifiées dans un état proche de leur conformation native, les chercheurs ont visualisé ces bourgeons dans des cellules pulmonaires humaines infectées par un flavivirus transmis par les tiques apparenté au virus de l'encéphalite. Ils ont constaté que le RE autour des régions infectées gonfle et se remplit d'amas d'organites de réplication, dont certains sont vides tandis que d'autres sont remplis d'ARN dense et filamenteux.
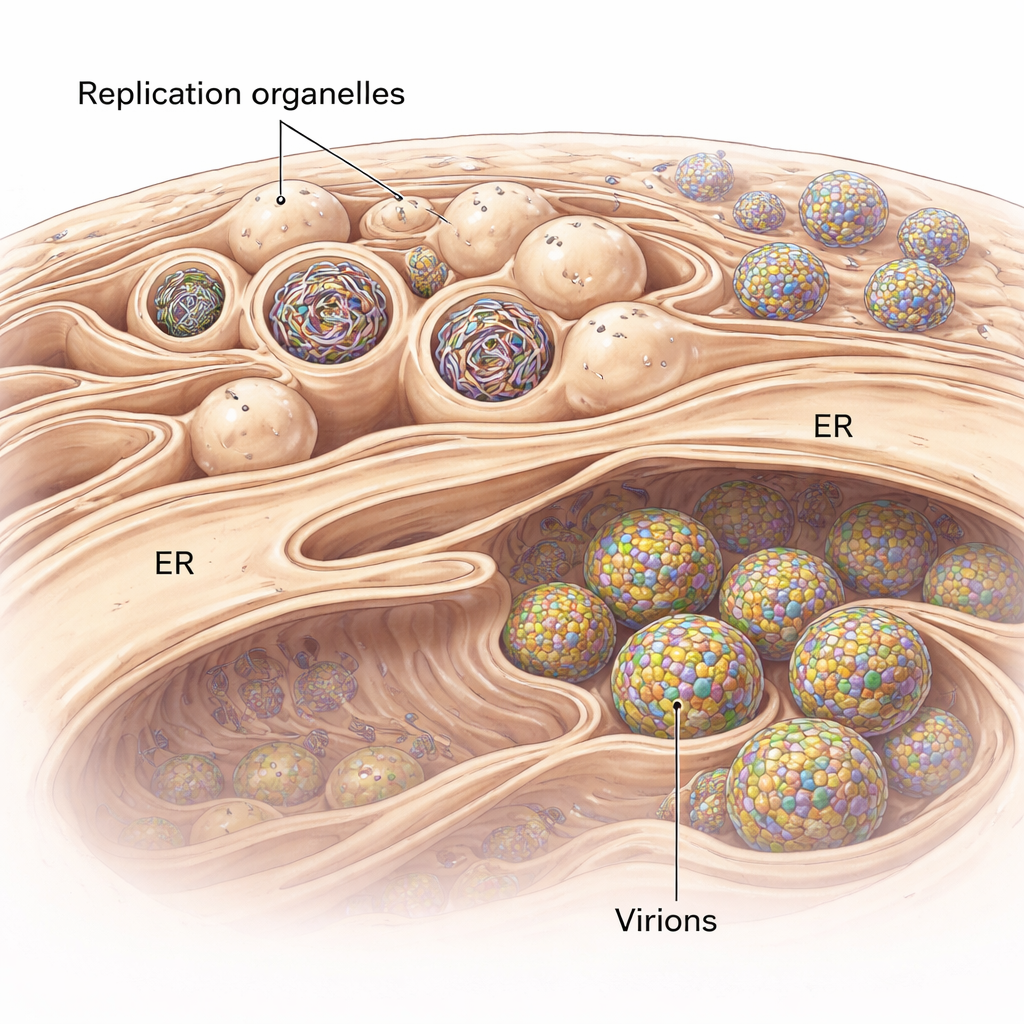
Construire la bulle virale idéale
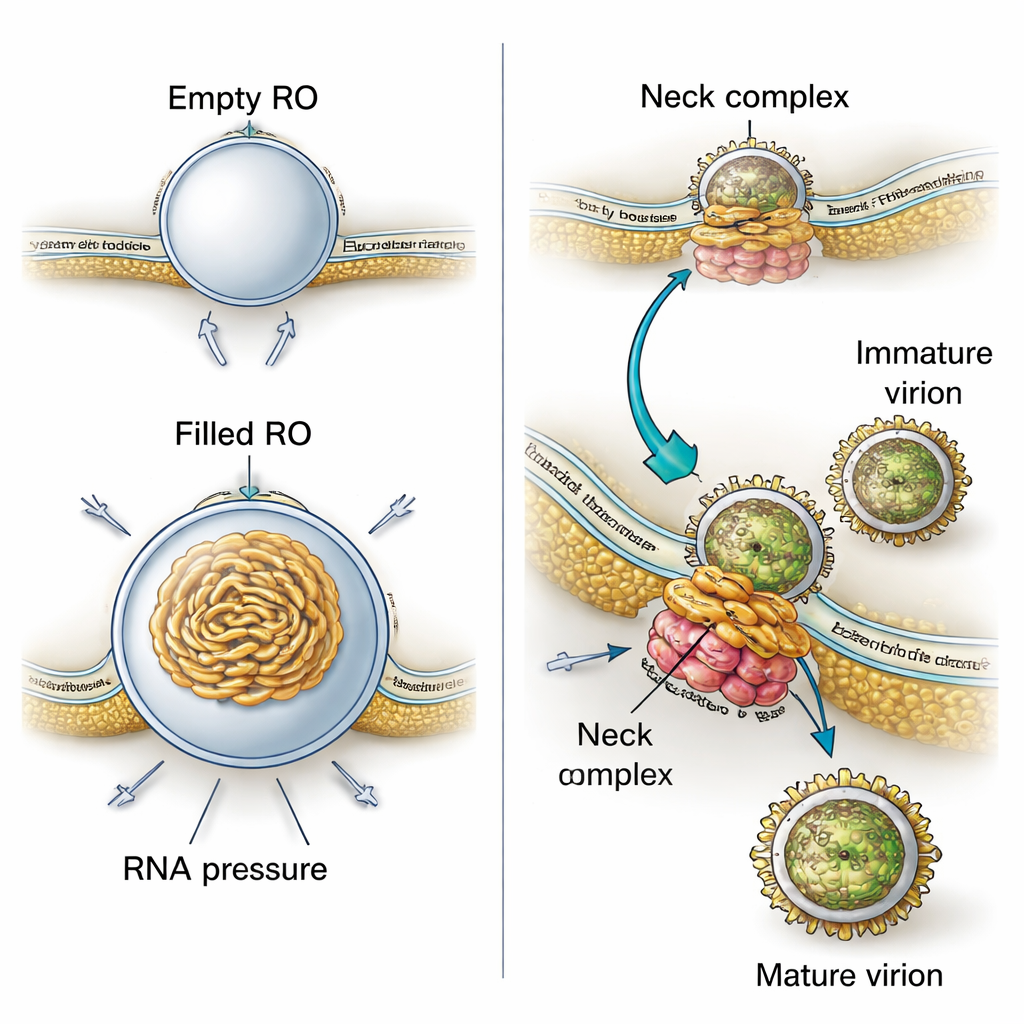
Pourquoi ces poches membranaires ont‑elles une forme si précise, en forme de bourgeon ? En combinant leurs images 3D avec des modèles physiques, les auteurs montrent que deux forces agissent de concert. D'une part, la membrane des organites de réplication est systématiquement plus épaisse que le RE normal, ce qui suggère que des protéines virales ou des lipides modifiés rigidifient et courbent la membrane pour former un bourgeon stable avant même l'entrée de l'ARN. D'autre part, lorsque l'ARN viral est présent, il s'enroule à l'intérieur de la poche et pousse vers l'extérieur, augmentant la taille du bourgeon. Des calculs fondés sur les tailles mesurées indiquent que chaque organite rempli contient vraisemblablement la pression équivalente à environ une copie du génome viral sous forme double brin. Autrement dit, le virus utilise à la fois une membrane préformée et la poussée physique de son propre matériel génétique pour construire et stabiliser ses mini‑usines.
Ligne d'assemblage : de la copie du génome aux nouveaux virus
L'étude révèle aussi à quel point la production virale est liée à ces sites de réplication. Dans leurs vues 3D, les chercheurs ont fréquemment observé de nouvelles particules virales se formant juste à côté des organites de réplication, bourgeonnant dans des espaces ressemblant au RE voisins. Les particules immatures présentaient une surface en pointes, tandis que les particules plus matures paraissaient lisses. Les mesures effectuées dans les tomogrammes montraient que les particules immatures se situent plus près des organites de réplication que les particules matures, ce qui implique que, en ne se déplaçant que sur une courte distance à travers des compartiments membranaires entremêlés, les particules subissent les changements structuraux nécessaires pour devenir infectieuses. Un grand assemblage protéique au niveau du « col » étroit où chaque bourgeon de réplication se connecte au cytoplasme semble attacher l'organite de réplication à une membrane voisine où le bourgeonnement a lieu. Ce complexe agirait comme une fermeture éclair moléculaire qui coordonne la production d'ARN avec l'encapsidation de cet ARN dans de nouvelles particules virales.
Ajuster la maturation par un seul acide aminé
Pour sonder le contrôle de la maturation virale, l'équipe a comparé deux versions d'un virus chimérique ne différant que par un seul acide aminé à un site reconnu par une enzyme cellulaire appelée furine. Cette enzyme clive une protéine de surface virale, contribuant à transformer les particules immatures en pointes en particules matures et lisses. Dans des essais de clivage in vitro et dans des cellules infectées, la variante portant une arginine à cette position était clivée plus rapidement que la variante portant une glutamine. Observé en cellules par cryo‑tomographie électronique, le virus à clivage plus rapide produisait une proportion plus élevée de particules matures à proximité des organites de réplication. Malgré ces différences microscopiques, les deux variantes présentaient des profils de croissance et de pathogénicité similaires chez la souris, ce qui suggère que le virus peut tolérer une gamme d'efficacités de maturation tout en restant infectieux.
Observer l'infection directement dans le cerveau
La plupart des études structurales sur les virus reposent sur des lignées cellulaires, mais ce travail s'étend aux tissus vivants. Les chercheurs ont isolé une structure cérébrale appelée plexus choroïde chez des souris infectées et l'ont préparée pour la cryo‑tomographie électronique en utilisant la vitrification par haute pression et le fraisage par faisceau d'ions focalisé. Même dans cet environnement complexe, ils ont observé les mêmes caractéristiques distinctives : amas d'organites de réplication, membranes épaissies et vésicules voisines remplies de particules virales matures. Cela démontre que le remodelage des membranes et la séquence étroitement couplée réplication–assemblage–maturation observée en culture cellulaire opèrent également dans le cerveau, où ces virus provoquent la maladie.
Pourquoi ces processus cachés importent
Pour un public non spécialiste, le message central est que ces virus infectant le cerveau exploitent une chaîne d'assemblage hautement organisée à l'intérieur de nos cellules. Ils sculptent les membranes cellulaires en minuscules bulles pressurisées où les génomes sont copiés, relient ces bulles directement aux sites où de nouvelles particules bourgeonnent, et entament même les dernières étapes de maturation à portée de main du site de réplication d'origine. L'identification des membranes de réplication épaissies, du complexe protéique traversant le col et des compartiments de maturation étroitement imbriqués explique non seulement l'efficacité de la réplication des flavivirus, mais souligne aussi de nouvelles cibles pour des antiviraux visant à perturber les usines virales cachées et leurs voies d'assemblage.
Citation: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
Mots-clés: flavivirus, cryo‑tomographie électronique, organites de réplication, maturation virale, encéphalite transmise par les tiques