Clear Sky Science · fr
Perspicacité spectroélectrochimique sur les catalyseurs cuivre-cobalt pour la co-électroréduction du CO2 et du nitrite en urée
Transformer des gaz résiduels en engrais
L’urée est au cœur de l’agriculture moderne, mais sa production conventionnelle demande beaucoup d’énergie et génère d’importantes émissions de carbone. Cette étude explore une approche très différente : utiliser l’électricité pour transformer directement le dioxyde de carbone (CO2) et des déchets azotés (comme le nitrite issu de gaz d’échappement ou d’eaux usées) en urée. Pour le lecteur non spécialiste, l’intérêt est évident : une voie vers un engrais essentiel qui pourrait réduire les émissions, valoriser des flux de déchets comme matières premières et, un jour, être alimentée par de l’électricité renouvelable.
Pourquoi repenser la fabrication de l’urée ?
Aujourd’hui, l’urée est principalement produite en deux étapes : on fabrique d’abord de l’ammoniac à partir de l’azote et d’un hydrogène d’origine fossile (procédé Haber–Bosch), puis on fait réagir l’ammoniac avec le CO2 à haute température et pression. Cette chaîne est centralisée, exigeante en capital et émet près d’une tonne de CO2 par tonne d’urée produite. À mesure que la demande mondiale en engrais augmente, les coûts environnementaux suivent. Une alternative consiste à contourner les combustibles fossiles en pilotant les étapes chimiques clés avec de l’électricité, idéalement renouvelable, et en utilisant le CO2 et les oxydes d’azote (NOx) actuellement traités comme des déchets.
Un nouveau rôle pour le cuivre et le cobalt
Les auteurs conçoivent des catalyseurs en film mince obtenus par co-sputtering de cuivre (Cu) et de cobalt (Co) sur du papier carbone, en ajustant finement le rapport Cu:Co. Ils se concentrent sur la réduction électrochimique simultanée du CO2 et du nitrite (NO2⁻) en milieu aqueux et à pH neutre, un contexte favorable à la formation délicate de liaisons carbone–azote (C–N) nécessaires à l’urée. La composition remarquable est un mélange 1:1 de Cu et Co, qui atteint un taux de production d’urée d’environ 61 millimoles par heure et par gramme de catalyseur à une tension appliquée modérée. La microscopie et les mesures aux rayons X montrent que les métaux sont intimement mélangés à l’échelle atomique et restent en grande partie métalliques pendant le fonctionnement, offrant une plateforme robuste où CO2 et nitrite peuvent réagir efficacement. 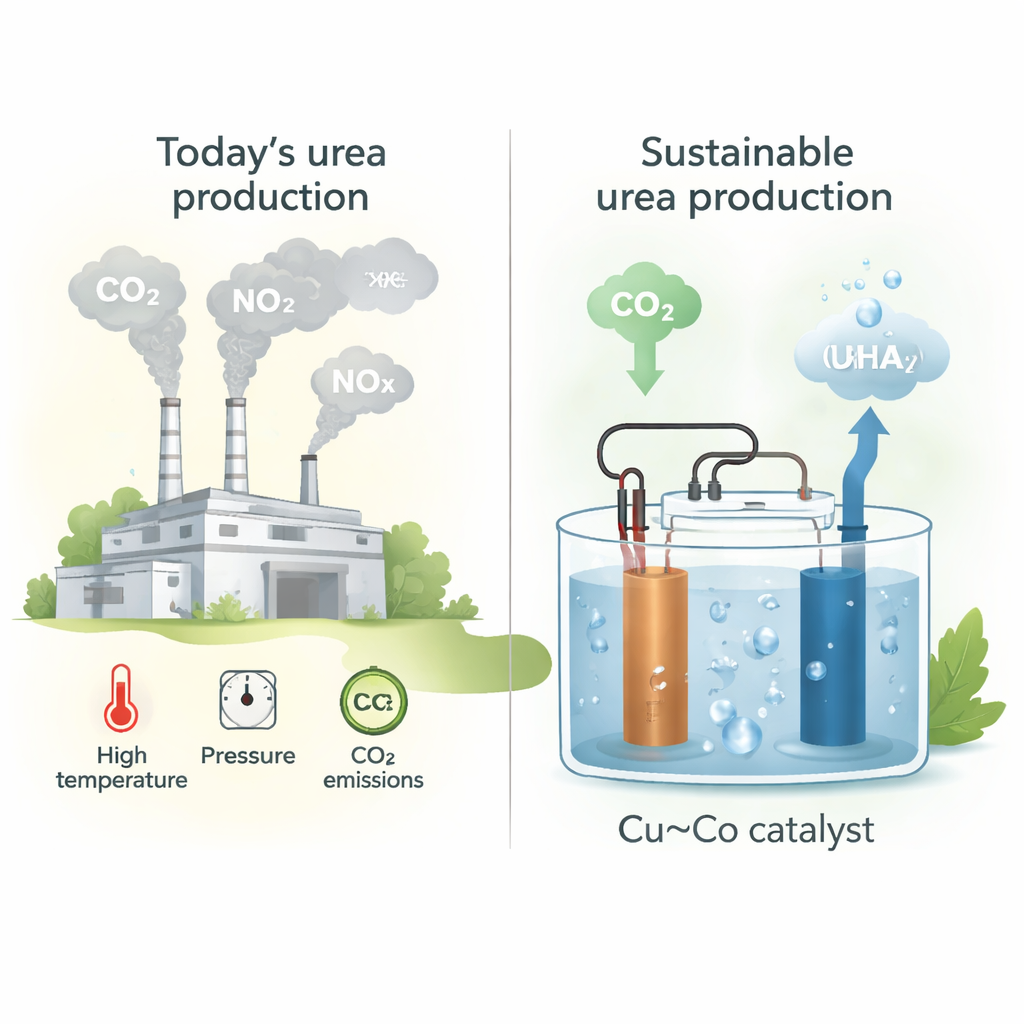
Comment le catalyseur répartit et partage le travail
Produire de l’urée de cette manière est difficile car des réactions plus simples — comme la formation d’hydrogène ou la réduction isolée du CO2 ou du nitrite — concurrencent fortement. Les chercheurs montrent que la clé est une division du travail entre des sites cuivre et cobalt qui agissent en tandem. Des tests électrochimiques révèlent que le cuivre seul convertit principalement le CO2 en carburants et produits carbonés, tandis que le cobalt seul réduit surtout le nitrite en ammoniac, sans formation d’urée dans les deux cas. Ce n’est que lorsque les atomes de Cu et Co sont étroitement mêlés qu’une production significative d’urée apparaît. Des « instantanés » spectroscopiques pris pendant la réaction détectent des fragments liés à la surface : des espèces carbonées dérivées du CO2 (*CO et *COOH) préférant le cuivre, et des espèces azotées dérivées du nitrite (*NH2 et groupes apparentés) préférant le cobalt. Aux frontières entre Cu et Co, ces fragments peuvent se rencontrer et se coupler pour former l’épine dorsale C–N de l’urée.
Trouver les bonnes conditions pour assembler les liaisons
L’étude montre que la composition seule ne suffit pas ; le milieu réactionnel et la membrane doivent aussi être optimisés. L’urée n’apparaît que dans un électrolyte bicarbonate neutre, qui maintient suffisamment de CO2 dissous et fournit la juste quantité de protons (ions hydrogène) pour piloter les étapes de « transfert proton–électron » sans saturer la surface par l’évolution de l’hydrogène. En conditions fortement acides ou fortement basiques, l’urée ne se forme pas ou se décompose rapidement en produits plus simples. Des expériences avec différentes sources d’azote montrent que le nitrite est particulièrement efficace pour la formation d’urée, surpassant le nitrate et l’hydroxylamine. Des tests sur plusieurs heures indiquent que les films Cu–Co sont relativement stables, avec seulement des pertes métalliques modestes et une production d’urée soutenue.
Regarder sous le capot avec la théorie
Pour comprendre pourquoi ce catalyseur en tandem fonctionne aussi bien, l’équipe a recours à des simulations informatiques basées sur la théorie de la fonctionnelle de la densité. Ces calculs corroborent l’idée que le cuivre favorise la fixation des espèces dérivées du CO2, tandis que le cobalt active mieux le nitrite et stabilise les fragments azotés. Les simulations pointent une étape particulière comme le goulot énergétique : le couplage d’un fragment *NH2 (issu du nitrite) avec un fragment *COOH (issu du CO2) pour former un intermédiaire parfois noté *NH2CO. Une fois cet élément en place, les étapes restantes vers l’urée sont comparativement aisées. L’interface Cu–Co abaisse le coût énergétique de ce couplage crucial par rapport au cuivre pur ou au cobalt pur, expliquant l’augmentation expérimentale du rendement en urée pour le système bimatériel. 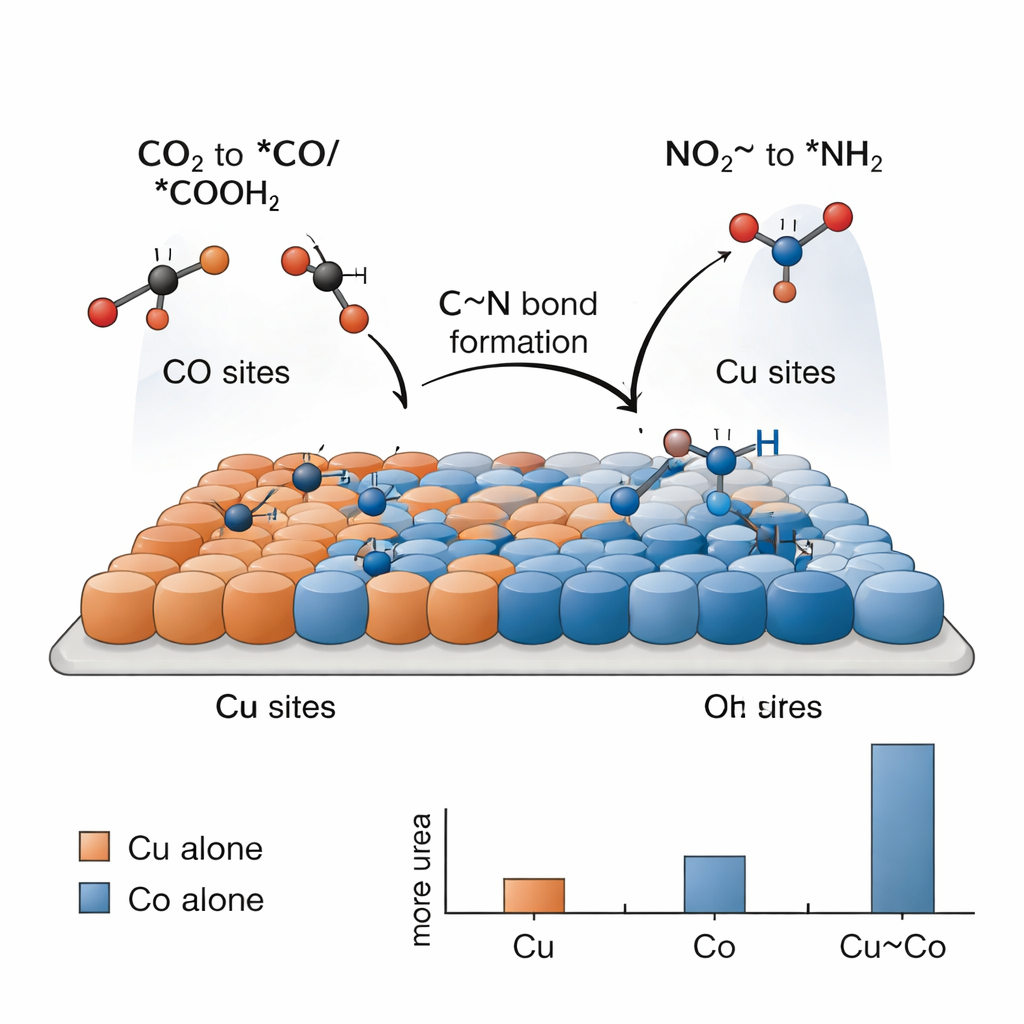
Des enseignements en laboratoire vers un engrais plus vert
En termes pratiques, ce travail ne remplace pas encore les immenses usines actuelles d’urée, mais il clarifie comment une future voie électrochimique pourrait être conçue. En montrant que le cuivre et le cobalt peuvent opérer en tandem — l’un fournissant des espèces carbonées activées, l’autre des espèces azotées activées, tous deux sous des conditions protoniques soigneusement contrôlées — l’étude trace une voie réaliste vers une production d’urée plus propre et potentiellement décentralisée, utilisant le CO2 et les déchets azotés comme ressources plutôt que comme polluants.
Citation: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Mots-clés: synthèse électrochimique d’urée, catalyseur cuivre cobalt, utilisation du CO2, réduction du nitrite, couplage C–N