Clear Sky Science · fr
Base structurale de l'inhibition sélective du transporteur GABA humain GAT3
Pourquoi il est important d'apaiser les signaux cérébraux
Notre cerveau dépend d'un équilibre délicat entre les signaux excitateurs et ceux qui apaisent. Un messager clé de l'inhibition est le GABA, une molécule qui aide à prévenir une activité incontrôlée associée à des affections comme l'épilepsie, les lésions d'AVC et la maladie d'Alzheimer. Cette étude se concentre sur une protéine appelée GAT3, qui élimine le GABA autour des cellules nerveuses. En révélant, à l'échelle atomique, comment une nouvelle molécule se fixe à GAT3 et l'inactive, les chercheurs fournissent une feuille de route structurale pour concevoir des médicaments de nouvelle génération capables de renforcer en douceur le système de freinage naturel du cerveau.
La pédale de frein du cerveau
Le GABA est le principal neurotransmetteur inhibiteur, donc calmant, du système nerveux central. Après sa libération au niveau des terminaisons nerveuses, il doit être rapidement éliminé pour que les circuits cérébraux puissent se réinitialiser. Ce nettoyage est assuré par des protéines de transport qui pompent le GABA vers l'intérieur des cellules. Deux de ces transporteurs dominent dans le cerveau : GAT1, principalement présent sur les neurones, et GAT3, localisé sur des cellules de soutien appelées astrocytes. Alors qu'un médicament bloquant GAT1 (la tiagabine) est utilisé depuis des décennies pour traiter l'épilepsie, des médicaments comparables ciblant GAT3 ont pris du retard. Pourtant GAT3 présente un intérêt particulier car il contrôle les niveaux de GABA en dehors des synapses et module une inhibition de fond durable qui peut affiner l'activité cérébrale. 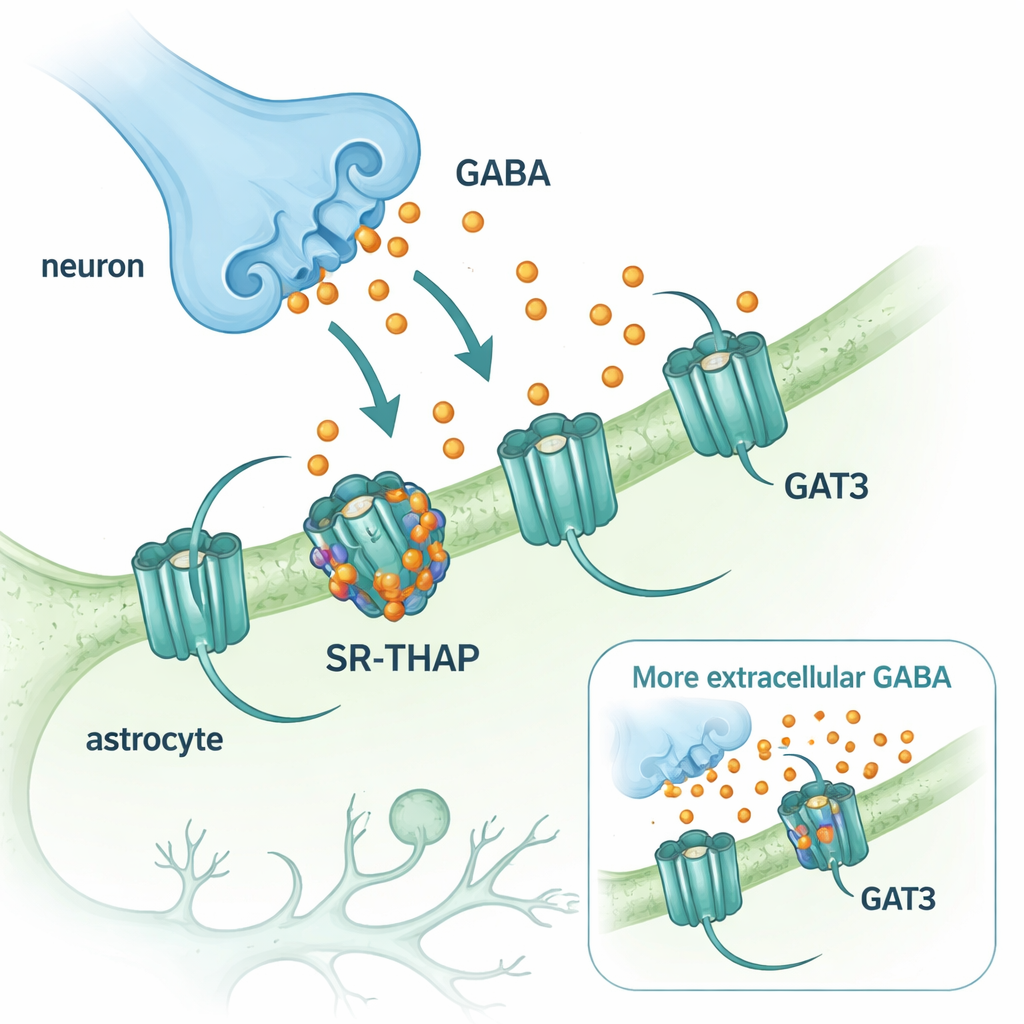
Concevoir une serrure moléculaire plus précise
Les tentatives pour inhiber GAT3 ont été freinées par le manque d'informations structurales détaillées. De nombreux composés antérieurs ont été créés par essai‑erreur, souvent en ajoutant des groupements volumineux à des molécules connues ressemblant au GABA. L'un des plus connus, (S)‑SNAP‑5114, s'est avéré chimiquement instable et difficile à utiliser in vivo. En s'appuyant sur un parent plus stable de ce composé, les auteurs ont mis au point SR‑THAP, une nouvelle petite molécule conçue pour s'ajuster plus parfaitement à GAT3 et résister à la dégradation. Des expériences sur des cultures cellulaires humaines ont montré que SR‑THAP bloque fortement GAT3 et le fait de manière non compétitive : au lieu de simplement rivaliser avec le GABA sur le site habituel, il modifie le fonctionnement du transporteur en réduisant sa capacité maximale de transport.
Observer GAT3 à résolution quasi atomique
Pour comprendre exactement comment SR‑THAP agit, l'équipe a eu recours à la cryo‑microscopie électronique, une technique qui image des protéines vitrifiées à l'aide d'électrons et reconstruit leur forme tridimensionnelle. Ils ont résolu trois variantes du GAT3 humain : lié à SR‑THAP, lié au GABA, et dans un état sans substrat. Les trois révèlent l'architecture typique observée chez des transporteurs de neurotransmetteurs apparentés : 12 hélices étroitement empaquetées qui traversent la membrane et forment un trajet central pour le GABA et ses ions compagnons, le sodium et le chlorure. Dans la structure liée au GABA, le transporteur se trouve dans un état « occlus vers l'intérieur » — le GABA et un ion sodium sont maintenus au centre, isolés de l'extérieur comme de l'intérieur. Un acide aminé aromatique clé forme une interaction spécialisée avec le groupe amino du GABA, ce qui aide à expliquer comment GAT3 reconnaît son substrat.
Comment SR‑THAP coince le transporteur ouvert
À l'inverse frappant, la structure liée à SR‑THAP capture GAT3 dans un état « ouvert vers l'intérieur », l'apex interne de la protéine béant vers l'intérieur cellulaire. SR‑THAP est niché profondément dans cette cavité interne, coincé entre plusieurs hélices qui se déplacent normalement durant le cycle de transport. Il occupe trois petites poches de caractères chimiques différents, établissant un réseau de liaisons hydrogène et d'interactions hydrophobes. Cette position bloque efficacement le transporteur de sorte que le GABA et les ions ne peuvent plus compléter leur trajet. Les auteurs montrent que quelques acides aminés spécifiques qui bordent cette cavité diffèrent entre GAT3 et ses proches parents ; l'échange de l'un de ces résidus modifie à la fois l'activité de transport et la puissance de SR‑THAP, ce qui contribue à expliquer pourquoi l'inhibiteur est bien plus sélectif pour GAT3 que pour GAT1 ou d'autres transporteurs apparentés. 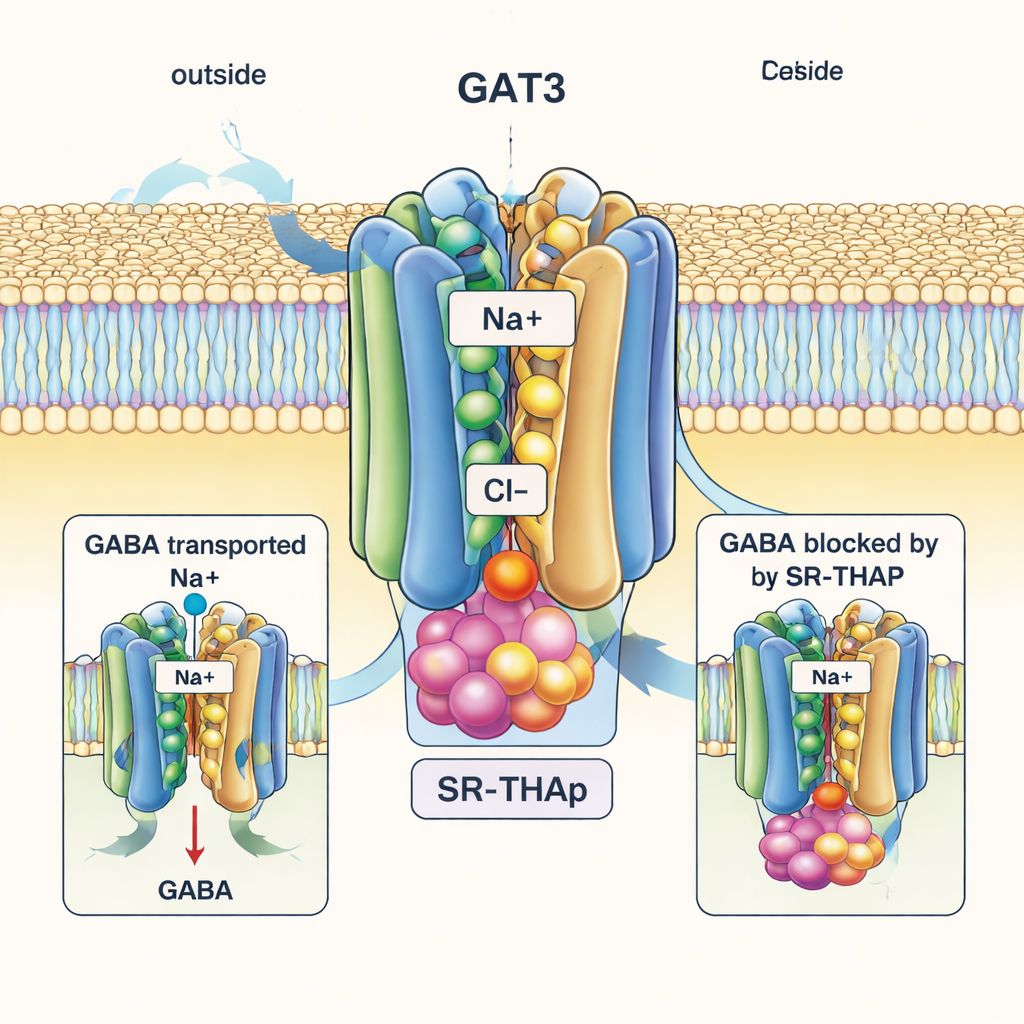
Ouvrir la voie à de nouveaux médicaments pour l'épilepsie et la santé cérébrale
Ensemble, ces structures montrent comment GAT3 alterne entre différentes conformations pour transporter le GABA, et comment SR‑THAP exploite une poche interne moins conservée pour figer ce cycle. Pour les non‑spécialistes, l'idée principale est que l'étude fournit un plan moléculaire détaillé pour désactiver GAT3 de manière hautement sélective. De tels composés pourraient augmenter les niveaux de GABA calmant de façon plus précisément ajustée que les médicaments existants, conduisant potentiellement à de nouveaux traitements ou à des outils de recherche pour l'épilepsie, la récupération après AVC, la maladie d'Alzheimer et d'autres affections où la signalisation inhibitrice est perturbée.
Citation: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Mots-clés: Transporteur de GABA, GAT3, épilepsie, cryo‑EM, inhibition des neurotransmetteurs