Clear Sky Science · fr
Un mécanisme stochastique entraîne une translocation rapide du substrat dans la machine AAA+ ClpB
Comment les machines cellulaires maintiennent les protéines en mouvement
À l’intérieur de chaque cellule, de minuscules machines moléculaires tirent, poussent et remodelent en permanence les protéines pour éviter qu’elles ne s’agglomèrent et pour réparer les dommages. L’une de ces machines, appelée ClpB, aide à dégager les protéines emmêlées — une fonction essentielle à la survie cellulaire en conditions de stress. Cette étude pose une question simple mais fondamentale : comment ClpB convertit-il le carburant chimique ATP en travail mécanique pour tirer une chaîne protéique à travers son pore central, et le fait-il par des pas réguliers et synchronisés ou de façon plus aléatoire et diffusif ?
Un anneau de sauvetage des protéines en action
ClpB appartient à une vaste famille d’enzymes appelées machines AAA+ qui s’assemblent en structures annelaires avec un tunnel central. Beaucoup ont été observées en détail par cryo-microscopie électronique, d’où a émergé le modèle populaire du « passage de main en main » : chaque molécule d’ATP hydrolysée entraînerait un petit pas précis, comme une équipe de personnes tirant successivement sur une corde. D’autres expériences laissaient toutefois entendre que ClpB pouvait déplacer les protéines bien plus vite que ne le laisserait penser sa lente consommation d’ATP. Pour résoudre cette énigme, les auteurs ont observé des molécules uniques de ClpB en temps réel alors qu’elles faisaient passer une protéine test flexible, la κ-caséine, à travers leur pore.
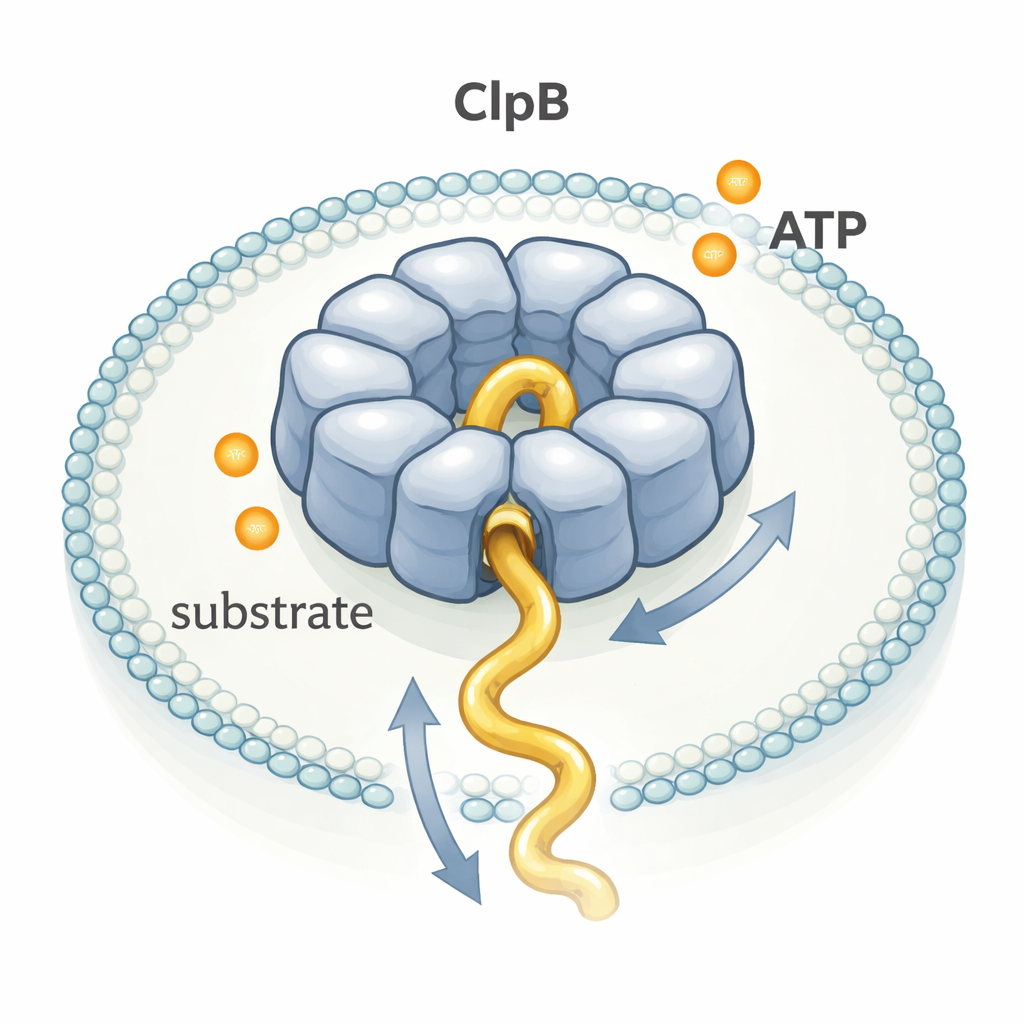
Observer une molécule à la fois
Les chercheurs ont piégé des anneaux individuels de ClpB et des molécules uniques de κ-caséine ensemble à l’intérieur de petites bulles lipidiques fixées sur une surface de verre. Ils ont fixé des colorants fluorescents à des points précis sur ClpB et sur la chaîne protéique, puis utilisé le FRET mono‑molécule, une technique qui rend compte de changements de distance entre colorants à l’échelle du nanomètre. Quand la κ-caséine glissait dans le pore de ClpB, les colorants se rapprochaient et le signal FRET montait en pic bref ; quand la chaîne ressortait, le signal retombait. En mesurant la durée et l’amplitude de milliers de ces pics, ils ont pu déduire la vitesse et la distance parcourue par des segments de la protéine à travers le pore.
Rapide, faiblement alimenté et presque insensible à la température
De manière surprenante, les évènements de translocation étaient extrêmement rapides : le segment marqué de la κ-caséine traversait typiquement plusieurs nanomètres du pore en environ 1–2 millisecondes — soit à peu près mille fois plus vite que l’intervalle moyen entre événements d’hydrolyse de l’ATP dans ClpB. La plupart des évènements étaient aussi courts et suivaient une large distribution en loi de puissance plutôt qu’un seul temps caractéristique. Faire varier la température de 10 à 32 °C ralentissait à peine ces mouvements, ce qui implique que la barrière d’énergie pour le déplacement est minime comparée à celle de moteurs à « coup de force » classiques comme la kinésine. De même, diminuer la concentration d’ATP réduisait fortement la fréquence des évènements, mais avait presque aucune incidence sur la durée de chaque évènement. L’ATP, en d’autres termes, contrôlait davantage le moment où ClpB s’engageait et la fréquence de ses actions que la vitesse des rafales individuelles de translocation.
Mouvement d’avant en arrière avec un biais vers l’avant
Pour savoir si les chaînes se déplaçaient toujours dans une seule direction, l’équipe a réalisé des expériences FRET à trois couleurs plus complexes, marquant les deux extrémités du pore et le substrat. Cela leur a permis de distinguer si la κ-caséine entrait par le haut ou par le bas de l’anneau et si elle traversait complètement ou reculait. Ils ont identifié six schémas distincts : passage complet avant et arrière, visites partielles plus longues où la chaîne explorait les deux extrémités du pore avant de partir, et rencontres fugaces près d’une seule extrémité. Environ les trois quarts des évènements complets allaient vers l’avant, mais une fraction substantielle allait en arrière, révélant que ClpB permet une diffusion bidirectionnelle du substrat avec seulement un biais avant modeste. Lorsque l’ATP était remplacé par un analogue hydrolysé lentement, les évènements devenaient rares et beaucoup plus lents, et la préférence vers l’avant disparaissait pratiquement.
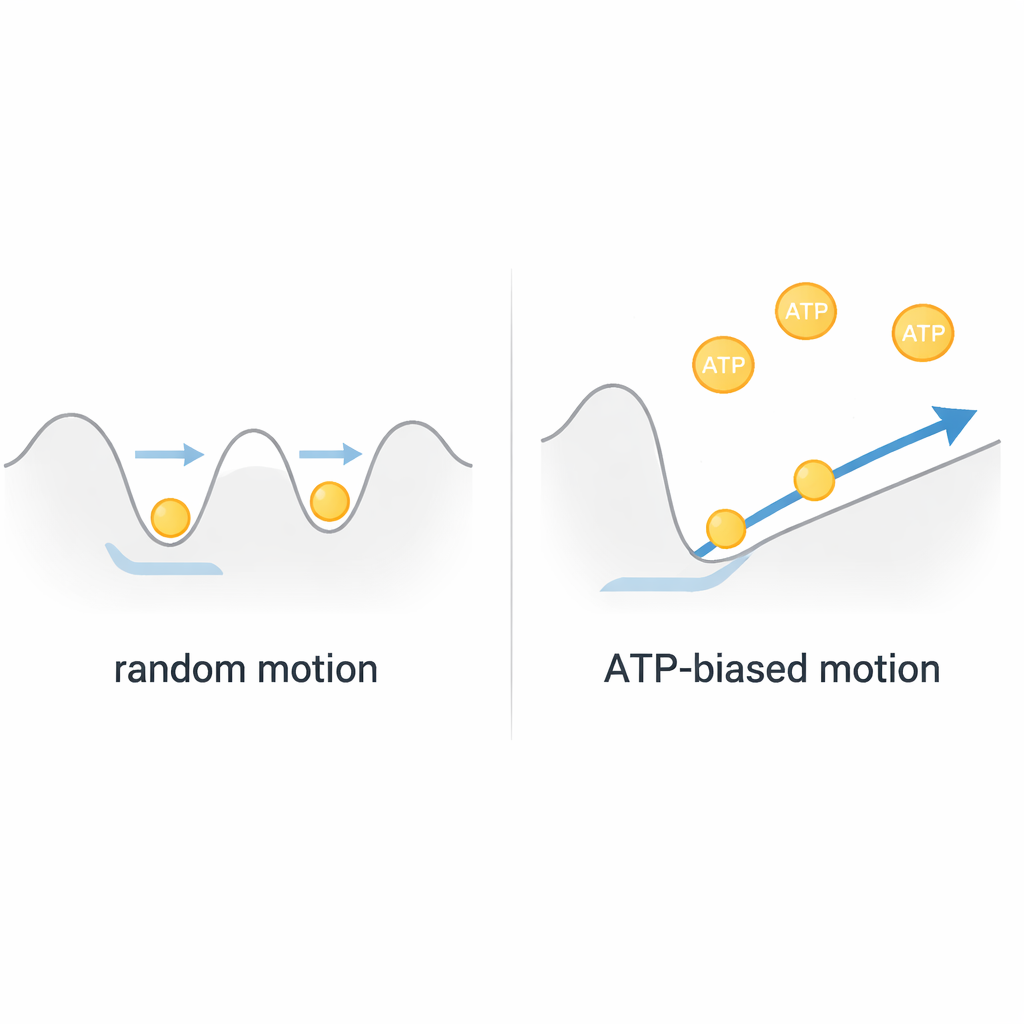
Un moteur brownien, pas un simple treuil
En rassemblant ces observations, les auteurs concluent que ClpB fonctionne davantage comme un moteur brownien qu’un treuil rigide entraîné par le carburant. La chaîne protéique vibre thermiquement dans un paysage énergétique peu profond à l’intérieur du pore, se déplaçant rapidement d’avant en arrière. L’ATP ne fournit pas directement de grands coups de traction discrets ; il module plutôt la forme de ce paysage via des mouvements rapides de « boucles de pore », favorisant subtilement le mouvement dans une direction. Comme chaque évènement complet de translocation corrèle avec seulement une ou deux molécules d’ATP consommées, ClpB atteint un transport remarquablement efficace et rapide en rectifiant le mouvement aléatoire plutôt qu’en le combattant. Cette perspective change notre vision de nombreuses machines AAA+, suggérant que les nanomoteurs biologiques exploitent souvent l’aléatoire au lieu de l’éliminer.
Citation: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Mots-clés: translocation des protéines, machine AAA+, moteur brownien, chaperonne moléculaire, FRET mono-molécule