Clear Sky Science · fr
Identification de PAM non canoniques thermotolérants pour une détection CRISPR‑Cas12a robuste en une seule étape
Augmenter la température des tests d’ADN
Des tests rapides et précis pour les infections et les altérations génétiques sont essentiels en médecine, mais les tests d’ADN actuels nécessitent souvent un équipement de laboratoire complexe et peuvent manquer des cibles rares ou subtiles. Cette étude montre que le simple fait d’exécuter un test basé sur CRISPR à une température légèrement plus élevée débloque beaucoup plus de « poignées » utilisables sur l’ADN, rendant les diagnostics en un tube plus rapides, plus sensibles et capables de distinguer même des différences d’une seule lettre dans le code génétique. 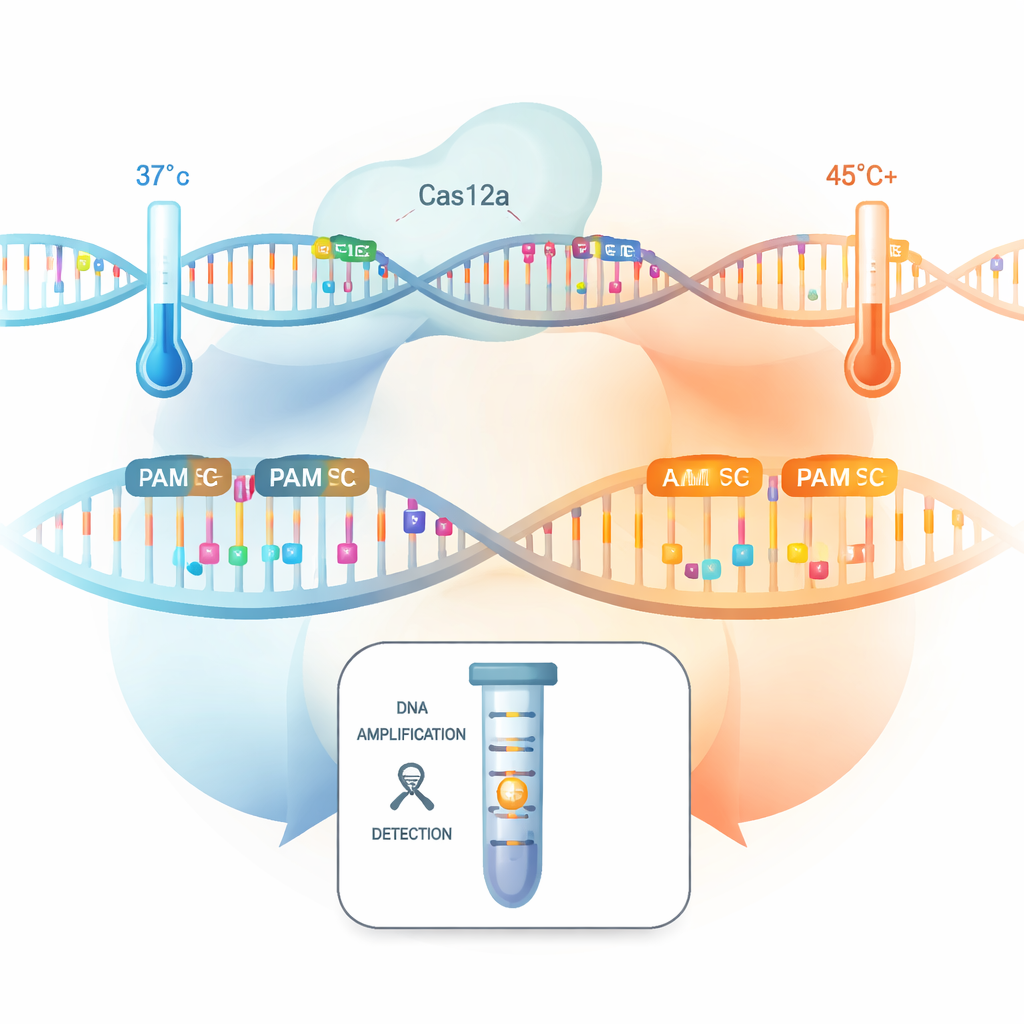
Pourquoi CRISPR a besoin d’un code postal
Les outils CRISPR comme Cas12a ciblent des séquences spécifiques d’ADN, guidés par un court ARN qui joue le rôle de chaîne de recherche. Mais ils ne peuvent se fixer et s’activer que si une étiquette voisine de quatre lettres, appelée PAM, présente la bonne séquence — traditionnellement un ensemble restreint commençant par « TTT ». C’est comme avoir besoin d’un numéro de maison pour livrer une lettre : si le bon numéro manque, le message n’arrive jamais. Cette exigence du PAM limite donc les endroits où CRISPR peut agir, ce qui est un sérieux inconvénient lorsque les cliniciens doivent détecter des mutations particulières, des marqueurs de résistance aux médicaments ou des variants viraux qui ne sont pas situés à côté de ces balises classiques.
Découvrir de nouvelles « portes » à des températures plus élevées
Les chercheurs ont testé systématiquement les 256 combinaisons possibles de PAM à quatre lettres pour évaluer dans quelle mesure elles activent l’activité de coupure « collatérale » de Cas12a — sa capacité à sectionner de nombreuses sondes d’ADN environnantes une fois la cible trouvée, principe des signaux diagnostiques CRISPR. À la température corporelle normale (37 °C), seules quelques PAM non standard offraient des performances comparables aux classiques. Mais en portant la réaction à environ 45 °C, un phénomène frappant est apparu : 82 PAM non canoniques ont soudainement produit une forte activité de coupure, rivalisant avec les balises standard. L’équipe pense que la chaleur supplémentaire assouplit la structure locale de l’ADN et rend le complexe Cas12a plus flexible, abaissant la barrière à la reconnaissance de ces PAM auparavant « faibles ».
Signal fort, template préservé
Cas12a présente deux modes de coupure. En mode « cis », il coupe l’ADN spécifique qu’il est chargé de reconnaître ; en mode « trans », une fois activé, il tranche rapidement toute sonde porteuse de signal à proximité, ce qui illumine le test. Les chercheurs ont constaté qu’à des températures plus élevées, les PAM non canoniques induisaient une coupe trans très forte — idéale pour un signal vif et rapide — tout en maintenant la coupe cis de l’ADN principal relativement faible. Cette combinaison est parfaite pour des tests en un seul tube, où l’ADN doit d’abord être amplifié sans être détruit. Ils ont également montré qu’à ces températures plus chaudes Cas12a devient beaucoup plus exigeant vis‑à‑vis des mésappariements entre l’ARN guide et la cible : même une seule lettre erronée peut éteindre le signal, en particulier lorsqu’on utilise des PAM non canoniques. 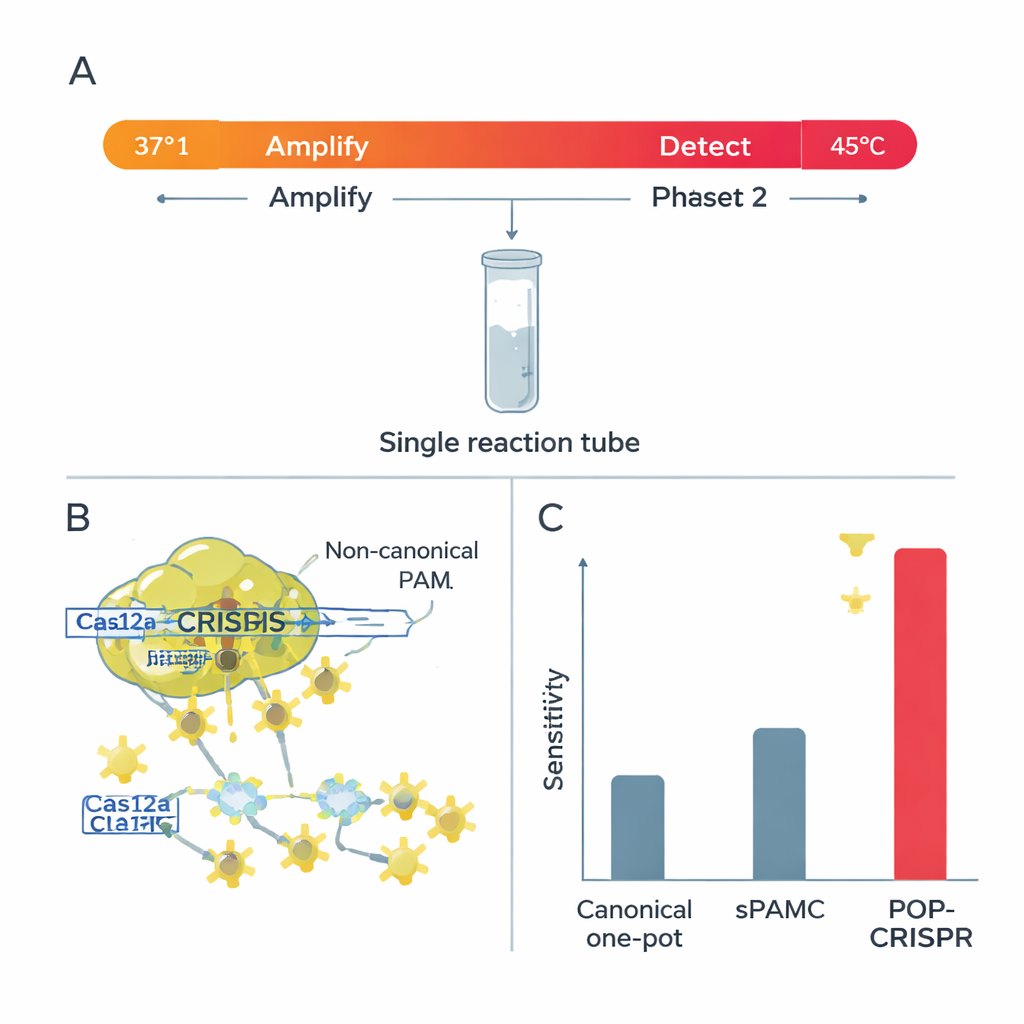
Un test one‑pot plus intelligent : POP‑CRISPR
S’appuyant sur ces observations, l’équipe a conçu POP‑CRISPR, un essai « poïkilotherme » (à température variable) en une seule étape. La réaction commence autour de 37 °C, où une méthode d’amplification isotherme multiplie discrètement tout ADN ou ARN cible pendant que Cas12a reste relativement inactif. Après environ 10 minutes, le mélange est chauffé à ~45 °C, un point où Cas12a — guidé vers des sites PAM non canoniques — s’active en un fort découpage trans et génère un signal fluorescent intense. Ce simple protocole en deux paliers de température a amélioré la sensibilité de détection d’environ dix fois par rapport aux méthodes one‑pot CRISPR antérieures qui utilisaient aussi des PAM faibles, et a nettement surpassé les formats one‑pot basés sur des PAM canoniques.
Du banc au chevet en quelques minutes
Le système POP‑CRISPR a été testé sur des échantillons cliniques réels. Il a détecté avec sensibilité le papillomavirus humain (HPV‑16) dans des prélèvements vaginaux et Mycoplasma pneumoniae dans des prélèvements respiratoires, y compris des cas de très faibles charges virales en « zone grise » que les méthodes standard ont du mal à identifier. Fait crucial, POP‑CRISPR a pu distinguer des souches de Mycoplasma résistantes aux médicaments portant une mutation d’une seule lettre dans un gène ribosomique, alors même qu’aucun PAM classique n’était proche de cette mutation — une tâche qui bloque de nombreux tests Cas12a existants. Pour rendre l’approche adaptée au terrain, les auteurs ont combiné une étape rapide de lyse par chaleur et Chelex de deux minutes (évitant une extraction complète de l’ADN) avec un lecteur de fluorescence de la taille d’une paume contrôlé par smartphone. Ensemble, ce flux permet de transformer un prélèvement brut en un résultat numérique oui/non en environ 20 minutes.
Qu’est‑ce que cela change pour les tests courants ?
En augmentant la température de réaction et en exploitant un ensemble beaucoup plus large de « portes » PAM, ce travail transforme Cas12a en un capteur plus flexible et plus précis. POP‑CRISPR offre une détection d’acides nucléiques plus rapide, plus sensible et plus spécifique dans un tube clos unique, tout en élargissant la gamme de sites génétiques ciblables — notamment des mutations d’un seul nucléotide associées à la résistance aux médicaments ou au cancer. Pour les patients, cela peut se traduire par des diagnostics plus rapides sur place et des traitements mieux adaptés ; pour les chercheurs et les développeurs de tests, c’est une nouvelle façon puissante de concevoir des diagnostics CRISPR à la fois plus robustes et plus discriminants.
Citation: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Mots-clés: diagnostique CRISPR, Cas12a, sites PAM, tests au point de soin, détection d'acides nucléiques