Clear Sky Science · fr
Mécanismes structuraux d’inhibition et d’activation du canal potassique humain SK2 activé par Ca2+ à faible conductance
Pourquoi de petits canaux potassiques sont importants
Chaque pensée que vous avez et chaque battement de cœur que vous ressentez dépendent de signaux électriques dans vos cellules. Ces signaux sont façonnés par des pores microscopiques, appelés canaux ioniques, qui laissent passer des atomes chargés. Une de ces familles, les canaux potassiques à petite conductance activés par le calcium (canaux SK), aide à contrôler l’excitabilité des neurones et le rythme cardiaque. Cet article révèle, à l’échelle atomique, comment différents médicaments et une toxine d’abeille peuvent soit fermer soit stimuler un membre clé de cette famille, le canal humain SK2 — des informations susceptibles d’orienter de nouveaux traitements pour des troubles allant de la fibrillation atriale aux tremblements et aux problèmes de mémoire.
Comment les canaux SK2 agissent comme des freins cellulaires
Les canaux SK2 se trouvent dans la membrane cellulaire et jouent le rôle de petits freins sur l’activité électrique. Lorsque l’intérieur d’une cellule se charge brièvement en ions calcium lors d’un signal électrique, une protéine auxiliaire nommée calmoduline détecte cette élévation. La calmoduline est attachée au côté interne de SK2 et, lorsqu’elle capture le calcium, elle tire sur une partie du canal comme une corde de traction, ouvrant une porte qui permet aux ions potassium de sortir. Ce flux sortant contribue à calmer la cellule après son déclenchement, modulant la fréquence d’émission des neurones et la régularité des battements cardiaques. Parce que les canaux SK1–3 sont largement répandus dans le cerveau et le cœur, et que SK2 est un sous‑type particulièrement important, comprendre exactement comment ils s’ouvrent, se ferment et répondent aux médicaments est crucial pour concevoir des traitements précis.
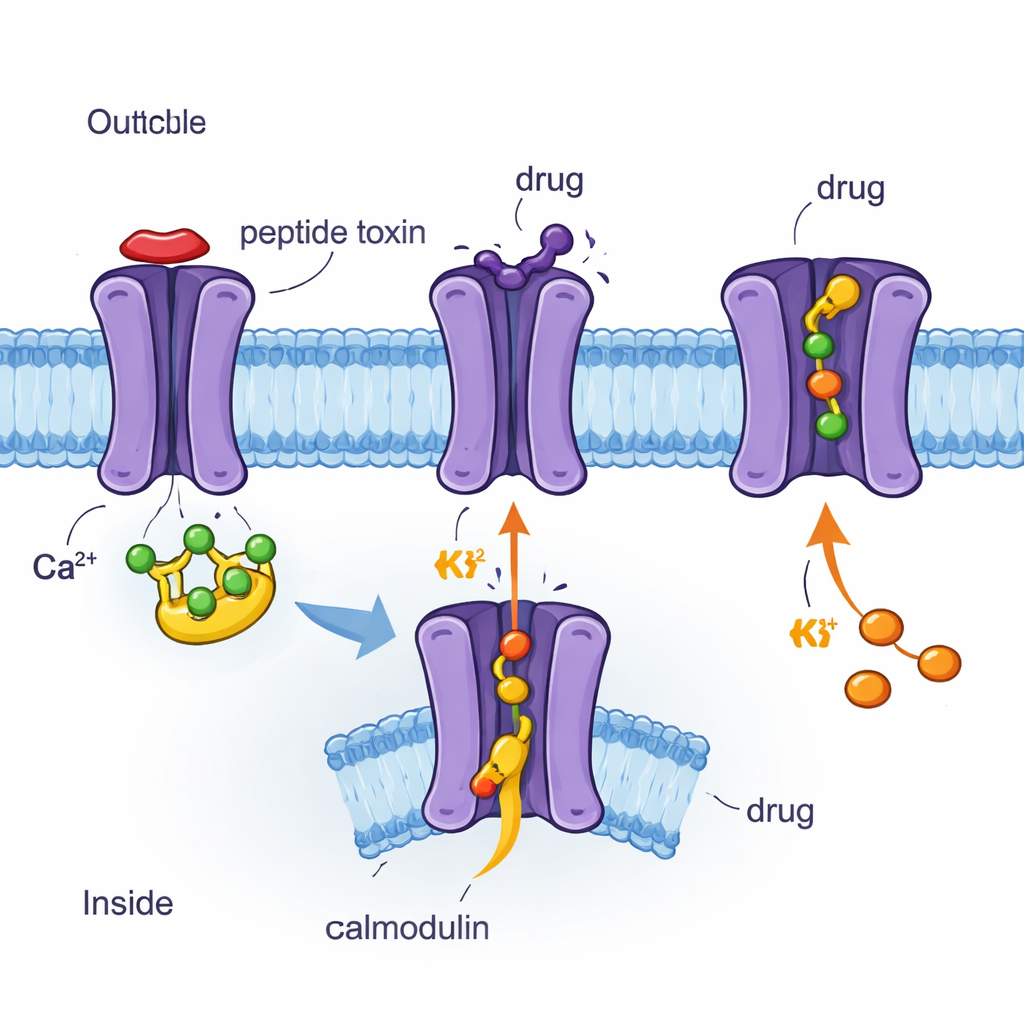
Utiliser la cryo‑EM pour voir canaux et médicaments atome par atome
Les auteurs ont utilisé la cryo‑microscopie électronique (cryo‑EM), une technique qui image des protéines vitrifiées à une résolution quasi‑atomique, pour déterminer quatre structures tridimensionnelles du canal SK2 humain lié à la calmoduline et à différentes molécules. Celles‑ci comprenaient le peptide du venin d’abeille apamine, le bloqueur synthétique UCL1684, l’inhibiteur clinique AP30663 et l’activateur clinique CAD‑1883. Les quatre structures montrent SK2 comme une assemblée en quatre parties traversant la membrane, avec la calmoduline attachée à l’intérieur. La comparaison de ces instantanés a révélé quelles parties du canal sont rigides, lesquelles sont flexibles, et comment la calmoduline se déplace lorsque le canal est fermé ou ouvert. Les chercheurs ont également combiné ces images avec des mesures électriques en cellule, testant comment des changements d’acides aminés spécifiques modifient la réponse du canal à chaque composé.
Une toxine d’abeille et un médicament de laboratoire qui obturent l’entrée externe
L’apamine, un petit peptide issu du venin d’abeille, est connue depuis longtemps comme un bloqueur extrêmement puissant et sélectif de SK2 utilisé en recherche. Les nouvelles structures montrent que l’apamine se lie comme un bouchon à l’entrée externe du pore SK2. Elle se loge dans un vestibule en forme de coupe formé par une courte boucle entre deux hélices (le linkeur S3–S4) qui est bien ordonnée dans SK2 mais souple dans un canal apparenté, SK4, ce qui explique l’insensibilité de SK4 à l’apamine. Des résidus positivement chargés clés sur l’apamine s’insinuent entre quatre chaînes latérales aromatiques du canal, établissant de fortes interactions électrostatiques et d’empilement qui scellent complètement le passage du potassium. UCL1684, un composé bis‑quinolinique synthétique, occupe essentiellement la même poche externe et bloque aussi la sortie des ions, mais sa taille plus petite lui permet de s’enfoncer plus profondément, mimant la position des charges positives critiques de l’apamine. La mutation des résidus du canal qui façonnent ce vestibule réduit fortement la sensibilité à l’apamine et, dans une moindre mesure, à UCL1684, confirmant que cette boucle externe sculptée est un déterminant majeur de l’action de la toxine et du médicament.
Un bouchon central et un coin interne qui affinent l’activité
En revanche, le candidat clinique AP30663 se lie dans la cavité centrale de SK2, juste en dessous du filtre de sélectivité qui choisit les ions potassium. Là, il agit comme un bouchon physique, calé entre des chaînes latérales spécifiques qui tapissent le pore. Des modifications de ces résidus de la paroi diminuent la capacité d’AP30663 à inhiber SK2, et des comparaisons de séquences expliquent pourquoi ses analogues proches distinguent SK1–3 de SK4. CAD‑1883, un modulateur positif développé pour les troubles du mouvement, utilise une stratégie différente. Il se glisse dans une poche à l’interface entre le lobe N de la calmoduline et un court linkeur (S4–S5) qui couple le mouvement de la calmoduline à la porte du canal. En renforçant les contacts dans cette poche, CAD‑1883 colle efficacement la calmoduline et SK2 dans une configuration qui tire la porte interne pour l’ouvrir et élargit le pore. Les comparaisons structurales montrent que cet état lié à CAD‑1883 ressemble à un canal complètement ouvert, bien que le filtre de sélectivité puisse adopter une forme inactivée après une ouverture prolongée.
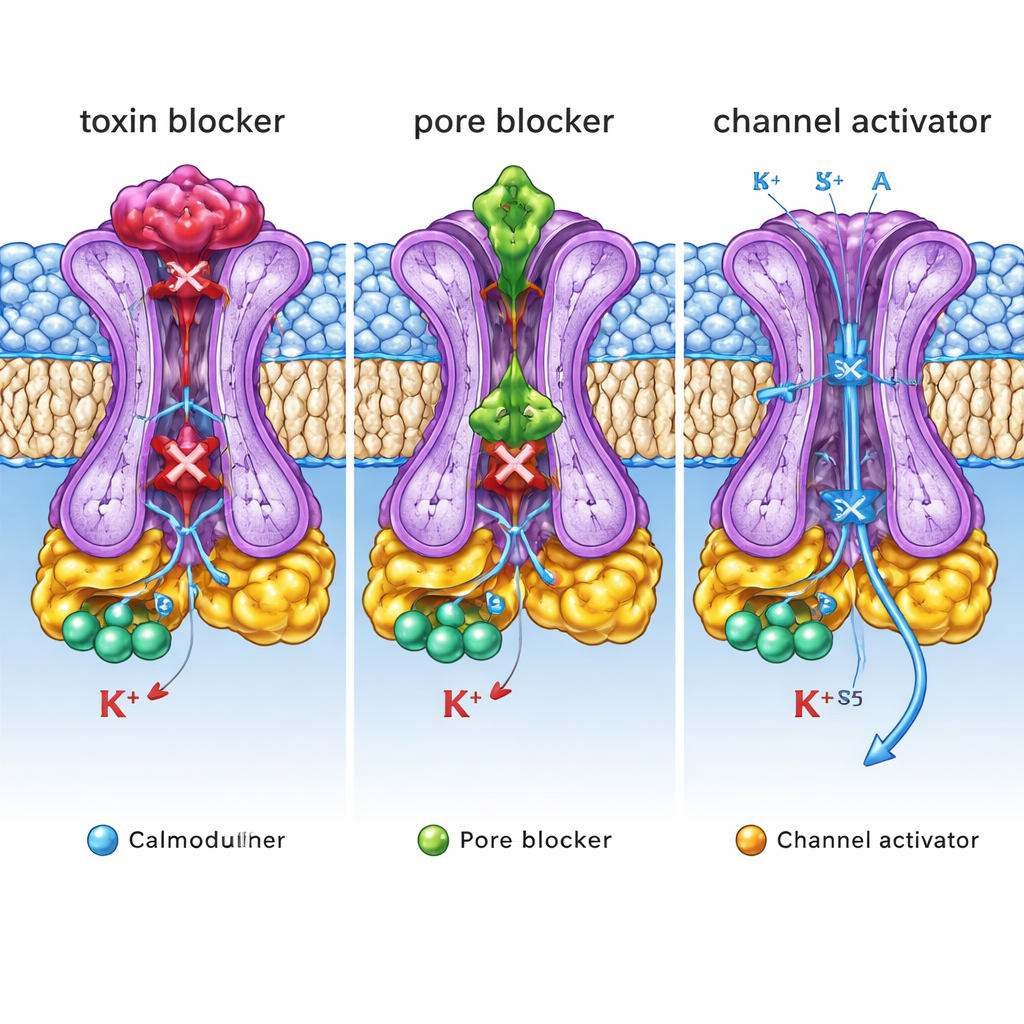
Ce que ces plans structuraux signifient pour la médecine
Pris ensemble, ces structures révèlent trois « boutons de contrôle » distincts sur un même canal SK2 : un couvercle externe où se logent des toxines et certains bloqueurs, une cavité interne du pore où d’autres inhibiteurs obturent le flux, et une poche latérale où des activateurs stabilisent l’ouverture. Pour un non‑spécialiste, le message clé est que le même canal ionique peut être modulé à la hausse ou à la baisse par des médicaments qui saisissent des poignées structurales très différentes. En cartographiant ces poignées avec une précision atomique et en reliant ces sites à des effets fonctionnels, ce travail fournit un plan détaillé pour concevoir des molécules de nouvelle génération qui diminuent ou renforcent sélectivement l’activité de SK2. De tels médicaments sur mesure pourraient un jour aider à normaliser des rythmes cérébraux anormaux, atténuer des tremblements ou corriger des battements cardiaques irréguliers avec moins d’effets secondaires.
Citation: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Mots-clés: Canaux potassiques SK2, canaux activés par le calcium, structures cryo‑EM, modulateurs de canaux ioniques, fibrillation atriale et tremblement