Clear Sky Science · fr
Migration et divisions altérées des cellules souches dans la dystrophie musculaire de Duchenne révélées par imagerie en direct
Pourquoi cette histoire musculaire est importante
La dystrophie musculaire de Duchenne (DMD) est une maladie infantile mortelle qui détruit progressivement le muscle. Pendant des décennies, la plupart des travaux se sont concentrés sur les grandes fibres musculaires qui se dégradent dans la DMD. Cette étude montre qu’un second acteur, plus discret, est lui aussi en difficulté : les cellules souches du muscle, qui réparent normalement les lésions. En observant ces cellules en vie, à l’intérieur des muscles de souris et sur des fibres individuelles, les auteurs révèlent comment les cellules souches dans la DMD perdent leur orientation, ouvrant de nouvelles pistes de traitement pour aider les muscles à se régénérer plus efficacement.
L’équipe de réparation intégrée du muscle
Chaque fibre musculaire squelettique est entourée d’une poignée de cellules souches résidentes, appelées cellules satellites musculaires. Dans un muscle sain, ces cellules sont le plus souvent au repos. Lorsqu’une blessure survient, elles se réveillent, se divisent et produisent soit de nouvelles cellules souches pour reconstituer la réserve, soit des cellules spécialisées qui fusionnent aux fibres endommagées. Cet équilibre soigneux entre auto-renouvellement et différenciation permet au tissu musculaire de rester robuste tout au long de la vie. Dans la DMD, cependant, les fibres musculaires se déchirent à répétition faute de dystrophine, une protéine structurale clé, ce qui soulève la question de savoir si l’équipe de réparation elle-même s’épuise ou se trompe de direction.
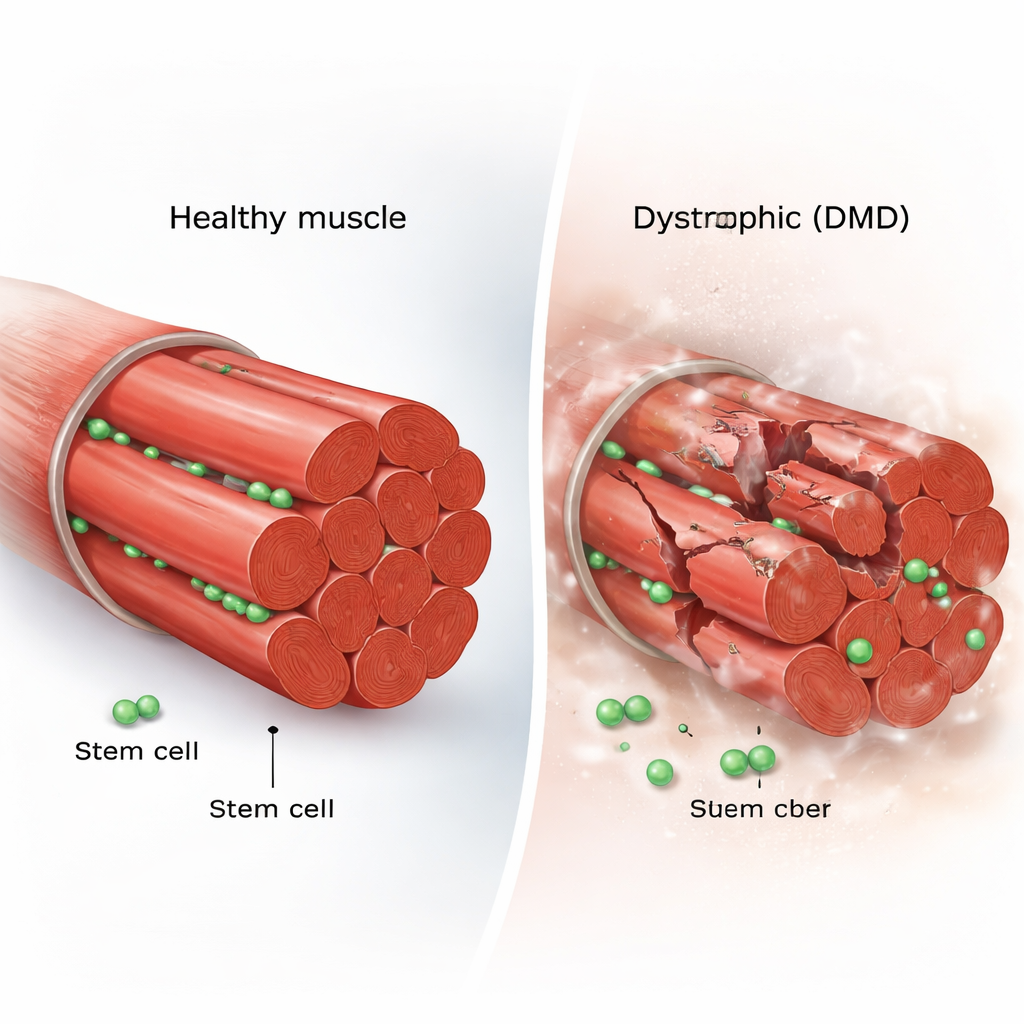
Filmer les cellules souches en action
Pour répondre à cette question, les chercheurs ont utilisé la souris mdx, un modèle standard de la DMD, et ont modifié ses cellules souches musculaires pour qu’elles brillent au microscope. Ils ont ensuite réalisé de l’imagerie intravitale, une technique qui permet de filmer des cellules vivantes à l’intérieur d’un animal anesthésié pendant de nombreuses heures. Ils ont aussi développé un système de « micropuits » sur mesure pour maintenir des fibres musculaires uniques en culture tout en suivant chaque division et chaque déplacement des cellules souches. Cette double approche leur a permis de suivre des cellules individuelles depuis le repos jusqu’à des divisions répétées, des migrations, et finalement la fusion dans un nouveau muscle, capturant des comportements que des clichés statiques pourraient facilement manquer.
Quand les cellules réparatrices se hâtent et trébuchent
Dans des muscles sains blessés, les cellules myogéniques issues des cellules souches s’allongeaient et rampaient le long des fibres selon des trajectoires relativement droites et dirigées, se divisant et se dispersant efficacement. En revanche, les cellules dystrophiques (mdx) devenaient souvent rondes et léthargiques. Elles se déplaçaient plus lentement et avec moins de direction, et une fraction notable restait presque immobile. L’équipe a également observé que les cellules mdx fusionnaient dans de nouvelles fibres musculaires plus tôt que la normale, et que de nombreuses cellules filles migraient ensemble au lieu de se séparer après la division. Globalement, les muscles mdx montraient des signes de « différenciation précoce » : les cellules souches se précipitaient pour devenir des cellules musculaires et former des fibres, au lieu de maintenir une réserve robuste pour des réparations futures.
Divisions cellulaires déséquilibrées et voisinage perturbé
Sur des fibres isolées, les chercheurs ont pu classifier la façon dont chaque cellule souche se divisait. Dans les muscles sains, la plupart des divisions étaient symétriques mais équilibrées : beaucoup produisaient deux filles proliférantes capables d’élargir la réserve de réparation, et moins produisaient deux cellules terminalement différenciées. Les divisions asymétriques, où une fille restait cellule souche et l’autre s’engageait dans la réparation, étaient relativement rares mais présentes. Dans les muscles mdx, le schéma a fortement changé : les divisions symétriques penchaient vers la production de deux cellules différenciées, avec beaucoup moins de divisions générant deux cellules renouvelantes. Des expériences de greffe croisée, où des cellules saines étaient placées sur des fibres dystrophiques et vice versa, ont montré que les défauts de migration étaient largement dictés par l’environnement de la fibre endommagée, tandis que le comportement excessivement différenciateur des cellules mdx suivait les cellules elles-mêmes, en partie façonné par leur histoire inflammatoire.
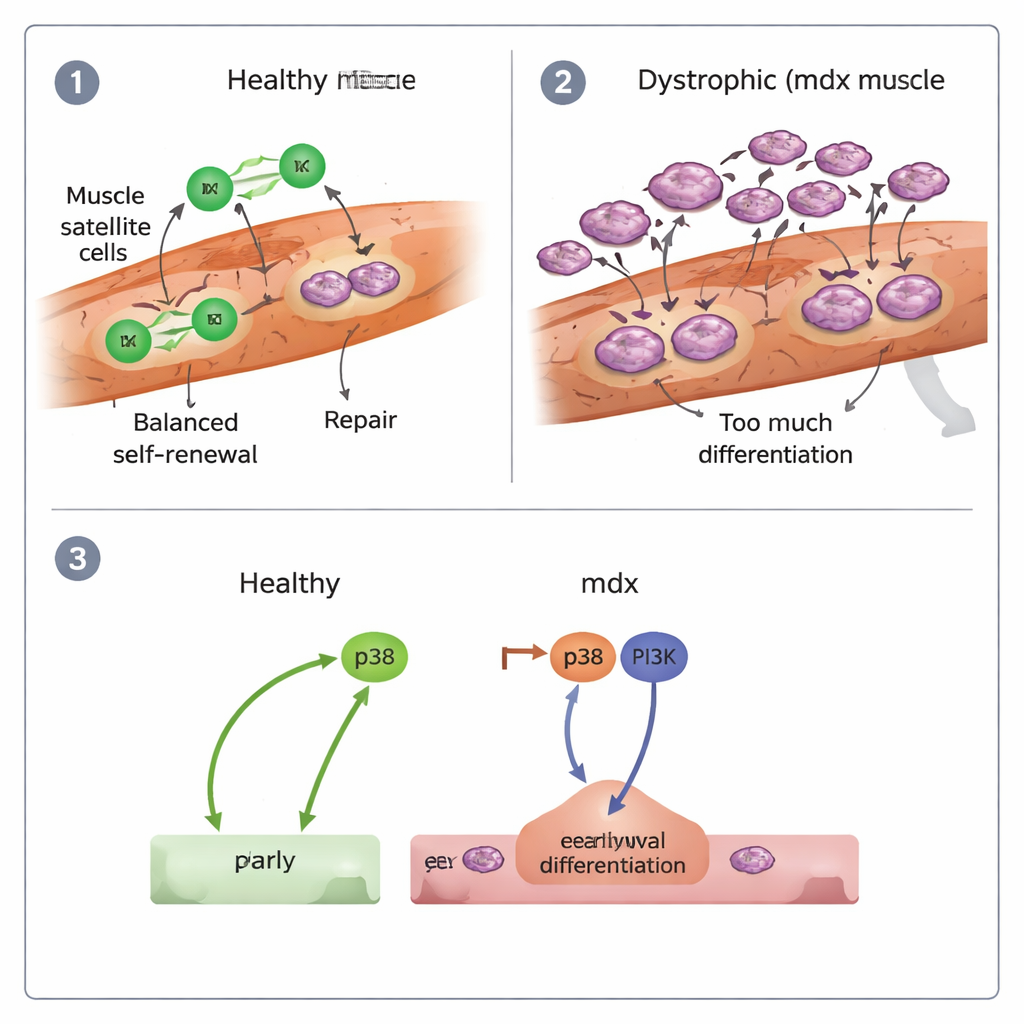
Signaux mal câblés et implications thérapeutiques
Les auteurs ont également sondé les interrupteurs moléculaires qui poussent les cellules souches à se différencier. Ils se sont concentrés sur deux voies de signalisation, connues sous les noms de p38 et PI3K. Dans les cellules saines, bloquer p38 réduisait fortement la différenciation, tandis qu’inhiber PI3K avait peu d’effet. Dans les cellules mdx, en revanche, il fallait bloquer les deux voies simultanément pour freiner la ruée excessive vers la spécialisation, et même dans ce cas leur capacité à continuer de proliférer restait faible. Cela suggère que les cellules souches dans la DMD sont poussées vers un « épuisement précoce » par l’activité combinée de p38 et PI3K, contribuant à une régénération qui commence vite mais ne peut être soutenue.
Une nouvelle vision de la Duchenne : aussi une maladie des cellules souches
Pour un lecteur non spécialiste, le message principal est que la DMD n’est pas seulement un problème de fibres musculaires fragiles ; c’est aussi un problème du système de réparation censé les réparer. Dans le muscle dystrophique, les cellules souches se déplacent moins efficacement, se divisent d’une manière qui épuise la réserve, et répondent de façon anormale à des signaux de croissance clés. En identifiant quels aspects sont causés par l’environnement musculaire endommagé et lesquels sont intégrés à l’état altéré des cellules souches, ce travail suggère de nouvelles stratégies : des thérapies qui tempèrent les signalisations p38 et PI3K, rétablissent des divisions cellulaires équilibrées ou améliorent le niche locale pourraient aider à reconstruire le muscle plus efficacement et prolonger les bénéfices des traitements géniques ou cellulaires pour les personnes vivant avec la dystrophie musculaire de Duchenne.
Citation: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
Mots-clés: Dystrophie musculaire de Duchenne, cellules souches musculaires, migration cellulaire, division des cellules souches, médecine régénérative