Clear Sky Science · fr
Des systèmes d'édition de bases séparés médiés par hétrodimères coiled-coil permettent des substitutions nucléotidiques flexibles et robustes
Réparer l'ADN avec moins d'effets indésirables
De nombreuses maladies sont causées par de petites fautes de frappe dans notre ADN — des erreurs d'une seule lettre qui peuvent avoir des conséquences potentiellement mortelles. Les scientifiques disposent d'outils puissants, appelés éditeurs de bases, capables de corriger ces erreurs sans couper l'ADN, mais ces outils sont volumineux et difficiles à délivrer en toute sécurité dans l'organisme. Cet article présente une nouvelle façon de scinder les éditeurs de bases en morceaux plus petits et plus intelligents qui conservent les performances de l'original, voire les dépassent, ouvrant de nouvelles voies pour traiter des maladies génétiques dans le foie, les muscles et au-delà.
Pourquoi la taille pose problème pour les outils de correction génétique
Les éditeurs de bases combinent des éléments du système CRISPR avec des enzymes capables d'échanger une lettre d'ADN contre une autre, par exemple transformer un A en G ou un C en T. Ces substitutions précises sont prometteuses pour traiter des affections comme l'hypercholestérolémie ou la dystrophie musculaire. Cependant, un vecteur de livraison majeur pour la thérapie génique, le virus adéno‑associé (AAV), ne peut transporter qu'environ 4,7 milliers de bases d'ADN, alors que les éditeurs de bases standard sont plus grands. Des travaux antérieurs ont tenté de scinder ces éditeurs en utilisant des « ciseaux » protéiques appelés inteines, ou en les compressant avec des enzymes miniatures, mais ces approches réduisaient souvent l'efficacité, complexifiaient la conception ou limitaient les sites génomiques accessibles.
Utiliser du Velcro moléculaire pour reconstruire l'éditeur
Pour résoudre ce problème, les chercheurs ont conçu un éditeur de bases « scindé » maintenu par de petits crochets protéiques en hélice appelés hétrodimères coiled‑coil — un peu comme du Velcro moléculaire. Ils ont séparé l'éditeur en deux parties : l'une portant la Cas9 nickase ciblant l'ADN et l'autre portant l'enzyme d'édition. De courtes peptides coiled‑coil sur chaque moitié se reconnaissent et s'assemblent lorsqu'elles atteignent la même séquence d'ADN. Cela crée des éditeurs de bases coiled‑coil (CC‑BE), incluant des variantes qui éditent le C (CC‑CBE), l'A (CC‑ABE) et des versions plus complexes capables d'effectuer différents types de substitutions. 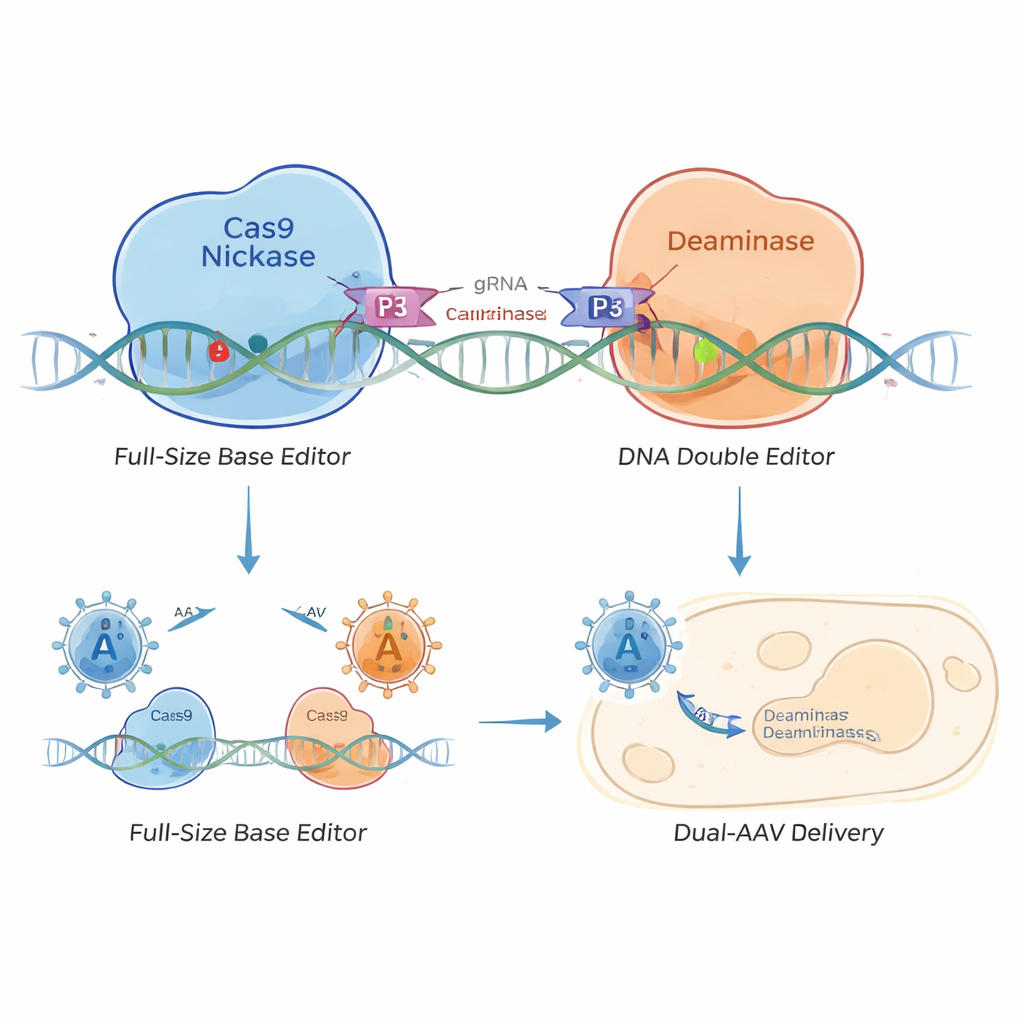
Édition flexible, puissante et précise
L'équipe a testé les CC‑BE dans plusieurs types cellulaires, y compris des cellules humaines et des cellules primaires porcines, et avec différentes formes de Cas9 reconnaissant une gamme plus large de séquences d'ADN. Les versions CC‑CBE non seulement fonctionnaient de manière fiable sur de nombreux sites, mais montraient aussi une « fenêtre d'édition » plus large, ce qui signifie qu'elles pouvaient modifier des lettres cibles sur une zone d'ADN plus étendue, offrant aux chercheurs plus de flexibilité dans le choix des ARN guides. Les versions CC‑ABE atteignaient une efficacité comparable aux meilleurs éditeurs d'adénine existants tout en produisant souvent moins de sous‑produits hors cible. Les chercheurs ont également adapté la stratégie coiled‑coil à des conceptions d'éditeurs plus récentes — comme le TadCBE compact et l'ABE9 précis — et ont de nouveau constaté que la scission des outils avec des paires coiled‑coil préservait ou améliorait les performances.
Des boîtes de culture aux souris vivantes
De façon cruciale, les auteurs ont montré que ces éditeurs scindés fonctionnent chez des animaux vivants en utilisant une délivrance par double AAV, où chaque particule virale transporte une moitié de l'éditeur. Chez la souris, un CC‑ABE ciblant le gène Pcsk9 dans le foie a obtenu des conversions A‑>G à des taux atteignant environ 70 %, réduisant fortement la protéine Pcsk9 et le cholestérol LDL sanguin sans signes de lésions hépatiques. 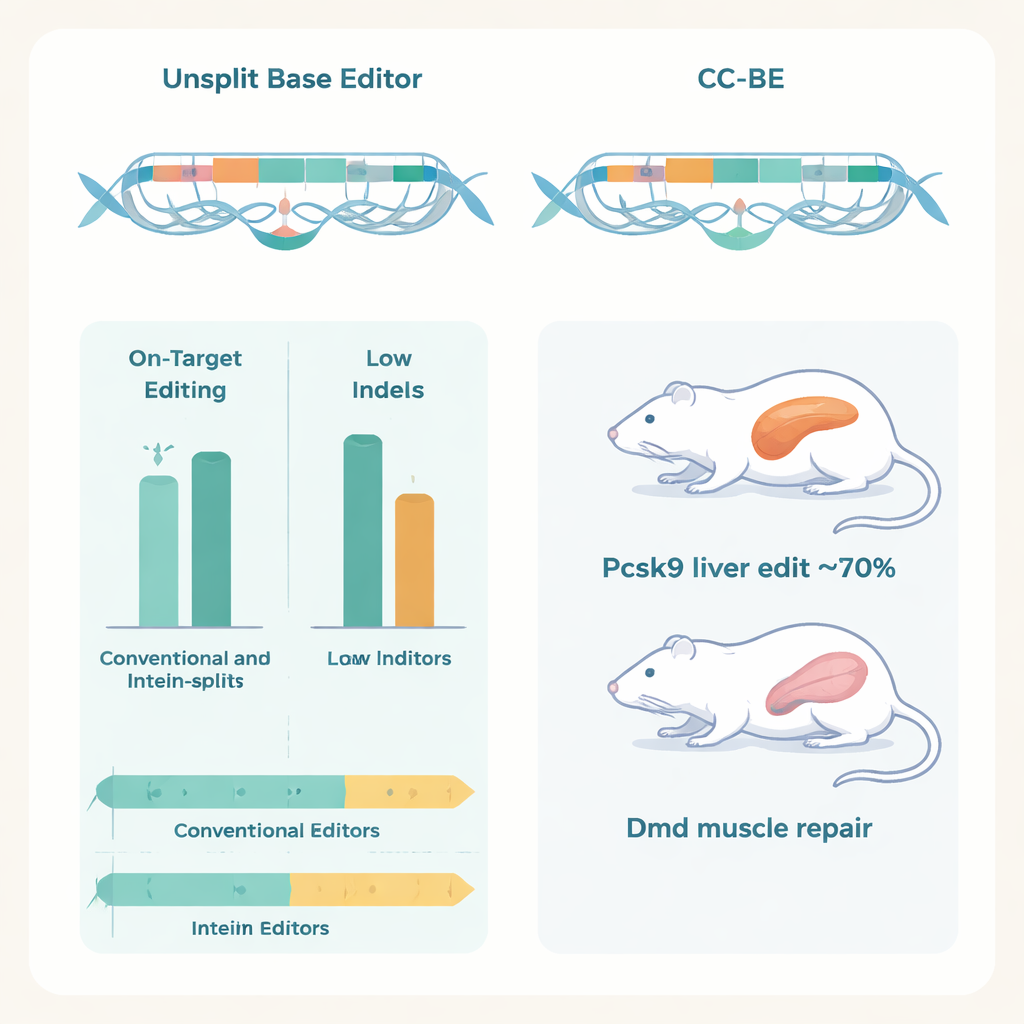
Une nouvelle voie vers une réparation de l'ADN applicable
Essentiellement, cette étude présente une astuce d'ingénierie simple mais puissante : utiliser de petits « crochets » coiled‑coil pour scinder de grands éditeurs de bases en modules de la taille compatible avec l'AAV qui ne se réunissent que là où ils sont nécessaires. Pour les non‑spécialistes, la conclusion est que les scientifiques peuvent désormais emballer des outils de réparation de l'ADN très performants dans des vecteurs viraux cliniquement éprouvés sans sacrifier la précision ni la puissance. Cette approche coiled‑coil pourrait faciliter la conception de traitements pour un large éventail de maladies génétiques dues à une seule lettre dans des organes comme le foie, le cœur et les muscles, rapprochant la correction génétique finement réglée des thérapies du monde réel.
Citation: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Mots-clés: édition de bases, thérapie génique, CRISPR, livraison par AAV, maladie génétique