Clear Sky Science · fr
Empreinte dépendante de H3K27me3 et régulation transcriptionnelle dans les premiers stades embryonnaires de la souris nécessitent la restriction de l’activité de PRC2 médiée par EZHIP
Pourquoi de minuscules embryons ont besoin d’une synchronisation génétique précise
Tout mammifère commence sa vie comme une seule cellule qui porte un jeu de chromosomes provenant de la mère et un jeu provenant du père. Bien que ces deux jeux contiennent presque les mêmes lettres d’ADN, ils arrivent emballés dans des marques chimiques différentes qui contribuent à décider quels gènes s’activent ou se taisent. Cette étude examine comment un de ces systèmes d’étiquetage est maintenu en équilibre durant les premiers jours après la fécondation chez la souris, et pourquoi perturber cet équilibre peut faire dérailler le développement normal.
Deux parents, deux génomes emballés différemment
Chez les mammifères, certains gènes se comportent différemment selon qu’ils proviennent de la mère ou du père, un phénomène appelé empreinte génomique. L’empreinte classique repose sur des marques chimiques directement sur l’ADN, mais ces dernières années les chercheurs ont découvert un second type, plus éphémère, qui dépend d’une modification des protéines histones appelée H3K27me3. Ces histones agissent comme des bobines autour desquelles l’ADN s’enroule, et H3K27me3 tend à réprimer les gènes voisins. Dans les embryons de souris normaux, le génome maternel porte davantage de cette marque que le génome paternel juste après la fécondation, ce qui contribue à silencier certaines copies maternelles de gènes tout en laissant fonctionner les copies paternelles.
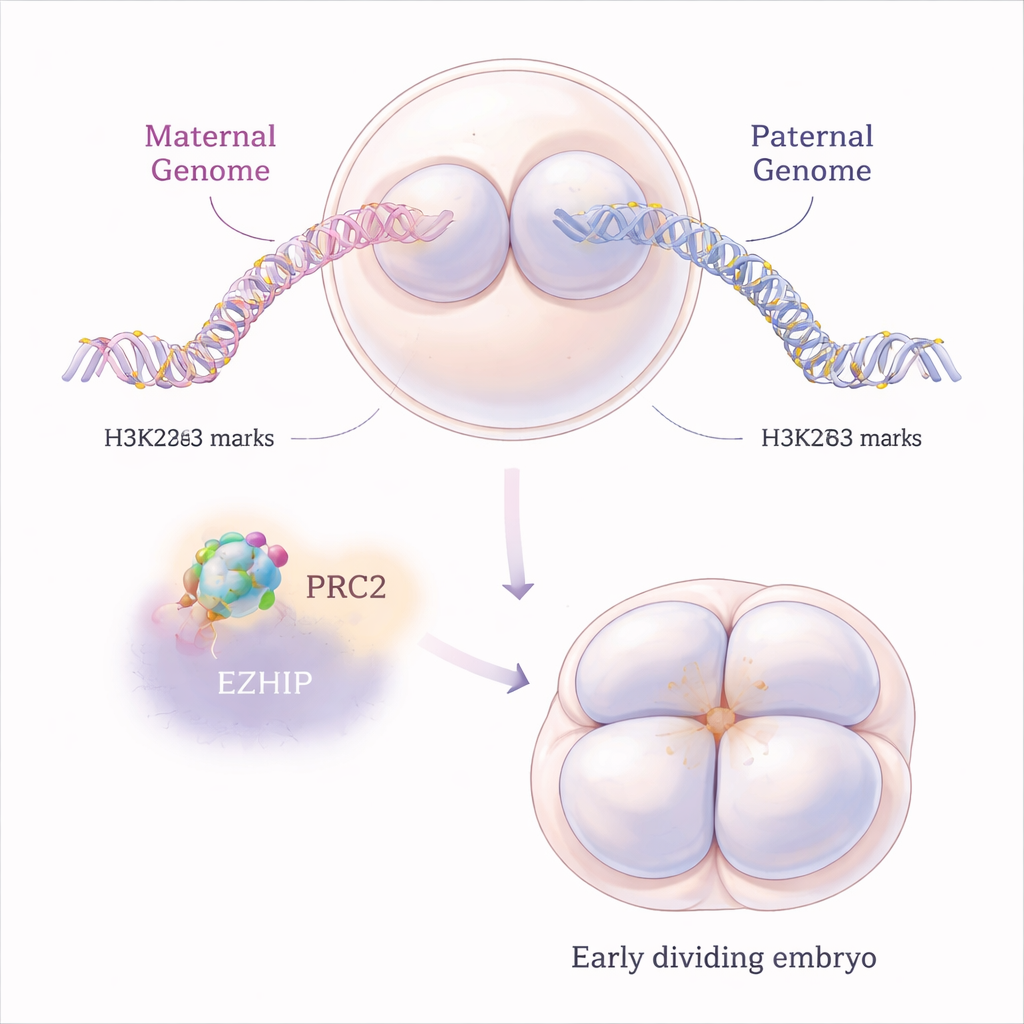
Un frein moléculaire sur un puissant répresseur
H3K27me3 est apposée sur la chromatine par une grande machinerie protéique appelée PRC2. Les auteurs se sont focalisés sur EZHIP, une protéine moins connue qui se lie à PRC2 et en ralentit l’activité. Les ovocytes de souris produisent beaucoup d’ARN Ezhip, et la protéine EZHIP résultante persiste dans les embryons pendant les premières divisions cellulaires. En étudiant des souris dont les mères sont dépourvues d’Ezhip, les chercheurs ont cherché à savoir ce qui se passe lorsque ce frein naturel est retiré. Ils ont constaté que, sans EZHIP, les ovules et les premiers embryons accumulaient des marques H3K27me3 supplémentaires, mais d’une manière étonnamment « aplatie » : au lieu de domaines nets et bien définis, la marque répressive se répandait plus largement et estompait les motifs normaux, affectant à la fois les chromosomes maternels et paternels.
Quand trop de répression casse l’empreinte
En utilisant des méthodes sensibles de cartographie du génome, l’équipe a montré que l’asymétrie habituelle entre les paysages H3K27me3 maternel et paternel est en grande partie perdue dans les embryons issus d’ovules déficients en Ezhip. De nombreuses régions qui conservent normalement H3K27me3 sur une seule copie parentale en ont maintenant sur les deux, ou voient leurs motifs diffusés. Ce changement a eu des conséquences importantes pour les gènes imprintés normalement contrôlés par H3K27me3 plutôt que par la méthylation de l’ADN. Dans les embryons témoins, ces gènes sont généralement exprimés principalement depuis l’allèle paternel. Dans les embryons dépourvus d’EZHIP maternel, en revanche, ces mêmes gènes s’exprimaient souvent depuis les deux copies parentales, et les niveaux d’ARN de beaucoup d’entre eux augmentaient au lieu d’être doublement réprimés.
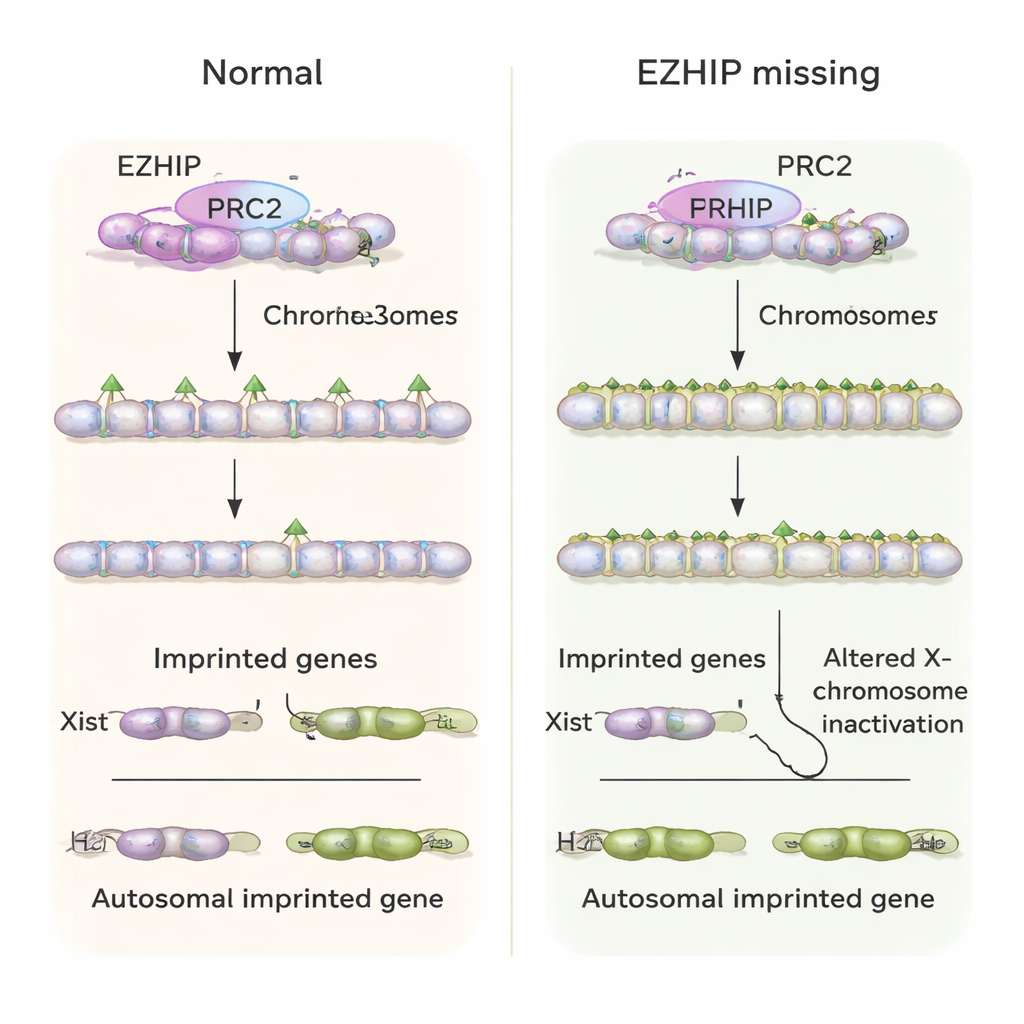
Contrôle perturbé du chromosome X et santé de l’embryon
Un gène imprinté clé dépendant de H3K27me3 est Xist, un long ARN qui enrobe et inactive un chromosome X dans les cellules femelles pour équilibrer la dose génique avec les mâles. Normalement, les embryons de souris précoces expriment Xist uniquement depuis le X paternel chez les femelles, et pas du tout chez les mâles. En l’absence d’EZHIP maternel, les auteurs ont observé que les embryons femelles exprimaient fréquemment Xist depuis les deux chromosomes X, tandis que les embryons mâles activaient « inappropriément » Xist depuis leur unique X. Cela a entraîné des schémas d’inactivation anormaux des gènes liés au X. Au niveau de l’organisme entier, les souris nées de mères déficientes en Ezhip étaient moins nombreuses, et les embryons présentaient une croissance altérée ainsi que des problèmes dans les tissus extra-embryonnaires qui soutiennent le placenta, cohérents avec un stress développemental persistant causé par l’échec précoce de l’empreinte.
Trop d’une bonne chose peut être nuisible
Pour un non-spécialiste, il peut sembler intuitif que davantage d’une marque de répression comme H3K27me3 réduirait simplement l’activité de plus de gènes. Au contraire, ce travail montre qu’une surcharge du génome par ces marques, lorsqu’elles sont disposées de manière inappropriée, peut en réalité compromettre leur capacité à agir comme des interrupteurs précis. En supprimant EZHIP, les chercheurs ont libéré PRC2, provoquant une propagation si large de H3K27me3 que les signaux d’empreinte se sont estompés et que des régulateurs critiques comme Xist ont été mal contrôlés. L’étude souligne que les embryons précoces dépendent non seulement de la présence des bonnes molécules, mais aussi d’un réglage fin de leurs activités afin que les génomes maternel et paternel soient lus dans le juste équilibre.
Citation: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
Mots-clés: épigénétique, empreinte génomique, développement embryonnaire précoce, inactivation du chromosome X, Polycomb PRC2