Clear Sky Science · fr
Exploiter l’immunité entraînée induite par le glucane pour le rééquipement épigénétique et métabolique des macrophages afin d’améliorer la réponse vaccinale contre le cancer colorectal
Réveiller les premiers intervenants de l’organisme
Le cancer colorectal est l’un des cancers les plus meurtriers au monde, et la plupart des patients ne bénéficient pas des immunothérapies actuelles. Cette étude explore une idée intrigante : et si l’on pouvait « entraîner » le système immunitaire inné — les premiers intervenants de l’organisme — à se souvenir du danger et à aider les vaccins à mieux lutter contre les tumeurs colorectales ? En utilisant un sucre naturel issu de la levure, le bêta‑glucane, les chercheurs montrent comment les cellules immunitaires précoces peuvent être reprogrammées pour que les vaccins anticancéreux déclenchent des attaques sur les tumeurs plus puissantes et plus durables.
Pourquoi le cancer colorectal a besoin de nouvelles défenses
Le cancer colorectal cause près d’un million de décès chaque année dans le monde, et les cas chez les jeunes adultes augmentent. Les traitements standards comme la chirurgie, la chimiothérapie et la radiothérapie peuvent être efficaces, mais de nombreux patients rechutent et subissent des effets secondaires importants. Les médicaments immunitaires récents, comme les inhibiteurs de points de contrôle, fonctionnent très bien uniquement dans un petit sous‑groupe de cancers colorectaux présentant des défauts particuliers de réparation de l’ADN. Pour la majorité des patients, ces médicaments et même les vaccins anticancéreux expérimentaux sont insuffisants parce que le microenvironnement tumoral est dominé par des cellules et des signaux qui atténuent l’attaque immunitaire.
Apprendre de nouveaux tours à l’immunité innée
Les cellules du système immunitaire inné — en particulier les macrophages — réagissent normalement vite mais brièvement aux menaces et sont considérées comme dépourvues de mémoire. Cependant, des travaux de la dernière décennie ont mis en évidence l’« immunité entraînée », où un stimulus initial fort laisse des traces durables sur ces cellules, leur permettant de répondre plus vigoureusement ultérieurement. Les auteurs ont utilisé le bêta‑glucane, un composant de la paroi des levures, pour induire cet état entraîné. Chez la souris, un traitement bref avec des particules entières de bêta‑glucane a reprogrammé les macrophages tant au niveau de l’activité génique que du métabolisme cellulaire. Lorsque ces animaux entraînés ont ensuite reçu un vaccin contre le cancer colorectal basé sur un adénovirus modifié (appelé PeptiCrad), leur système immunitaire a produit des lymphocytes T cytotoxiques plus puissants, meilleurs pour reconnaître et attaquer des cibles spécifiques de la tumeur. 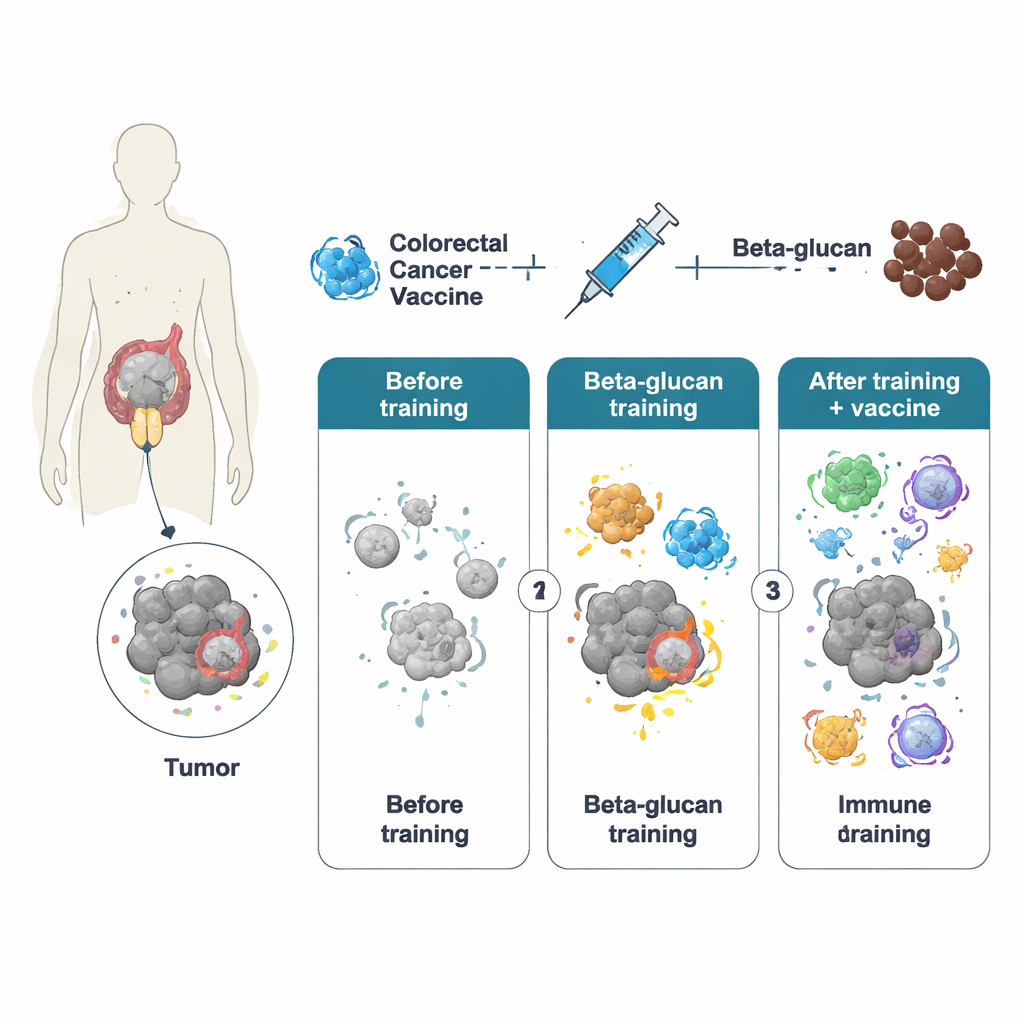
Reconfigurer l’énergie et la communication à l’intérieur des tumeurs
En creusant davantage, les chercheurs ont isolé des cellules immunitaires provenant des tumeurs et ont profilé leur métabolisme et leur activité génique cellule par cellule. Ils ont constaté que les macrophages entraînés passaient à un mode métabolique de haute intensité ressemblant à l’effet Warburg, où les cellules consomment rapidement du sucre et détournent des ressources vers des éléments de construction pour la croissance et la fonction. Ces cellules ont aussi augmenté le métabolisme de la créatine — mieux connu dans le contexte des compléments sportifs — ce qui a aidé à fournir l’énergie supplémentaire nécessaire à la production de molécules inflammatoires. Parallèlement, des marques chimiques spécifiques sur les protéines associées à l’ADN (notamment une augmentation de H3K4me3) ont marqué les gènes impliqués dans la production de chimiokines, verrouillant de fait un programme pro‑inflammatoire et anti‑tumoral qui a perduré dans le temps.
Construire une équipe de relais immunitaire
Le séquençage unicellulaire a révélé une succession en relais entre différentes cellules immunitaires à l’intérieur de la tumeur. D’abord, les macrophages entraînés ont libéré de fortes quantités de deux signaux clés, CXCL9 et CXCL10, qui ont attiré les cellules tueuses naturelles (NK) via un récepteur appelé CXCR3. Une fois recrutées, ces cellules NK n’ont pas seulement tué les cellules cancéreuses ; elles ont aussi sécrété un autre messager, CCL5, qui a attiré un sous‑ensemble spécialisé de cellules dendritiques connu sous le nom de cDC1. Ces cellules dendritiques excellent dans la présentation des fragments tumoraux aux lymphocytes T. En conséquence, plus de lymphocytes T CD8 sont devenus activés et ont basculé vers des cellules mémoiré effectrices — des cellules qui répondent rapidement et vigoureusement lors d’une nouvelle rencontre avec la tumeur. Bloquer l’utilisation de la créatine, épuiser les macrophages ou les cellules NK, ou interrompre ces voies de chimiokines affaiblissait le contrôle tumoral, soulignant combien le succès du vaccin dépendait de ce circuit macrophage–NK–dendritique–T. 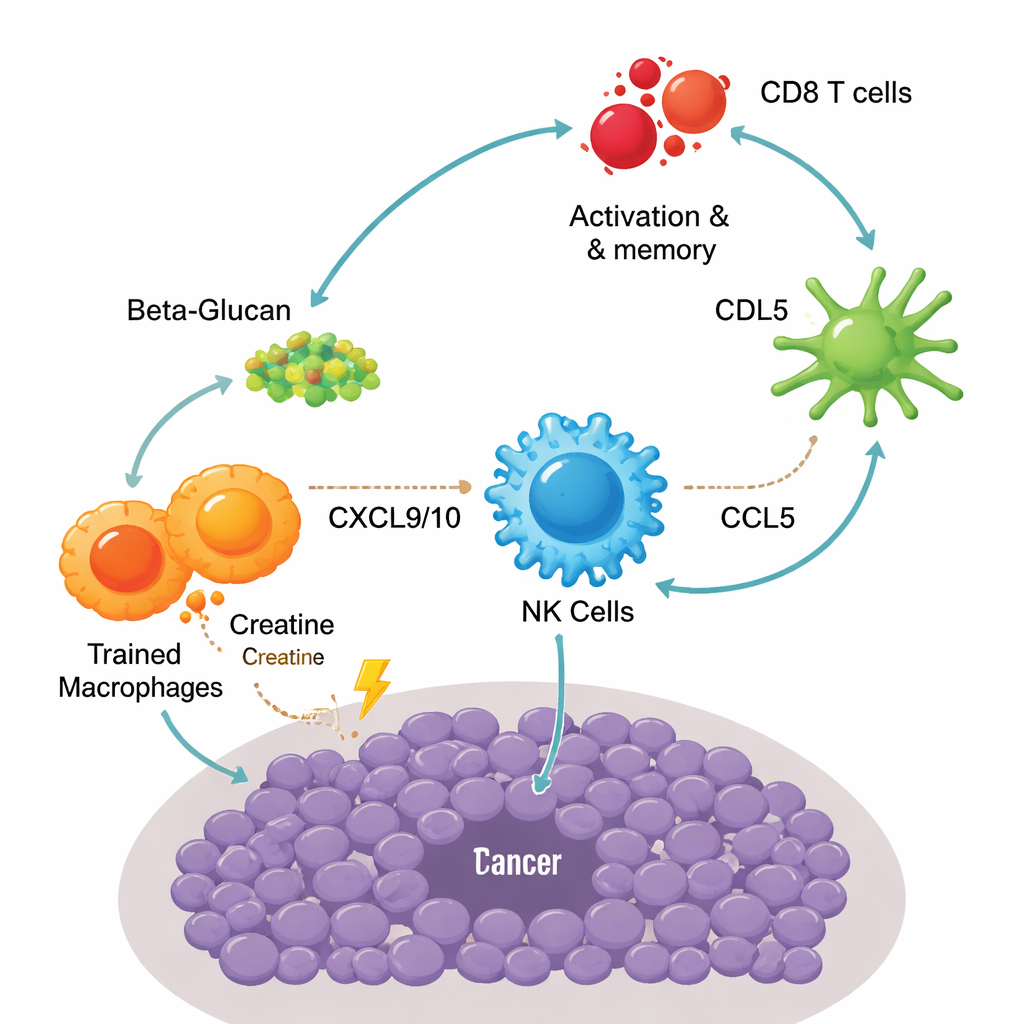
Des modèles murins aux organoïdes tumoraux humains
L’équipe a testé son approche dans plusieurs modèles murins de cancer colorectal, y compris un type particulièrement tenace qui résiste aux immunothérapies courantes. Dans chaque cas, la combinaison de l’entraînement au bêta‑glucane et du vaccin ralentissait la croissance tumorale plus efficacement que chaque traitement pris séparément. Surtout, ils sont allés au‑delà des souris. Des cellules sanguines humaines exposées au bêta‑glucane se sont montrées meilleures pour répondre à un peptide vaccinal contre le cancer colorectal, produisant davantage de cytokines stimulant l’immunité. Lorsque ces cellules immunitaires entraînées ont été amplifiées puis cocultivées avec de mini‑tumeurs colorectales dérivées de patients (organoïdes), elles ont tué plus de cellules cancéreuses que des cellules non entraînées. L’enlèvement des monocytes et macrophages humains du système effaçait cet avantage, confirmant que ces cellules entraînées sont des organisateurs essentiels plutôt que de simples tueurs directs de tumeurs.
Ce que cela pourrait signifier pour les vaccins anticancéreux futurs
En termes simples, ce travail montre qu’un sucre sûr dérivé de la levure peut « coacher » les cellules immunitaires innées pour soutenir une vaccination contre le cancer colorectal plus efficace. En reconfigurant la manière dont les macrophages utilisent l’énergie et quels gènes ils gardent prêts à l’action, l’entraînement au bêta‑glucane déclenche un effet domino : les macrophages appellent les cellules NK, les NK recrutent des cellules dendritiques expertes, et ensemble elles forment une armée renforcée de lymphocytes T CD8 mémoire. Bien que beaucoup reste à tester en essais cliniques — notamment la sécurité, le calendrier et les meilleures combinaisons vaccinales — l’immunité entraînée apparaît ici comme une stratégie adjuvante prometteuse pour transformer davantage de tumeurs colorectales « froides » et suppressives en cibles que le système immunitaire peut reconnaître et contrôler.
Citation: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
Mots-clés: immunothérapie du cancer colorectal, immunité entraînée, bêta‑glucane, macrophages et cellules NK, vaccins anticancéreux