Clear Sky Science · fr
Criblage CRISPR in vivo identifie des membres du complexe SAGA comme régulateurs clés de l'hématopoïèse
Pourquoi il est important de maintenir l'équilibre de la production de sang
Chaque jour, votre organisme fabrique discrètement des centaines de milliards de nouvelles cellules sanguines qui transportent l'oxygène, combattent les infections et arrêtent les saignements. Cette production continue repose sur de rares « cellules mères » dans la moelle osseuse, appelées cellules souches hématopoïétiques. Quand la machinerie qui contrôle ces cellules se dérègle, des personnes peuvent développer une anémie, une immunité affaiblie ou des cancers comme la leucémie. Cette étude pose une question simple mais puissante : parmi les milliers de gènes de notre génome, lesquels sont réellement essentiels pour maintenir une production de cellules sanguines saine et équilibrée ?
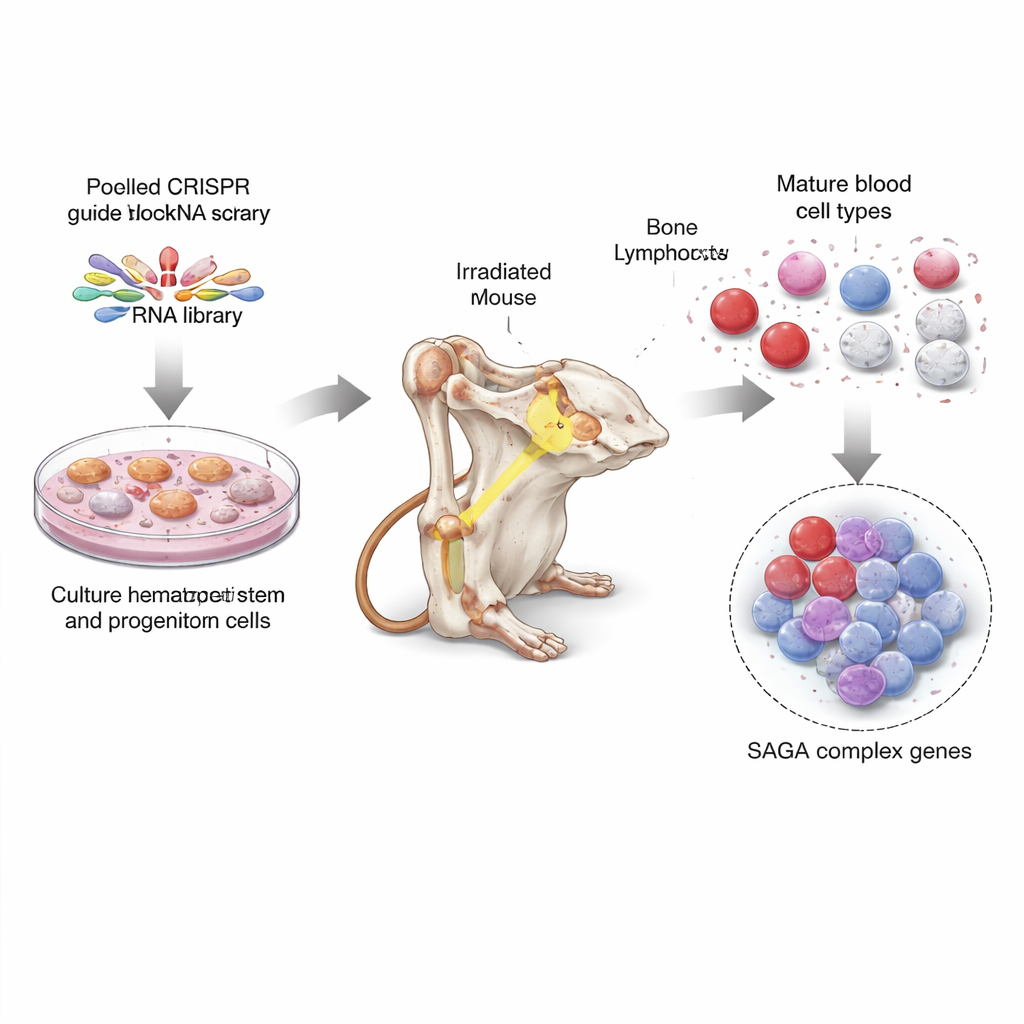
Une chasse au trésor à l'échelle du génome dans les cellules souches de souris
Pour répondre à cela, les chercheurs ont utilisé CRISPR, l'outil d'édition génétique souvent comparé à des ciseaux moléculaires, pour éteindre presque chaque gène du génome de la souris, dix guides par gène. Ils ont d'abord cultivé en grand nombre des cellules souches et progénitrices de la moelle osseuse dans des conditions de culture spéciales, puis ont infecté ces cellules avec des banques de guides CRISPR de façon à ce que chaque cellule porte l'inactivation d'un gène différent. Ensuite, ils ont transplanté ces cellules modifiées et mélangées dans des dizaines de souris irradiées, permettant aux cellules éditées de reconstruire le système sanguin des animaux. Des mois plus tard, ils ont purifié divers types cellulaires sanguins matures et des cellules de type souche de la moelle osseuse et ont lu quelles guides CRISPR étaient sur- ou sous‑représentés. Cela a révélé quelles pertes de gènes favorisaient les cellules immatures et lesquelles soutenaient la production de cellules sanguines pleinement formées.
Un centre de contrôle caché appelé SAGA se précise
Parmi de nombreux régulateurs connus de la formation du sang, un ensemble surprenant de hits est apparu : plusieurs éléments structurels d'une grande assemblée protéique appelée complexe SAGA, y compris des gènes nommés Tada2b, Taf5l et Tada1. SAGA ne fabrique pas directement les cellules sanguines ; il aide plutôt à activer ou réprimer d'autres gènes en marquant chimiquement les protéines d'emballage de l'ADN appelées histones. Lorsque l'équipe a inactivé individuellement ces composants de SAGA et transplanté les cellules éditées chez des souris, ils ont observé un schéma constant. Les cellules immatures de la moelle osseuse s'accumulaient, mais leur capacité à maturer en globules blancs circulants, globules rouges et certains types de cellules immunitaires était fortement réduite. En substance, les cellules souches et progénitrices restaient bloquées dans un goulot d'étranglement, incapables d'achever le parcours jusqu'à des cellules sanguines pleinement fonctionnelles.
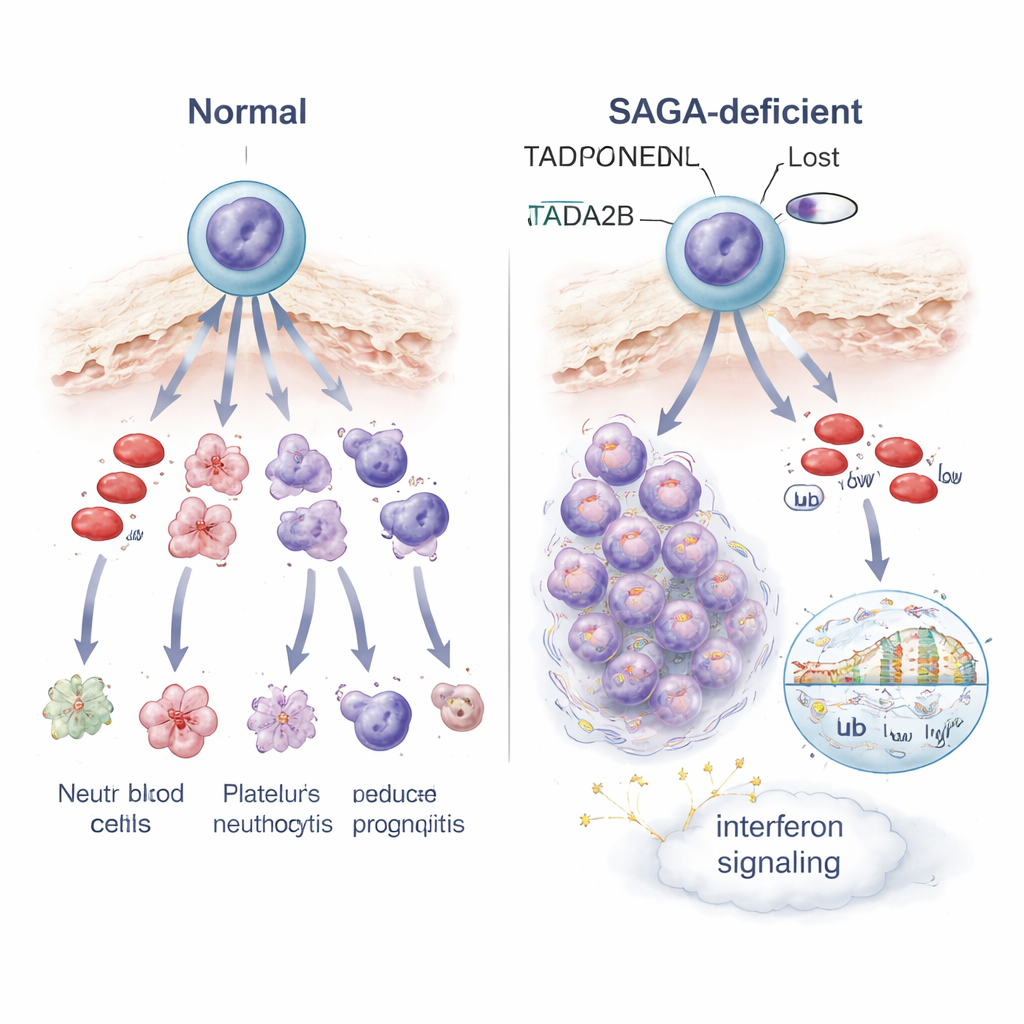
Comment un contrôle génétique perturbé modifie le destin cellulaire et les signaux de stress
Pour comprendre ce qui tourne mal à l'intérieur de ces cellules bloquées, les scientifiques ont profilé l'activité génique cellule par cellule et en population. La perte de Tada2b ou de Taf5l a réorienté l'activité de nombreux gènes dans les cellules souches, avec deux thèmes marquants. D'une part, des gènes impliqués dans la signalisation par l'interféron — normalement partie de la défense antivirale de l'organisme — étaient activés, indiquant une alarme interne ou un état de stress. D'autre part, les mitochondries des cellules, les petites centrales énergétiques qui alimentent le travail cellulaire, sont devenues moins actives, et les cellules altérées se sont montrées plus sensibles à un médicament qui cible la production d'énergie mitochondriale. Au niveau du conditionnement de l'ADN, les cellules dépourvues de Tada2b présentaient des niveaux réduits d'une marque d'histone associée à une chromatine ouverte et active, ainsi que des modifications d'une autre marque liée à la lecture des gènes. Ces changements dans la chimie de la chromatine expliquent probablement en partie pourquoi de nombreux gènes, y compris ceux qui guident la maturation correcte du sang, sont mal régulés.
Des mécanismes fondamentaux aux modèles de maladie
L'équipe a ensuite examiné si augmenter ou diminuer l'activité de SAGA pouvait inverser ces effets. Forcer les cellules à produire plus de Tada2b a réduit l'activité des gènes liés à l'interféron et diminué la proportion de cellules de type souche, l'image miroir de l'inactivation. Traiter des cellules souches normales avec un médicament inhibant les sous‑unités enzymatiques clés de SAGA a reproduit une grande partie du profil de perte de Tada2b, renforçant l'idée que l'activité de modification de la chromatine de SAGA est centrale à sa fonction. Enfin, les chercheurs se sont tournés vers un modèle cellulaire humain du syndrome myélodysplasique, un état pré‑leucémique dans lequel la production de sang faiblit et où les voies d'interféron sont souvent élevées. Lorsqu'ils ont inactivé des composants de SAGA dans ces cellules humaines et les ont transplantées dans des souris immunodéficientes, les cellules éditées ont gagné un avantage de croissance et ont de nouveau activé des programmes géniques liés à l'interféron et au lignage myéloïde, suggérant que ce centre régulateur influence aussi le comportement de la maladie.
Ce que cela signifie pour la santé du sang et les thérapies futures
Pour le lecteur non spécialiste, le message principal est que cette étude révèle un centre de contrôle puissant — le complexe SAGA — qui aide les cellules souches hématopoïétiques à décider quand rester immatures, quand mûrir et comment éviter des réponses de stress délétères. Lorsque des parties clés de SAGA manquent, les cellules souches s'accumulent mais ne parviennent pas à produire suffisamment de cellules sanguines opérationnelles, tandis que les signaux de stress et de type antiviral augmentent et que les mitochondries défaillent. Ces découvertes approfondissent non seulement notre compréhension de la manière dont la production de sang saine est maintenue au cours de la vie, mais suggèrent aussi que des variations subtiles de l'activité de SAGA pourraient contribuer à des troubles sanguins liés à l'âge et à des maladies comme le syndrome myélodysplasique. À long terme, cartographier ce circuit de contrôle pourrait aider les scientifiques à concevoir des thérapies visant à ramener les cellules souches défaillantes vers une production sanguine équilibrée et résiliente.
Citation: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Mots-clés: cellules souches hématopoïétiques, criblage CRISPR, complexe SAGA, signalisation par l'interféron, syndrome myélodysplasique