Clear Sky Science · fr
Administration intranasale d’un inhibiteur peptidique macrocyclique à large spectre protégeant contre les variants Omicron du SARS-CoV-2
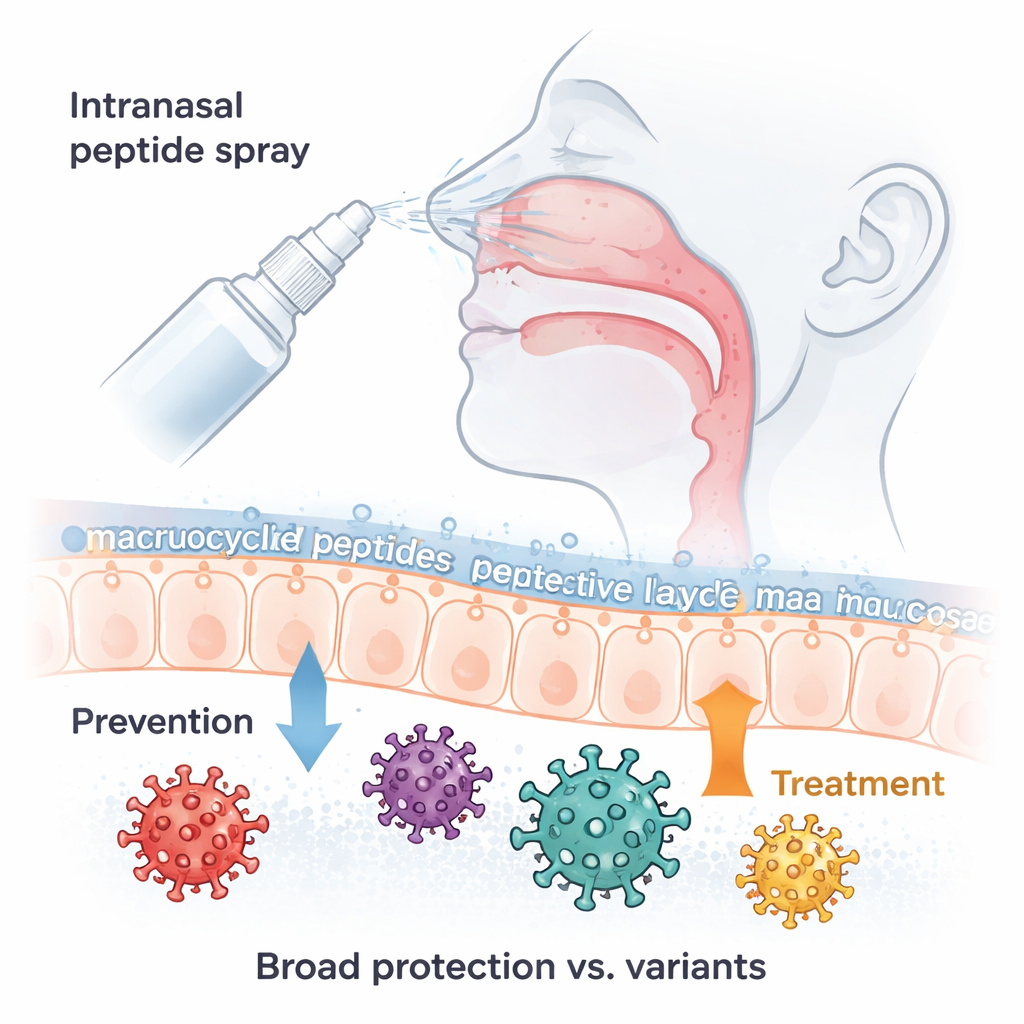
Pourquoi un spray nasal contre la COVID reste important
Même si l’urgence pandémique due à la COVID-19 est désormais terminée, le virus responsable, le SARS-CoV-2, continue d’infecter et de tuer des personnes dans le monde, en particulier les personnes âgées et celles dont le système immunitaire est affaibli. De nouveaux variants comme Omicron continuent d’évoluer et de contourner nos vaccins et nos traitements par anticorps. Cette étude décrit un nouveau type de médicament : une petite molécule en forme d’anneau administrée sous forme de spray nasal simple, capable de bloquer une large gamme de variants Omicron et d’autres variants du SARS-CoV-2 avant qu’ils ne s’installent, et pouvant aussi aider à traiter l’infection après son démarrage.
Transformer des anneaux conçus en bloqueurs du virus
Les chercheurs se sont concentrés sur les peptides macrocycliques — de petits fragments protéiques en forme d’anneau déjà considérés comme des candidats-médicaments prometteurs car ils peuvent saisir fortement leurs cibles, pénétrer les tissus et sont relativement faciles à produire. En utilisant une plateforme de criblage puissante appelée système RaPID, ils ont construit et testé d’immenses banques de ces anneaux pour trouver ceux qui se fixent sur une région critique de la protéine spike du coronavirus, le domaine de liaison au récepteur (RBD). De cette recherche, ils ont identifié un composé principal nommé 6L3 puis l’ont amélioré progressivement par des modifications précises de ses acides aminés, créant finalement des variantes beaucoup plus puissantes nommées 6L3-3P et 6L3-3P11K qui bloquent fortement l’infection par de nombreux sous-variants Omicron en culture cellulaire.
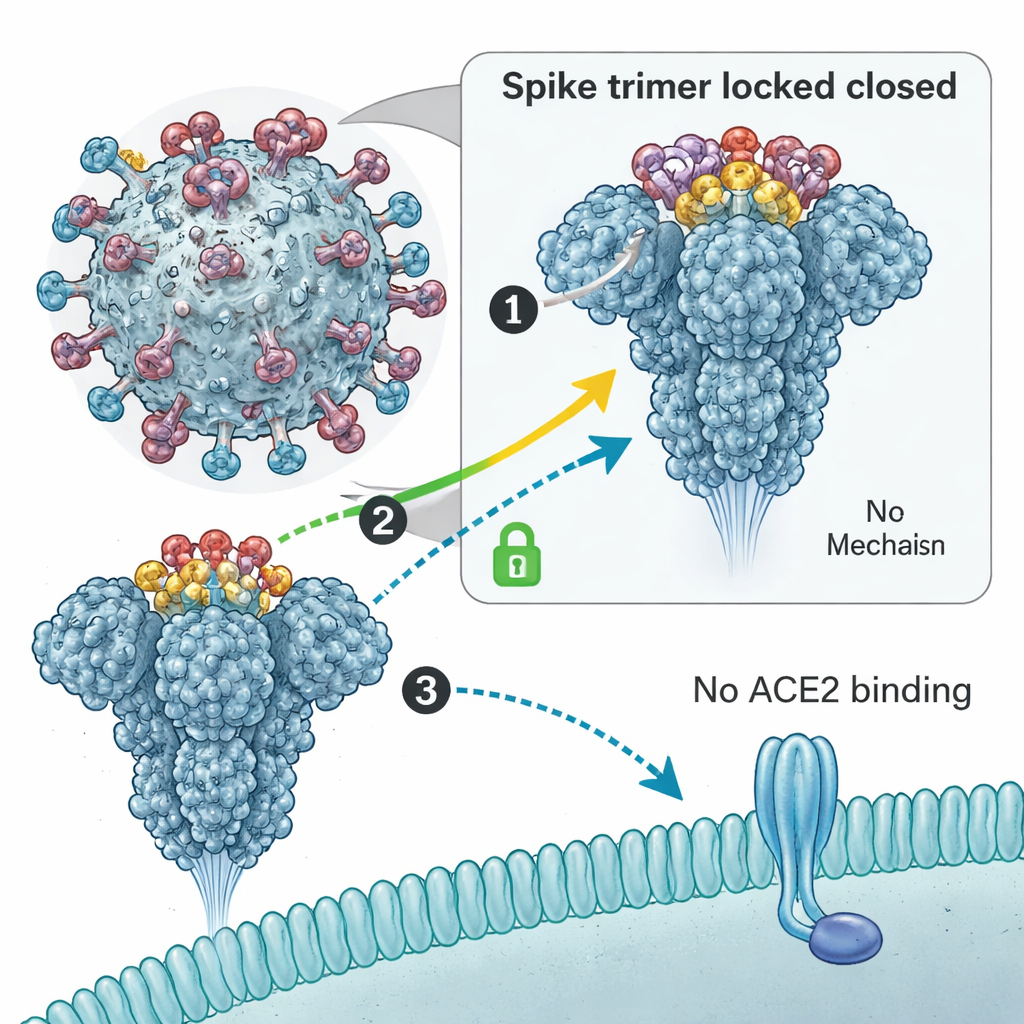
Coller la spike en position fermée
Pour comprendre comment ces anneaux stoppent le virus, l’équipe a utilisé la cryo-microscopie électronique pour les visualiser liés à la protéine spike avec un grand niveau de détail. Ils ont découvert que trois copies du peptide macrocyclique se regroupent en un petit trimère qui s’insère dans une cavité au sommet de la spike constituée de trois RBD. Cela agit comme de la colle moléculaire, verrouillant les trois RBD dans une position « vers le bas » ou fermée. Dans cette posture, la spike ne peut pas relever l’un de ses RBD pour saisir le récepteur ACE2 de nos cellules — une première étape nécessaire à l’infection. Des mesures biophysiques ont confirmé que, en présence du peptide, les spikes perdent leur capacité de se lier à ACE2. Fait important, le peptide cible une région conservée qui n’est pas le site d’attache habituel des anticorps, ce qui signifie que les mutations courantes observées dans les variants ont jusqu’à présent laissé cette cavité largement inchangée.
Du plat de culture aux tissus humains simulés et aux souris
Fort des informations structurales, les scientifiques ont affiné la molécule pour la rendre à la fois plus puissante et plus stable dans l’organisme. Une version finale optimisée, 6L3-1F3P11hR, résiste à la dégradation enzymatique, tolère la chaleur et des pH différents, et reste majoritairement dans les voies nasales lorsqu’elle est pulvérisée chez la souris, minimisant l’exposition du reste de l’organisme. Dans des organoïdes nasaux humains cultivés en laboratoire — cultures tridimensionnelles qui reproduisent la muqueuse nasale réelle — ce peptide a fortement réduit la réplication des récents variants Omicron même à faible dose. Chez des souris génétiquement modifiées exprimant l’ACE2 humain et développant une maladie pulmonaire sévère proche de la COVID, une administration intranasale du peptide, soit peu avant soit peu après l’infection, a réduit les niveaux de virus dans le nez et les poumons, protégé le tissu pulmonaire des dégâts, et a obtenu des résultats comparables à la pilule antivirale approuvée nirmatrelvir (composant de Paxlovid) dans ces essais.
Prendre de l’avance sur les variants futurs
Parce que le peptide se lie à une zone « non liée au récepteur » de la spike qui est fortement conservée et agit par un mécanisme de verrouillage physique plutôt qu’en ciblant une enzyme virale unique, il pourrait être plus difficile pour le virus d’échapper à ce blocage sans nuire à sa propre capacité d’infection. Les auteurs montrent aussi que de simples substitutions ponctuelles dans la séquence peptidique peuvent ajuster sa puissance et son spectre d’action, ce qui suggère une voie pour adapter le médicament contre des coronavirus apparentés à l’avenir. Leurs études pharmacocinétiques indiquent que le composé se concentre là où le virus atterrit d’abord — les voies nasales — en faisant un candidat logique pour un spray préventif ou un traitement précoce utilisable à domicile.
Ce que cela pourrait signifier pour la protection quotidienne
Pour les non-spécialistes, l’essentiel est que ce travail propose un candidat antiviral bien caractérisé, administré par le nez, qui pince physiquement la spike du coronavirus pour l’empêcher de se fixer sur nos cellules. En cellules, dans des tissus nasaux proches du tissu humain, et dans un modèle de souris susceptible, le peptide macrocyclique optimisé a nettement réduit les niveaux viraux et les lésions pulmonaires sur de nombreux sous-variants Omicron et quelques souches antérieures. Alors que des essais cliniques chez l’humain restent nécessaires, cette stratégie ouvre la voie à un futur où un spray nasal stable à température ambiante pourrait offrir une protection et un traitement à la demande contre les variants actuels et émergents du SARS-CoV-2, et peut‑être contre d’autres coronavirus apparentés.
Citation: Wang, M., Yang, J., Tan, Y. et al. Intranasal administration of broad-spectrum macrocyclic peptide inhibitor protects against SARS-CoV-2 Omicron variants. Nat Commun 17, 1753 (2026). https://doi.org/10.1038/s41467-026-68462-9
Mots-clés: COVID-19, variants du SARS-CoV-2, spray nasal antiviral, inhibiteur de la protéine spike, peptide macrocyclique