Clear Sky Science · fr
Inférer l’architecture de la chromatine à un locus unique par localisation probabiliste de l’ADN in situ
Comment la forme 3D de l’ADN contrôle l’activation des gènes
On représente souvent notre ADN comme une échelle droite, mais à l’intérieur des cellules il se replie en boucles et en enroulements complexes. Ces formes comptent : elles contribuent à décider quels gènes s’allument, quand et où. Cette étude présente une nouvelle manière d’observer les minuscules agencements tridimensionnels de l’ADN autour d’un gène unique dans des embryons de mouche en développement, révélant comment de subtils changements dans le repliement de l’ADN peuvent modifier les motifs d’activité génique qui façonnent le plan corporel.
Observer le contrôle génique dans un embryon en développement
Lorsqu’un embryon se développe, des milliers de gènes doivent s’activer ou se réprimer aux moments précis. Beaucoup de ces décisions sont prises par de courtes séquences d’ADN appelées enhanceurs, qui peuvent se trouver à des dizaines de milliers de bases du gène qu’ils contrôlent. Pour fonctionner, les enhanceurs doivent s’approcher physiquement de leur gène cible dans l’espace 3D, formant des boucles de l’ADN pour que des sites éloignés se touchent. Mais ces boucles sont minuscules, dynamiques et difficiles à voir. Les auteurs se sont concentrés sur un gène unique, brinker (brk), chez la mouche Drosophila. Ce gène contribue au modelage de l’embryon précoce, s’activant en une bande le long du côté de l’oeuf. Trois éléments de contrôle voisins — deux enhanceurs (E1 et E2) et un élément promoteur‑proche (PPE) adjacent au gène — coopèrent pour produire ce motif précis.
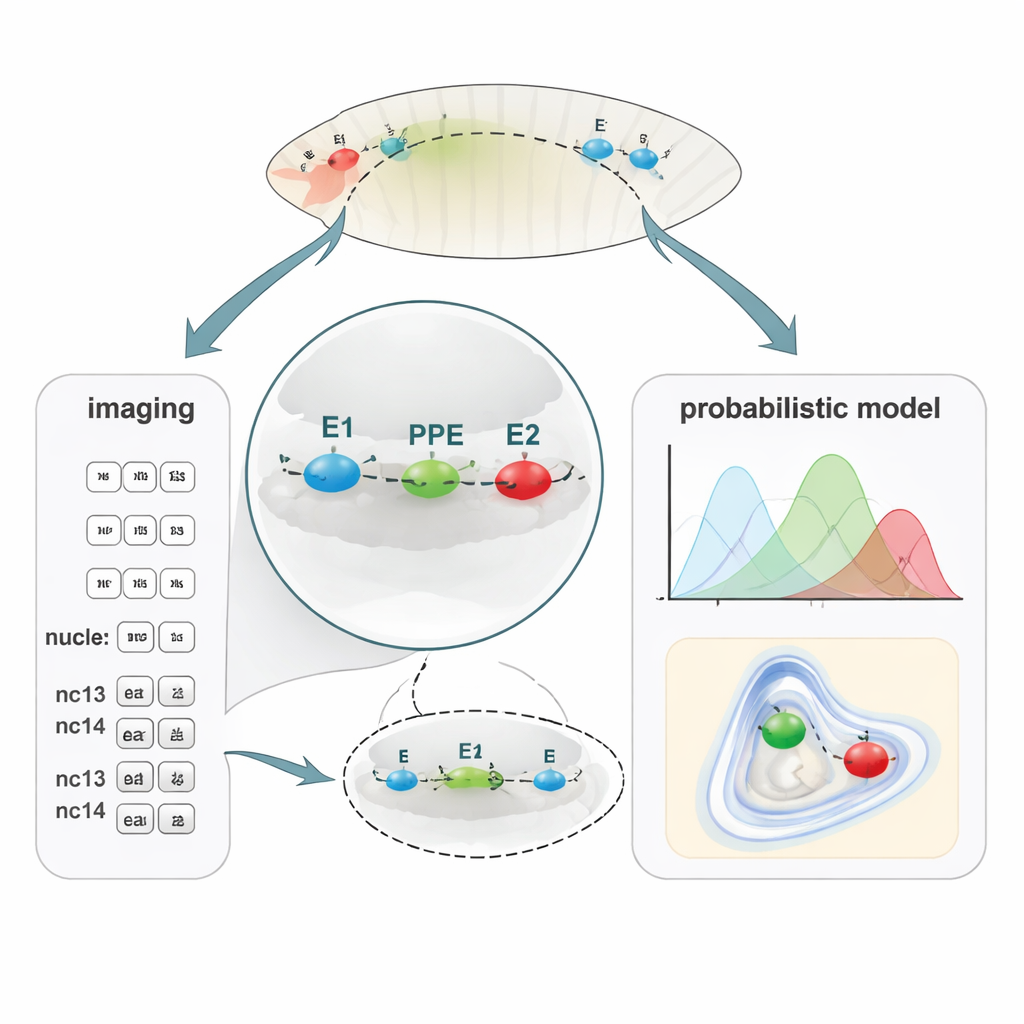
Une nouvelle manière de cartographier des distances d’ADN infimes
Pour relier le repliement de l’ADN à l’activité génique, l’équipe a développé PLOTTED (Probabilistic Localization of Oligopaint Tagged Target Element Distances). D’abord, ils ont utilisé une méthode de marquage de l’ADN appelée Oligopaint FISH pour attacher trois colorants fluorescents différents aux régions E1, PPE et E2 dans des embryons de mouche fixés. À l’aide d’un microscope confocal en super‑résolution, ils ont mesuré des distances 3D entre ces trois points colorés dans des dizaines de milliers de noyaux à travers des embryons à des cycles nucléaires successifs, depuis juste avant le début de l’activité génique (pré‑nc13) jusqu’à des stades ultérieurs (nc13 et nc14). Ils ont ensuite alimenté toutes ces distances dans une chaîne de traitement computationnelle sur mesure qui filtre les mesures bruitées et construit des cartes de probabilité montrant où chaque élément est le plus susceptible de se situer par rapport aux autres. Plutôt que de produire une unique « boucle » statique, PLOTTED génère un paysage des formes de chromatine probables à chaque stade du développement.
Quand l’ADN se compacte, le gène s’éveille
Dans des embryons normaux, les chercheurs ont observé qu’à l’approche du cycle nucléaire 13, les deux enhanceurs se rapprochent du PPE : le voisinage local d’ADN autour du gène brk devient plus compact. Après ce point, les distances entre les trois éléments restent relativement stables. Fait important, ce timing correspond au déclenchement de l’expression de brk, ce qui suggère que le resserrement de la configuration de l’ADN facilite l’activation du gène. PLOTTED a également révélé que cet agencement compact apparaît plus fréquemment dans les régions de l’embryon où brk est actif, tandis que des configurations plus lâches dominent là où le gène est réprimé, renforçant le lien entre architecture 3D et transcription.
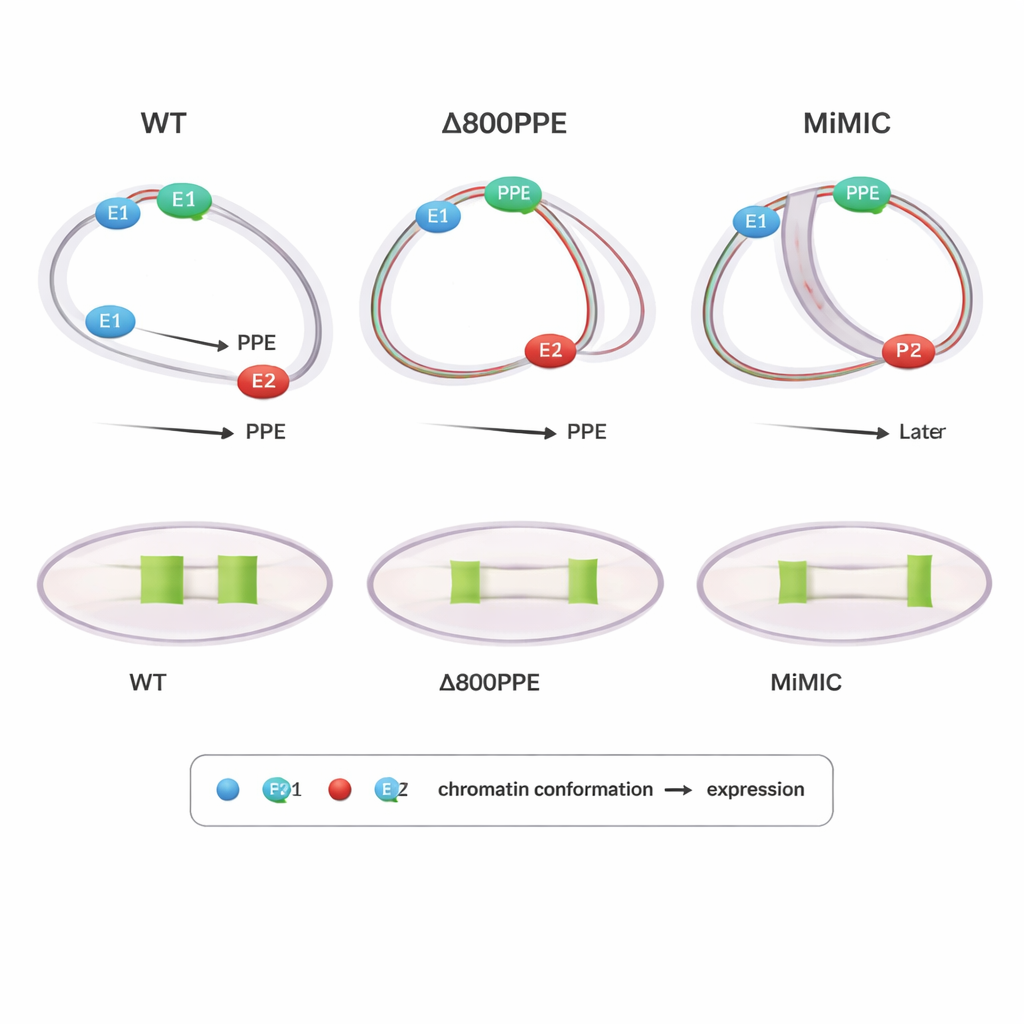
Les mutations révèlent l’importance du moment et de la position
Pour sonder la causalité, les auteurs ont examiné des mouches porteuses de modifications conçues au locus brk. Dans un mutant, 800 paires de bases du PPE ont été supprimées, affaiblissant cet élément central ; dans un autre, une cassette d’ADN de 7,3 kilobases (MiMIC) a été insérée entre E1 et le PPE, les éloignant effectivement et ajoutant un promoteur supplémentaire. Les deux mutants présentaient un retard ou une diminution de l’expression de brk. PLOTTED a montré pourquoi : dans la lignée avec suppression du PPE, la compaction des distances entre le PPE et les deux enhanceurs se produisait plus tard que la normale, et aux stades tardifs le PPE restait trop proche d’E1, empêchant E2 de générer le motif d’expression étendu observé à l’état sauvage. Dans la lignée MiMIC, le PPE s’associait trop tôt et trop fortement avec E2 puis ne se rapprochait d’E1 que plus tard, perturbant à nouveau le relais normal entre enhanceurs. Ces résultats suggèrent que ce n’est pas seulement si les éléments se rassemblent, mais aussi quand et avec quel partenaire ils sont le plus proches, qui est crucial pour une expression génique correcte.
Le repliement de l’ADN varie selon les régions de l’embryon
Parce que PLOTTED préserve l’information spatiale à l’intérieur d’embryons intacts, l’équipe a aussi pu comparer l’architecture de l’ADN dans différentes régions du corps. En comparant les zones latérales où brk est actif aux zones ventrales où il est réprimé, ils ont constaté que les trois éléments se tiennent plus près les uns des autres dans les régions actives et s’écartent davantage dans les domaines réprimés. Selon l’axe tête‑queue, ils ont observé que les distances E1–PPE évoluent différemment à l’avant et à l’arrière de l’embryon, ce qui laisse entendre que des indices régionaux ajustent l’architecture de la chromatine pour affiner les motifs d’expression génique. Ces observations soutiennent l’idée que l’agencement 3D de l’ADN régulateur dépend du contexte, suivant à la fois le temps et la position dans l’organisme en développement.
Pourquoi cela compte au‑delà des mouches
En termes simples, cette étude montre que la manière dont l’ADN se replie autour d’un gène unique est étroitement liée au moment et au lieu d’activation de ce gène. La nouvelle méthode PLOTTED offre une façon pratique de cartographier ces minuscules voisinages d’ADN dans des tissus intacts en utilisant des microscopes largement disponibles et une chimie simple, associée à un puissant modèle probabiliste. Bien que démontrée dans des embryons de mouche, l’approche peut être appliquée à de nombreux organismes et modèles de maladies. À mesure que les scientifiques découvrent que des anomalies du repliement de la chromatine sous-tendent des troubles du développement et des cancers, des outils comme PLOTTED aideront à dévoiler comment de petits déplacements dans la configuration 3D des enhanceurs et des gènes peuvent engendrer de grands changements de destin cellulaire et de santé.
Citation: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Mots-clés: architecture de la chromatine, interactions enhanceur‑promoteur, embryogenèse de Drosophila, régulation génique, imagerie super‑résolution